Bahan aktif: Fingolimod
Kapsul keras GILENYA 0.5 mg
Petunjuk Mengapa Gilenya digunakan? Untuk apa itu?
Apa itu Gilenya
Bahan aktif dalam Gilenya adalah fingolimod.
Untuk apa Gilenya
Gilenya digunakan pada orang dewasa untuk rawatan multiple sclerosis (MS) kambuh, terutama dalam:
Pesakit yang belum bertindak balas terhadap terapi dengan rawatan MS.
atau
Pesakit dengan MS teruk yang cepat berkembang.
Gilenya tidak menyembuhkan MS, tetapi membantu mengurangkan jumlah kambuh dan memperlambat perkembangan kecacatan fizikal yang disebabkan oleh MS.
Apa itu sklerosis berganda
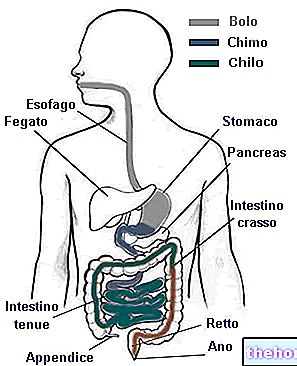
MS adalah penyakit kronik yang mempengaruhi sistem saraf pusat (CNS), yang merangkumi otak dan saraf tunjang. Di MS, keradangan menghancurkan sarung pelindung (disebut myelin) yang melapisi saraf di CNS dan mencegah saraf berfungsi sebagaimana mestinya.Proses ini disebut demyelination.
Relapsing-remitting MS dicirikan oleh serangan kambuh (kambuh) gejala neurologi yang mencerminkan keadaan keradangan sistem saraf pusat. Gejala bervariasi dari pesakit ke pesakit, tetapi biasanya melibatkan kesukaran berjalan, mati rasa, penglihatan atau gangguan keseimbangan. Gejala kambuh mungkin hilang sepenuhnya ketika kambuh berakhir, tetapi beberapa aduan mungkin berlanjutan.
Bagaimana Gilenya berfungsi
Gilenya membantu melindungi sistem saraf dari serangan sistem imun dengan mengurangkan keupayaan beberapa sel darah putih (limfosit) untuk beredar secara bebas di dalam badan dan menghalangnya daripada sampai ke otak dan saraf tunjang. Ini membatasi kerosakan saraf yang disebabkan oleh MS.
Kontraindikasi Bila Gilenya tidak boleh digunakan
Jangan ambil Gilenya
- jika anda mempunyai tindak balas imun yang berkurang (kerana sindrom imunodefisiensi, penyakit atau ubat-ubatan yang menekan sistem imun).
- jika anda mempunyai jangkitan berterusan yang teruk atau jangkitan berterusan kronik seperti hepatitis atau tuberkulosis.
- jika anda menghidap barah aktif (kecuali jika ia adalah sejenis barah kulit yang disebut barah sel sel basal).
- jika anda mempunyai masalah hati yang teruk.
- jika anda alah kepada fingolimod atau bahan-bahan lain dari ubat ini.
Sekiranya ada yang berlaku kepada anda, beritahu doktor anda sebelum mengambil Gilenya.
Langkah berjaga-jaga untuk penggunaan Apa yang perlu anda ketahui sebelum mengambil Gilenya
Bercakap dengan doktor anda sebelum mengambil Gilenya:
- jika anda mempunyai degupan jantung yang tidak teratur dan tidak normal.
- jika anda mengalami gejala degupan jantung yang rendah (seperti pening, loya atau berdebar).
- jika anda mempunyai masalah jantung, penyumbatan saluran darah di jantung anda, pernah mengalami serangan jantung atau serangan jantung pada masa lalu, atau mengalami angina.
- jika anda pernah mengalami strok pada masa lalu.
- sekiranya anda mengalami kegagalan jantung.
- sekiranya anda mengalami masalah pernafasan yang teruk semasa tidur (apnea tidur yang teruk).
- jika anda diberitahu bahawa anda mempunyai EKG yang tidak normal.
- jika anda mengambil atau baru-baru ini mengambil ubat untuk degupan jantung yang tidak teratur seperti quinidine, disopyramide, amiodarone atau sotalol.
- jika anda mengambil atau baru-baru ini mengambil ubat yang memperlahankan degupan jantung (seperti beta blocker, verapamil, diltiazem atau ivabradine, digoxin, ubat antikolinesterase atau pilocarpine).
- jika anda pernah mengalami episod kehilangan kesedaran atau pengsan secara tiba-tiba (sinkop).
- jika anda berhasrat untuk mendapat vaksin.
- jika anda tidak pernah menghidap cacar air.
- jika anda mengalami atau mengalami gangguan penglihatan atau tanda-tanda pembengkakan lain di kawasan penglihatan pusat (makula) di bahagian belakang mata (keadaan yang dikenali sebagai edema makula, lihat di bawah), jika anda mempunyai atau mengalami "radang atau" jangkitan pada mata (uveitis), atau jika anda menghidap diabetes (yang boleh menyebabkan masalah pada mata).
- sekiranya anda mempunyai masalah hati.
- jika anda mempunyai tekanan darah tinggi yang tidak dapat dikawal dengan ubat-ubatan.
- jika anda mempunyai masalah paru-paru yang teruk atau jika anda batuk akibat merokok.
Sekiranya ada yang berlaku kepada anda, beritahu doktor anda sebelum mengambil Gilenya.
Denyut jantung perlahan (bradikardia) dan degupan jantung tidak teratur: Pada permulaan rawatan, Gilenya menyebabkan penurunan degupan jantung. Akibatnya anda mungkin mengalami pening atau letih, kesedaran mengenai degupan jantung anda atau penurunan tekanan darah. Diucapkan, hubungi doktor, kerana anda mungkin memerlukan rawatan segera. Gilenya juga boleh menyebabkan degupan jantung tidak teratur, terutama selepas dos pertama. Denyutan jantung tidak teratur biasanya kembali normal dalam masa kurang dari satu hari. Denyutan jantung yang perlahan biasanya akan kembali. kembali normal dalam sebulan.
Doktor anda akan meminta anda tinggal di klinik atau hospital sekurang-kurangnya 6 jam setelah memberikan dos pertama Gilenya, di mana nadi dan tekanan darah anda akan diukur pada bila-bila masa: dengan cara ini, langkah-langkah yang sesuai dapat diambil sekiranya kesan sampingan yang berlaku pada awal rawatan. Anda mesti mempunyai elektrokardiogram sebelum dos pertama Gilenya dan pada akhir 6 jam pemantauan. Doktor anda boleh memeriksa elektrokardiogram anda secara berterusan dalam tempoh ini. Sekiranya selepas 6 o ' jam. kadar denyutan jantung anda sangat rendah atau menurun, atau jika EKG anda menunjukkan kelainan, anda mungkin perlu diperhatikan untuk jangka masa yang lebih lama (sekurang-kurangnya 2 jam lagi dan mungkin sehingga keesokan paginya), sehingga masalah ini dapat diselesaikan. perkara yang sama boleh berlaku jika dia mengambil G lagi ilenya selepas gangguan rawatan, bergantung pada berapa lama gangguan itu dan berapa lama anda mengambil Gilenya sebelum gangguan tersebut.
Sekiranya anda mempunyai atau berisiko mengalami degupan jantung yang tidak teratur atau tidak normal, jika EKG anda tidak normal, atau jika anda mempunyai penyakit jantung atau kegagalan jantung, Gilenya mungkin tidak sesuai untuk anda.
Sekiranya anda pernah mengalami episod kehilangan kesedaran secara tiba-tiba atau penurunan kadar jantung, Gilenya mungkin tidak sesuai untuk anda. Anda akan dijumpai oleh pakar kardiologi (pakar jantung) yang akan memberi nasihat mengenai cara memulakan rawatan dengan Gilenya, termasuk pemantauan hingga keesokan paginya.
Sekiranya anda mengambil ubat-ubatan yang boleh menyebabkan penurunan kadar jantung, Gilenya mungkin tidak sesuai untuk anda. Anda akan dilihat oleh pakar kardiologi yang akan menilai sama ada anda boleh mengambil ubat-ubatan yang tidak menurunkan kadar denyutan jantung anda sebagai alternatif dan membolehkan anda memulakan rawatan dengan Gilenya. Sekiranya perubahan dalam terapi ini tidak dapat dilakukan, pakar kardiologi anda akan memberi nasihat mengenai cara memulakan rawatan dengan Gilenya, termasuk pemantauan hingga keesokan harinya.
Sekiranya anda tidak pernah mengalami cacar air: Sekiranya anda tidak pernah mengalami cacar air, doktor anda akan memeriksa kekebalan anda terhadap virus yang menyebabkannya (virus varicella zoster). Sekiranya anda tidak dilindungi daripada virus, anda mungkin memerlukan vaksinasi sebelum memulakan rawatan dengan Gilenya. Sekiranya ini berlaku, doktor anda akan menangguhkan permulaan rawatan Gilenya sehingga satu bulan setelah menyelesaikan kursus vaksinasi sepenuhnya.
Jangkitan: Gilenya mengurangkan bilangan sel darah putih (terutamanya limfosit). Sel darah putih melawan jangkitan. Semasa mengambil Gilenya (dan sehingga 2 bulan setelah menghentikan rawatan), anda mungkin mendapat jangkitan dengan lebih mudah. Sebarang jangkitan yang ada boleh menjadi lebih teruk. Jangkitan boleh menjadi serius dan mengancam nyawa. Sekiranya anda fikir anda mempunyai jangkitan, jika anda demam, jika anda mempunyai gejala selesema, atau jika anda mengalami sakit kepala disertai leher kaku, kepekaan terhadap cahaya, mual dan / atau kekeliruan (ini boleh menjadi gejala meningitis), hubungi doktor segera.
Edema makula: Sebelum memulakan rawatan dengan Gilenya, jika anda mengalami atau mengalami gangguan penglihatan atau tanda-tanda bengkak lain di kawasan penglihatan pusat (makula) di bahagian belakang mata, jika anda mempunyai atau mengalami "inflamasi atau" jangkitan mata (uveitis) atau jika anda menghidap diabetes, doktor anda mungkin meminta anda menjalani pemeriksaan mata.
Doktor anda mungkin meminta anda menjalani pemeriksaan mata 3-4 bulan setelah memulakan rawatan dengan Gilenya.
Makula adalah kawasan kecil retina yang terletak di bahagian belakang mata yang membolehkan anda melihat bentuk, warna dan perincian dengan jelas dan tajam. Gilenya boleh menyebabkan pembengkakan makula, suatu keadaan yang dikenali sebagai edema makula. bengkak berlaku. biasanya pada 4 bulan pertama rawatan dengan Gilenya.
Edema makula lebih cenderung terjadi jika anda menghidap diabetes atau mengalami "radang mata" yang disebut uveitis. Dalam kes ini, doktor anda ingin memeriksa anda secara kerap untuk mengetahui tanda-tanda pertama edema makula.
Sekiranya anda mengalami edema makula, berbincanglah dengan doktor anda sebelum memulakan semula rawatan dengan Gilenya.
Edema makula boleh menyebabkan beberapa gejala visual (neuritis optik) yang juga berlaku semasa serangan MS. Pada peringkat awal mungkin tidak ada gejala. Pastikan anda memberitahu doktor mengenai perubahan penglihatan. Doktor anda mungkin meminta anda merujuknya menjalani pemeriksaan mata, terutamanya jika:
- kawasan pandangan tengah tidak fokus atau mempunyai bayang-bayang;
- titik buta berkembang di kawasan penglihatan pusat;
- menghadapi masalah untuk membezakan warna atau perincian halus.
Ujian fungsi hati: Sekiranya anda mempunyai masalah hati yang teruk, anda tidak boleh mengambil Gilenya. Rawatan dengan Gilenya boleh mempengaruhi fungsi hati anda. Anda mungkin tidak akan menyedari sebarang gejala, tetapi jika anda melihat menguningnya kulit atau putih mata anda, air kencing gelap yang tidak normal atau mual dan muntah yang tidak dapat dijelaskan, beritahu doktor anda dengan segera.
Sekiranya anda mendapat gejala ini setelah memulakan rawatan Gilenya, sila beritahu doktor anda dengan segera.
Selama dua belas bulan pertama rawatan, doktor anda akan meminta anda menjalani ujian darah untuk memeriksa fungsi hati anda. Sekiranya hasilnya menunjukkan bahawa ada masalah hati, rawatan dengan Gilenya mungkin perlu dihentikan.
Tekanan tinggi
Kerana Gilenya menyebabkan sedikit peningkatan tekanan darah, doktor anda mungkin memeriksa tekanan darah anda secara berkala. Masalah paru-paru Gilenya mempunyai kesan lemah terhadap fungsi paru-paru. Pada pesakit dengan masalah paru-paru yang teruk atau batuk akibat merokok, kesan sampingan mungkin berlaku dengan lebih mudah.
Kira-kira darah Kesan rawatan yang diingini dengan Gilenya adalah mengurangkan jumlah sel darah putih dalam darah. Ini biasanya akan kembali normal dalam 2 bulan setelah menghentikan rawatan. Sekiranya anda perlu menjalani ujian darah, beritahu doktor anda bahawa anda mengambil Gilenya .
Sebelum memulakan rawatan dengan Gilenya, doktor anda akan mengesahkan jika jumlah sel darah putih anda mencukupi, dan mungkin meminta anda mengulang kiraannya secara berkala. Sekiranya anda tidak mempunyai sel darah putih yang mencukupi, anda mungkin perlu berhenti mengambil Gilenya.
Sindrom ensefalopati terbalik posterior (PRES)
Sindrom yang disebut ensefalopati posterior reversibel (PRES) jarang dilaporkan pada pesakit dengan sklerosis berganda yang dirawat dengan Gilenya. Gejala boleh merangkumi timbulnya sakit kepala yang teruk secara tiba-tiba, kekeliruan, kejang, dan perubahan penglihatan. Beritahu doktor anda jika ada gejala ini berlaku semasa rawatan dengan Gilenya.
Gunakan pada orang tua
Pengalaman dengan Gilenya pada pesakit tua yang berusia lebih dari 65 tahun adalah terhad. Sekiranya anda mempunyai pertanyaan lebih lanjut, tanyakan kepada doktor anda.
Kanak-kanak dan remaja
Gilenya tidak dimaksudkan untuk digunakan pada kanak-kanak dan remaja di bawah 18 tahun kerana belum dipelajari pada pesakit MS di bawah usia 18 tahun.
Interaksi Dadah atau makanan mana yang boleh mengubah kesan Gilenya
Beritahu doktor atau ahli farmasi anda jika anda mengambil, baru-baru ini mengambil atau mungkin mengambil ubat lain. Beritahu doktor anda jika anda mengambil ubat berikut:
- Ubat yang menekan atau mengubah sistem imun, termasuk ubat lain yang digunakan untuk merawat MS, seperti interferon beta, glatiramer asetat, natalizumab, mitoxantrone, teriflunomide, dimethyl fumarate atau alemtuzumab. Anda tidak boleh menggunakan Gilenya dengan ubat-ubatan ini kerana boleh meningkatkan kesan pada sistem imun (lihat juga "Jangan mengambil Gilenya").
- Kortikosteroid, kerana kemungkinan kesan tambahan pada sistem imun.
- Vaksin-vaksin. Sekiranya anda perlu melakukan vaksinasi, minta nasihat doktor terlebih dahulu. Selama dan hingga 2 bulan setelah rawatan dengan Gilenya, Anda tidak boleh menerima beberapa jenis vaksin (vaksin yang dilemahkan secara langsung) kerana boleh memicu jangkitan yang seharusnya mereka cegah. Vaksin lain mungkin tidak berfungsi seperti biasa jika diberikan pada waktu ini .
- Ubat yang memperlahankan degupan jantung (seperti beta-blocker, seperti atenolol). Penggunaan Gilenya secara bersamaan dengan ubat-ubatan ini dapat meningkatkan kesan pada degupan jantung pada hari-hari pertama rawatan Gilenya.
- Ubat untuk degupan jantung yang tidak teratur, seperti quinidine, disopyramide, amiodarone atau sotalol. Doktor anda mungkin memutuskan untuk tidak menetapkan Gilenya jika anda mengambil ubat jenis ini kerana boleh meningkatkan kesan pada degupan jantung yang tidak teratur.
- Ubat-ubatan lain:
- inhibitor protease, anti-infeksi seperti ketoconazole, antifungals azole, clarithromycin atau telithromycin.
- carbamazepine, rifampicin, phenobarbital, phenytoin, efavirenz atau St. John's wort (potensi risiko berkurangnya keberkesanan).
Amaran Penting untuk mengetahui bahawa:
Kehamilan dan penyusuan
Sebelum memulakan rawatan dengan Gilenya, doktor anda mungkin meminta anda menjalani ujian kehamilan untuk memastikan anda tidak hamil. Semasa mengambil Gilenya atau selama dua bulan setelah menghentikan rawatan, anda harus mengelakkan hamil kerana terdapat risiko membahayakan bayi. Bercakap dengan doktor anda mengenai kaedah kontrasepsi yang boleh digunakan semasa rawatan. Dengan Gilenya dan selama 2 bulan setelah menghentikan rawatan. .
Sekiranya anda hamil semasa mengambil Gilenya, hentikan rawatan dan beritahu doktor anda dengan segera. Doktor anda akan memutuskan apa yang terbaik untuk anda dan bayi anda.
Jangan menyusu semasa mengambil Gilenya. Gilenya dikeluarkan dalam susu ibu dengan risiko kesan sampingan yang serius bagi bayi yang baru lahir.
Minta nasihat doktor atau ahli farmasi anda sebelum mengambil sebarang ubat.
Memandu dan menggunakan mesin
Doktor anda akan memberitahu anda jika penyakit anda membolehkan anda memandu dan menggunakan mesin dengan selamat. Gilenya tidak diharapkan dapat mempengaruhi kemampuan memandu dan menggunakan mesin.
Walau bagaimanapun, pada permulaan rawatan, anda perlu tinggal di pejabat atau hospital doktor anda selama 6 jam setelah mengambil dos pertama Gilenya. Keupayaan untuk memandu dan menggunakan mesin mungkin terganggu selama ini dan berpotensi melebihi.
Dos dan kaedah penggunaan Cara penggunaan Gilenya: Dos
Rawatan dengan Gilenya akan diawasi oleh doktor yang berpengalaman dalam rawatan multiple sclerosis.
Sentiasa ambil ubat ini tepat seperti yang diberitahu oleh doktor anda.
Sekiranya ragu-ragu, berjumpa doktor. Dosnya adalah satu kapsul sekali sehari. Ambil Gilenya sekali sehari dengan segelas air.Gilenya boleh diambil dengan atau tanpa makanan.
Mengambil Gilenya pada waktu yang sama setiap hari akan membantu anda mengingat kapan mengambil ubat tersebut.
Jangan melebihi dos yang disyorkan.
Doktor anda boleh menukar anda secara langsung dari rawatan dengan interferon beta, glatiramer acetate atau dimethyl fumarate ke Gilenya jika tidak ada tanda-tanda kelainan yang disebabkan oleh rawatan sebelumnya. Doktor anda mungkin meminta anda melakukan ujian darah untuk mengesahkan keabnormalan ini. Selepas menghentikan natalizumab, perlu menunggu 2-3 bulan sebelum memulakan rawatan dengan Gilenya. Untuk beralih dari teriflunomide, doktor anda mungkin menasihati anda untuk menunggu sejumlah waktu atau untuk meneruskan prosedur penghapusan yang dipercepat. Sekiranya anda telah dirawat dengan alemtuzumab, penilaian dan perbincangan yang teliti dengan doktor anda diperlukan untuk memutuskan apakah Gilenya sesuai untuk anda.
Sekiranya anda tidak pasti berapa lama anda akan mengambil Gilenya, tanyakan kepada doktor atau ahli farmasi anda.
Overdosis Apa yang perlu dilakukan jika anda mengambil terlalu banyak Gilenya
Sekiranya anda mengambil lebih banyak Gilenya daripada yang sepatutnya
Sekiranya anda mengambil terlalu banyak kapsul Gilenya, beritahu doktor anda dengan segera.
Sekiranya anda terlupa mengambil Gilenya
Sekiranya anda mengambil Gilenya kurang dari 1 bulan dan lupa mengambil 1 dos selama sehari penuh, berbincanglah dengan doktor anda sebelum mengambil dos seterusnya. Doktor anda mungkin memutuskan untuk memerhatikan anda apabila anda mengambil dos seterusnya.
Sekiranya anda mengambil Gilenya selama sekurang-kurangnya 1 bulan dan terlupa mengambil ubat anda selama lebih dari 2 minggu, berbincanglah dengan doktor anda sebelum mengambil dos seterusnya. Doktor anda mungkin memutuskan untuk memerhatikan anda apabila anda mengambil dos seterusnya. Namun, jika anda terlupa mengambil ubat anda selama 2 minggu atau kurang, anda boleh mengambil dos seterusnya seperti yang dirancang.
Jangan sekali-kali mengambil dos berganda untuk menebus dos yang dilupakan.
Sekiranya anda berhenti mengambil Gilenya
Jangan berhenti mengambil Gilenya atau menukar dos anda tanpa terlebih dahulu bercakap dengan doktor anda.
Gilenya akan kekal di dalam badan sehingga 2 bulan setelah menghentikan rawatan. Jumlah sel darah putih (limfosit) mungkin tetap rendah selama ini dan kesan sampingan yang dijelaskan dalam risalah ini mungkin masih berlaku. Setelah menghentikan rawatan Gilenya, perlu menunggu 6-8 minggu sebelum memulakan rawatan baru untuk sklerosis berganda.
Sekiranya anda perlu menghidupkan semula Gilenya setelah lebih dari 2 minggu menghentikan rawatan, kesan pada degupan jantung yang biasanya berlaku pada permulaan rawatan boleh berlaku lagi.rumah sakit di bawah pemerhatian Jangan mulakan semula Gilenya setelah menghentikannya selama lebih dari dua minggu tanpa berunding dengan doktor.
Sekiranya anda mempunyai pertanyaan lebih lanjut mengenai penggunaan ubat ini, tanyakan kepada doktor atau ahli farmasi anda
Kesan Sampingan Apakah kesan sampingan Gilenya
Seperti semua ubat, ubat ini boleh menyebabkan kesan sampingan, walaupun tidak semua orang mendapatnya.
Beberapa kesan sampingan boleh menjadi serius
Biasa (boleh mempengaruhi sehingga 1 dari 10 orang):
- Batuk dengan kahak, ketidakselesaan dada, demam (tanda-tanda gangguan paru-paru)
- Jangkitan virus herpes (St. Anthony's fire atau herpes zoster), dengan gejala seperti melepuh, terbakar, gatal-gatal, atau sakit pada kulit, biasanya di bahagian atas badan atau di wajah. Gejala lain mungkin demam dan lemah pada peringkat awal jangkitan, diikuti dengan rasa mati rasa, gatal-gatal, atau bintik-bintik merah dengan kesakitan yang teruk
- Denyutan jantung yang perlahan (bradikardia), irama jantung yang tidak teratur
Tidak biasa (boleh mempengaruhi sehingga 1 dari 100 orang):
- Pneumonia dengan gejala seperti demam, batuk, sukar bernafas
- Edema makula (bengkak di kawasan penglihatan pusat retina di bahagian belakang mata) dengan gejala seperti bayang-bayang atau bintik-bintik buta di pusat penglihatan, penglihatan kabur, masalah membezakan warna atau perincian
Jarang (boleh mempengaruhi sehingga 1 dari 1000 orang):
- Sindrom yang disebut ensefalopati posterior terbalik. Gejala boleh merangkumi timbulnya sakit kepala yang teruk secara tiba-tiba, kekeliruan, sawan dan / atau gangguan penglihatan
Kes terpencil:
- Jangkitan kriptokokus (sejenis jangkitan kulat), termasuk meningitis kriptokokus dengan gejala seperti sakit kepala disertai kekakuan leher, kepekaan terhadap cahaya, mual dan / atau kekeliruan.
Sekiranya anda mendapat kesan sampingan ini, beritahu doktor anda dengan segera.
Kesan sampingan yang lain
Sangat biasa (boleh mempengaruhi lebih daripada 1 dari 10 orang):
- Jangkitan virus influenza dengan gejala seperti keletihan, menggigil, sakit tekak, sakit sendi atau otot, demam
- Rasa tekanan atau sakit di pipi dan dahi (sinusitis)
- Sakit kepala
- Cirit-birit
- Sakit belakang
- Ujian darah menunjukkan tahap enzim hati yang lebih tinggi
- Batuk
Biasa (boleh mempengaruhi sehingga 1 dari 10 orang):
- Kurap, "jangkitan kulat pada kulit (pityriasis versicolor)
- Pening
- Sakit kepala yang teruk sering disertai dengan loya, muntah dan kepekaan terhadap cahaya (migrain)
- Tahap rendah sel darah putih (limfosit, leukosit)
- Kelemahan
- Ruam kulit dengan gatal, kemerahan dan terbakar (eksim)
- Gatal-gatal
- Peningkatan tahap lemak (trigliserida) dalam darah
- Keguguran rambut
- Mengi
- Kemurungan
- Penglihatan kabur (lihat juga bahagian "edema makula" Beberapa kesan sampingan mungkin atau menjadi serius ")
- Hipertensi (Gilenya boleh menyebabkan sedikit peningkatan tekanan darah)
Tidak biasa (boleh mempengaruhi sehingga 1 dari 100 orang):
- Tahap rendah beberapa sel darah putih (neutrofil)
- Suasana tertekan
Jarang (boleh mempengaruhi sehingga 1 dari 1000 orang):
- Gangguan saluran darah
- Gangguan sistem saraf
- Kanser sistem limfa (limfoma)
Tidak diketahui (frekuensi tidak dapat dianggarkan dari data yang tersedia):
- Reaksi alergi dan ruam kulit
Sekiranya ada kesan sampingan ini, sila beritahu doktor anda.
Melaporkan kesan sampingan
Sekiranya anda mendapat kesan sampingan, berbincanglah dengan doktor atau ahli farmasi anda. Ini termasuk kemungkinan kesan sampingan yang tidak disenaraikan dalam risalah ini. Anda juga boleh melaporkan kesan sampingan secara langsung melalui sistem pelaporan nasional yang disenaraikan dalam Lampiran V. Dengan melaporkan kesan sampingan, anda dapat membantu memberikan lebih banyak maklumat mengenai keselamatan ubat ini.
Tamat Tempoh dan Pengekalan
Jauhkan ubat ini dari pandangan dan jangkauan kanak-kanak.
Jangan gunakan ubat ini selepas tarikh luput yang dinyatakan pada kadbod dan lepuh selepas "EXP" / "EXP". Tarikh luput merujuk pada hari terakhir bulan itu.
Jangan simpan di atas 25ºC.
Simpan dalam bungkusan asal untuk melindungi ubat daripada kelembapan.
Jangan gunakan pakej yang rosak atau menunjukkan tanda-tanda gangguan.
Jangan buang ubat melalui air buangan atau sampah rumah. Tanya ahli farmasi anda bagaimana membuang ubat yang tidak lagi anda gunakan. Ini akan membantu melindungi alam sekitar.
Apa yang dikandung oleh Gilenya
- Bahan aktifnya adalah fingolimod. Setiap kapsul mengandungi 0.5 mg fingolimod (sebagai hidroklorida).
- Bahan-bahan lain adalah: Kandungan kapsul: magnesium stearate, mannitol Shell capsule: iron iron oxide (E172), titanium dioxide (E171), gelatin Ink: lacquer (E904), dehydrated alcohol, isopropyl alcohol, butyl alcohol, propylene glycol, purified water , larutan ammonia pekat, kalium hidroksida, oksida besi hitam (E172), oksida besi kuning (E172), titanium dioksida (E171), dimeticone
Seperti apa Gilenya dan kandungan peknya
Kapsul keras Gilenya 0,5 mg mempunyai badan legap putih legap dan penutup legap kuning pekat. Tulisan hitam "FTY0,5mg" terukir di kepala dan dua jalur kuning terukir di badan.
Gilenya tersedia dalam pek yang mengandungi 7, 28 atau 98 kapsul, atau dalam bungkusan yang mengandungi 84 kapsul (3 bungkus dari 28 kapsul). Tidak semua saiz pek boleh dipasarkan.
Risalah Pakej Sumber: AIFA (Badan Perubatan Itali). Kandungan yang diterbitkan pada Januari 2016. Maklumat yang ada mungkin tidak terkini.
Untuk mempunyai akses ke versi paling terkini, disarankan untuk mengakses laman web AIFA (Badan Perubatan Itali). Penafian dan maklumat berguna.
01.0 NAMA PRODUK PERUBATAN
CAPSULES GILENYA 0.5 MG
Product Produk ubat tertakluk kepada pemantauan tambahan. Ini akan membolehkan pengenalan maklumat keselamatan baru dengan cepat. Para profesional penjagaan kesihatan diminta untuk melaporkan sebarang reaksi buruk yang disyaki. Lihat bahagian 4.8 untuk maklumat mengenai cara melaporkan reaksi buruk.
02.0 KOMPOSISI KUALITATIF DAN KUANTITATIF
Setiap kapsul keras mengandungi 0.5 mg fingolimod (sebagai hidroklorida).
Untuk senarai lengkap eksipien, lihat bahagian 6.1.
03.0 BORANG FARMASI
Kapsul keras.
Kapsul 16 mm dengan penutup legap kuning dan badan legap putih; ukiran hitam "FTY0.5 mg" di kepala dan dua jalur kuning bulat yang terukir di badan.
04.0 MAKLUMAT KLINIKAL
04.1 Petunjuk terapeutik
Gilenya ditunjukkan dengan sendirinya, sebagai ubat pengubah penyakit, dalam pelbagai sklerosis berulang yang sangat aktif dalam kumpulan pesakit dewasa berikut:
- Pesakit dengan aktiviti penyakit tinggi walaupun menjalani rawatan dengan sekurang-kurangnya satu terapi pengubahsuaian penyakit (lihat bahagian 4.4 dan 5.1 untuk pengecualian dan maklumat mengenai pencucian).
Pesakit ini dapat didefinisikan sebagai mereka yang belum menanggapi terapi yang lengkap dan mencukupi (biasanya sekurang-kurangnya satu tahun rawatan) dengan sekurang-kurangnya satu terapi pengubahsuaian penyakit. Pesakit mesti mengalami sekurang-kurangnya 1 kambuh pada tahun sebelumnya semasa menjalani terapi, dan mempunyai sekurang-kurangnya 9 lesi hipertensi T2 pada MRI otak atau sekurang-kurangnya 1 lesi peningkatan gadolinium. bukan responden ia juga boleh didefinisikan sebagai pesakit yang mempunyai kadar kambuh yang tidak berubah atau meningkat berbanding tahun sebelumnya atau yang mengalami kambuh yang teruk.
atau
- Pesakit dengan sklerosis kambuh-remitting yang teruk yang cepat berkembang, yang ditakrifkan oleh dua atau lebih relaps yang melumpuhkan dalam satu tahun, dan dengan 1 atau lebih lesi peningkatan gadolinium pada MRI otak atau dengan peningkatan beban lesi T2 yang ketara berbanding MRI sebelumnya baru-baru ini dijalankan.
04.2 Posologi dan kaedah pentadbiran
Rawatan harus dimulakan dan diawasi oleh doktor yang berpengalaman dalam pelbagai sklerosis.
Dos
Dos Gilenya yang disyorkan adalah satu kapsul 0,5 mg yang diambil secara lisan sekali sehari. Gilenya boleh diambil semasa makan dan menjauhi makanan.
Dianjurkan untuk melakukan pemantauan yang sama seperti pada permulaan rawatan setelah dos pertama jika rawatan dihentikan untuk:
• 1 atau lebih hari selama dua minggu pertama rawatan
• lebih dari 7 hari selama minggu ketiga dan keempat rawatan
• lebih dari 2 minggu selepas satu bulan rawatan.
Sekiranya gangguan rawatan lebih lama daripada yang dijelaskan di atas, rawatan harus diteruskan dengan pemberian dos berikutnya seperti yang direncanakan (lihat bahagian 4.4).
Populasi khas
Warga emas
Gilenya harus digunakan dengan hati-hati pada pasien yang berusia 65 tahun dan lebih tua kerana data dan keselamatan yang mencukupi tidak tersedia (lihat bahagian 5.2).
Fungsi buah pinggang terjejas
Dalam kajian penting utama yang dilakukan dalam sklerosis berganda, Gilenya belum dikaji pada pesakit dengan gangguan fungsi ginjal. Berdasarkan kajian farmakologi klinikal, tidak diperlukan penyesuaian dos pada pesakit dengan gangguan ginjal ringan hingga teruk.
Fungsi hati terjejas
Gilenya tidak boleh digunakan pada pesakit dengan gangguan hati yang teruk (Child-Pugh kelas C) (lihat bahagian 4.3). Walaupun tidak diperlukan penyesuaian dos pada pasien dengan gangguan hati ringan atau sederhana, berhati-hati disarankan ketika memulai perawatan pada pasien ini (lihat bahagian 4.4 dan 5.2).
Pesakit diabetes
Gilenya belum dipelajari pada pesakit dengan sklerosis berganda dan diabetes mellitus. Gilenya harus digunakan dengan berhati-hati pada pesakit ini kerana kemungkinan peningkatan risiko edema makula (lihat bahagian 4.4 dan 4.8). Pesakit ini harus menjalani pemeriksaan oftalmologi secara berkala untuk tanda-tanda edema makula.
Populasi kanak-kanak
Keselamatan dan keberkesanan Gilenya pada anak-anak berusia 0-18 tahun belum terbukti. Data yang ada saat ini dijelaskan di bahagian 5.2 tetapi tidak ada cadangan mengenai posologi yang dapat dibuat.
04.3 Kontraindikasi
- Sindrom imunodefisiensi yang didiagnosis.
- Pesakit yang mempunyai peningkatan risiko jangkitan oportunistik, termasuk pesakit imunokompromis (termasuk mereka yang dirawat dengan terapi imunosupresif bersamaan atau mereka yang dikompromikan oleh terapi sebelumnya).
- Jangkitan aktif yang teruk, jangkitan aktif kronik (hepatitis, tuberkulosis).
- Diagnosis tumor ganas aktif, kecuali pesakit dengan kanser kulit sel basal.
- Kerosakan hati yang teruk (Child-Pugh kelas C).
- Hipersensitiviti terhadap bahan aktif atau salah satu daripada eksipien yang disenaraikan dalam bahagian 6.1.
04.4 Amaran khas dan langkah berjaga-jaga yang sesuai untuk digunakan
Bradyarrhythmia
Permulaan rawatan Gilenya mengakibatkan penurunan kadar denyutan jantung sementara dan mungkin juga dikaitkan dengan kelewatan pengaliran atrioventricular, termasuk episod terpencil yang lengkap, sementara dan menyelesaikan sekatan atrioventrikular (lihat bahagian 4.8 dan 5.1).
Selepas pemberian dos pertama, penurunan kadar jantung bermula dalam satu jam dan maksimum dalam 6 jam pertama. Pada hari-hari berikutnya kesan pasca-dos ini berterusan, walaupun pada amnya kurang intensiti, dan biasanya menurun pada minggu-minggu berikutnya Dengan pentadbiran yang berterusan, kadar denyutan jantung rata-rata kembali ke tahap awal dalam satu bulan. Walau bagaimanapun, pada pesakit tertentu, degupan jantung mungkin tidak akan kembali ke awal pada akhir bulan pertama. Kelainan konduksi biasanya bersifat sementara dan tidak simptomatik. Umumnya tidak diperlukan rawatan dan diselesaikan dalam 24 jam pertama selepas memulakan rawatan. Sekiranya perlu, penurunan kadar denyutan jantung yang disebabkan oleh fingolimod dapat diterbalikkan dengan pemberian dosis atropin atau isoprenalin secara parenteral.
Semua pesakit harus menjalani pengukuran tekanan darah dan elektrokardiogram sebelum dos pertama Gilenya dan selepas 6 jam. Semua pesakit harus dipantau selama 6 jam untuk tanda-tanda dan gejala bradikardia, dengan pengukuran kadar denyutan jantung dan tekanan darah setiap jam. Pemantauan ECG berterusan (masa nyata) disyorkan selama 6 jam ini.
Sekiranya gejala bradyarrhythmia berlaku selepas pentadbiran, prosedur pengurusan pesakit klinikal yang sesuai harus dimulakan dan pemantauan berlanjutan sehingga gejala dapat diselesaikan. Sekiranya pesakit memerlukan campur tangan farmakologi semasa pemantauan setelah dosis pertama, pemantauan harus dilakukan hingga keesokan harinya di rumah sakit dan harus diulang setelah dos kedua Gilenya.
Sekiranya, pada akhir 6 jam, nilai degupan jantung adalah yang terendah setelah dos pertama (menunjukkan bahawa kesan farmakodinamik maksimum pada jantung belum dapat dilihat), pemantauan harus diteruskan sekurang-kurangnya 2 jam dan hingga jantung kadar meningkat lagi. Pemantauan tambahan juga diperlukan (sekurang-kurangnya hingga keesokan harinya dan dalam kes apa pun sehingga gejala diselesaikan) jika, setelah 6 jam dari pemberian dos pertama, degupan jantung berdegup seminit, atau jika elektrokardiogram menunjukkan permulaan tahap kedua atau blok atrioventrikular yang lebih tinggi, atau jika selang QTc adalah ≥500 msec. Permulaan blok atrioventrikular darjah ketiga pada bila-bila masa juga mesti menyebabkan berlakunya pemantauan (sekurang-kurangnya hingga keesokan harinya).
Oleh kerana risiko gangguan irama yang teruk, Gilenya tidak boleh digunakan pada pesakit dengan Mobitz jenis II darjah kedua atau blok atrioventricular yang lebih tinggi, pada pesakit dengan sindrom sinus sakit atau blok sino-atrium, sejarah bradikardia simptomatik atau sinkop berulang, atau pada pesakit dengan pemanjangan QT yang ketara (QTc> 470 msec (wanita) atau> 450 msec (lelaki)). Oleh kerana bradikardia yang ketara dapat ditoleransi dengan buruk pada pesakit dengan penyakit jantung iskemia yang diketahui (termasuk angina pectoris), penyakit serebrovaskular, sejarah infark miokard, kegagalan jantung kongestif, sejarah penangkapan jantung, hipertensi yang tidak terkawal atau apnea tidur yang teruk, Gilenya tidak boleh digunakan pesakit-pesakit ini. Rawatan dengan Gilenya hanya dapat dipertimbangkan pada pesakit ini jika manfaat yang diharapkan melebihi risiko yang mungkin terjadi; jika diputuskan untuk memulakan terapi dengan Gilenya, seorang pakar kardiologi harus berunding sebelum memulakan rawatan untuk menentukan pemantauan yang paling tepat. Pemantauan disarankan sekurang-kurangnya hingga keesokan harinya untuk permulaan rawatan (lihat juga bahagian 4.5).
Gilenya belum dipelajari pada pesakit dengan aritmia yang memerlukan rawatan dengan kelas Ia (mis. Quinidine, disopyramide) atau kelas III (mis. Amiodarone, sotalol) antiaritmia. Antiarrhythmics Kelas Ia dan kelas III telah dikaitkan dengan kes torsades de pointes pada pesakit dengan bradikardia. Oleh kerana permulaan rawatan dengan Gilenya mengakibatkan penurunan detak jantung, Gilenya tidak boleh digunakan bersamaan dengan ubat-ubatan ini.
Pengalaman dengan Gilenya pada pesakit dengan rawatan bersamaan dengan beta-blocker, penyekat saluran kalsium yang menyebabkan penurunan kadar jantung (seperti verapamil, diltiazem atau ivabradine), atau dengan ubat lain yang dapat menurunkan kadar jantung (misalnya digoxin, ubat antikolinesterase atau pilocarpine) Oleh kerana permulaan rawatan Gilenya juga dikaitkan dengan penurunan kadar jantung (lihat juga bahagian 4.8 Bradyarrhythmia), penggunaan ubat-ubatan ini secara bersamaan pada permulaan rawatan Gilenya mungkin dikaitkan dengan bradikardia dan sekatan jantung yang teruk. Oleh kerana potensi kesan tambahan pada degupan jantung, rawatan dengan Gilenya tidak boleh dimulakan pada pasien yang menerima ubat ini (lihat juga bahagian 4.5). Pada pesakit ini, rawatan dengan Gilenya hanya dapat dipertimbangkan jika manfaat yang diharapkan melebihi risiko yang mungkin terjadi. Sekiranya terapi dengan Gilenya dipertimbangkan, disarankan agar ahli kardiologi berunding sebelum memulakan rawatan untuk mempertimbangkan beralih ke produk ubat lain yang tidak menyebabkan penurunan kadar jantung. Sekiranya tidak mungkin untuk menghentikan rawatan dengan ubat-ubatan ini, seorang pakar kardiologi harus berkonsultasi untuk menentukan pemantauan yang mencukupi pada permulaan rawatan. Pemantauan sekurang-kurangnya hingga keesokan harinya dianjurkan (lihat juga bahagian 4.5).
Bergantung pada jangka masa gangguan dan tempoh rawatan (masa antara permulaan rawatan dan penghentiannya), kesan pada degupan jantung dan pengaliran atrioventrikular dapat kembali apabila rawatan dengan Gilenya dimulakan semula. Dianjurkan untuk melakukan pemantauan yang sama seperti pada permulaan rawatan setelah dos pertama jika rawatan dihentikan untuk:
• 1 atau lebih hari selama dua minggu pertama rawatan
• lebih dari 7 hari selama minggu ketiga dan keempat rawatan
• lebih dari 2 minggu selepas satu bulan rawatan.
Sekiranya gangguan rawatan lebih lama daripada yang dijelaskan di atas, rawatan harus diteruskan dengan pemberian dos seterusnya seperti yang dirancang.
Selang QT
Dalam kajian selang QT menyeluruh yang dilakukan dengan dosis fingolimod 1,25 mg atau 2,5 mg, pada keadaan stabil (ketika kesan kronotropik negatif dari fingolimod masih ada), rawatan dengan fingolimod menyebabkan pemanjangan dos. Selang QT yang diperbetulkan (QTc), dengan had atas 90% selang keyakinan ≤ 13.0 ms. Tidak ada hubungan dos-tindak balas atau pendedahan-tindak balas yang diamati antara pemanjangan selang fingolimod dan QTc., Baik sebagai nilai mutlak maupun sebagai perubahan dari garis dasar.
Kepentingan klinikal penemuan ini tidak diketahui. Tidak ada pemanjangan selang QT yang signifikan secara klinis dalam kajian pada pasien dengan sklerosis berganda, tetapi pesakit yang berisiko mengembangkan pemanjangan selang QT tidak termasuk dalam ujian klinikal.
Produk ubat yang dapat memanjangkan selang QTc harus dielakkan pada pesakit dengan faktor risiko yang signifikan, seperti hipokalaemia atau pemanjangan selang QT kongenital.
Jangkitan
Kesan farmakodinamik Gilenya yang relevan adalah pengurangan bergantung kepada dos dalam limfosit periferi hingga 20-30% dari nilai awal. Ini disebabkan oleh penyerapan limfosit yang boleh dibalikkan dalam tisu limfoid (lihat bahagian 5.1).
Jumlah darah lengkap baru-baru ini (iaitu diambil dalam masa 6 bulan sebelum atau setelah menghentikan terapi sebelumnya) harus ada sebelum memulakan rawatan dengan Gilenya. Dianjurkan juga semasa rawatan untuk menilai jumlah darah secara berkala selepas 3 bulan dan sekurang-kurangnya setiap tahun selepas itu, dan sekiranya timbul tanda-tanda jangkitan. Kiraan limfosit mutlak di bawah 0.2x109 / l, jika disahkan, harus menyebabkan penghentian. kembali normal, kerana fingolimod dihentikan dalam ujian klinikal pada pesakit dengan jumlah limfosit mutlak di bawah 0.2x109 / l.
Permulaan rawatan dengan Gilenya harus ditangguhkan pada pesakit dengan jangkitan teruk yang berterusan sehingga pemulihan.
Pesakit harus dinilai status imuniti mereka untuk cacar air sebelum memulakan rawatan dengan Gilenya. Sekiranya tidak ada riwayat cacar air yang disahkan oleh doktor atau bukti kursus vaksinasi varicella yang lengkap, disarankan agar pesakit diuji antibodi terhadap virus varicella-zoster (VZV) sebelum memulakan terapi Gilenya. Bagi pesakit dengan titri antibodi negatif, disyorkan kursus vaksinasi lengkap terhadap varicella sebelum memulakan rawatan dengan Gilenya (lihat bahagian 4.8).Permulaan rawatan dengan Gilenya harus ditunda selama 1 bulan agar vaksinasi menjadi efektif sepenuhnya.
Kesan Gilenya pada sistem imun boleh meningkatkan risiko jangkitan (lihat bahagian 4.8). Strategi diagnostik dan terapi yang berkesan harus dilaksanakan pada pesakit yang dirawat dengan Gilenya yang mengalami gejala jangkitan. Pesakit harus diarahkan untuk melaporkan gejala jangkitan kepada doktor mereka semasa menjalani rawatan dengan Gilenya.
Sekiranya terdapat jangkitan yang teruk pada pesakit, penghentian terapi Gilenya harus dipertimbangkan dan keseimbangan risiko-manfaat harus dinilai sebelum melanjutkan rawatan.
Penghapusan fingolimod setelah pemberhentian terapi mungkin memakan masa hingga dua bulan dan oleh itu kawalan jangkitan harus dilakukan selama tempoh ini. Pesakit harus diarahkan untuk melaporkan gejala jangkitan dalam masa dua bulan setelah menghentikan fingolimod.
Edema makula
Edema makula dengan atau tanpa gangguan penglihatan telah dilaporkan pada 0,5% pesakit yang dirawat dengan 0,5 mg fingolimod, terutama pada 3-4 bulan pertama terapi (lihat bahagian 4.8). Oleh itu, penilaian oftalmologi disarankan 3-4 bulan setelah permulaan rawatan.Jika pesakit melaporkan gangguan penglihatan pada bila-bila masa semasa rawatan, pemeriksaan fundus, termasuk makula, harus dilakukan.
Pesakit dengan sejarah uveitis dan pesakit diabetes mellitus berisiko tinggi mengalami edema makula (lihat bahagian 4.8). Gilenya belum dikaji pada pesakit dengan sklerosis berganda dan diabetes mellitus bersamaan. Adalah disyorkan bahawa pesakit dengan sklerosis berganda dan diabetes mellitus bersamaan atau dengan riwayat uveitis menjalani penilaian oftalmologi sebelum memulakan terapi dan pemeriksaan susulan semasa rawatan.
Lanjutan rawatan Gilenya pada pesakit dengan edema makula belum dipelajari. Sebaiknya rawatan Gilenya dihentikan sekiranya edema makula terjadi pada pesakit. Dalam memutuskan sama ada terapi Gilenya harus disambung semula setelah sembuh, kemungkinan manfaat dan risiko bagi setiap pesakit harus dipertimbangkan.
Fungsi hati
Peningkatan enzim hati, terutama alanine aminotransferase (ALT) tetapi juga gamma glutamyltranspeptidase (GGT) dan aspartate transaminase (AST) telah dilaporkan pada pesakit dengan sklerosis berganda yang dirawat dengan Gilenya. Dalam ujian klinikal, peningkatan ALT ≥3 kali had atas had normal (ULN) berlaku pada 8.0% pesakit yang dirawat dengan fingolimod 0.5 mg berbanding dengan 1.9% pesakit yang dirawat dengan plasebo. Peningkatan 5 kali had atas julat normal berlaku pada 1.8% pesakit yang dirawat dengan fingolimod dan pada 0.9% pesakit yang dirawat dengan plasebo.Dalam percubaan klinikal, rawatan dengan fingolimod dihentikan jika kenaikan> 5 kali batas atas dari rentang normal. Pada beberapa pesakit yang dirawat semula setelah penghentian, peningkatan transaminase hepatik berulang, mengesahkan hubungan antara peningkatan ini dan ubat. Dalam kajian klinikal, peningkatan transaminase hepatik berlaku pada bila-bila masa semasa rawatan, walaupun kebanyakannya berlaku pada 12 bulan pertama. Tahap transaminase darah kembali normal kira-kira 2 bulan setelah pemberhentian fingolimod.
Gilenya belum dipelajari pada pesakit dengan gangguan hepatik teruk yang sudah ada (Child-Pugh kelas C) dan oleh itu tidak boleh digunakan pada pesakit ini (lihat bahagian 4.3).
Oleh kerana sifat imunosupresif fingolimod, permulaan rawatan harus ditangguhkan pada pesakit dengan hepatitis virus aktif hingga penyembuhan fasa aktif.
Analisis terkini (iaitu dalam 6 bulan sebelumnya) tahap transaminase dan bilirubin harus tersedia sebelum memulakan rawatan dengan Gilenya. Sekiranya tidak ada gejala klinikal, tahap transaminase hati harus diperiksa setelah 1, 3, 6, 9 dan 12 bulan rawatan dan secara berkala selepas itu.Jika tahap transaminase hepatik mencapai nilai melebihi 5 kali had normal (ULN), pemeriksaan yang lebih kerap harus diatur, termasuk pemeriksaan bilirubin serum dan alkali fosfatase (ALP) Jika setelah pemeriksaan hati berulang nilai transaminase tetap melebihi 5 kali daripada had normal (ULN), rawatan dengan Gilenya harus dihentikan dan dimulakan semula hanya apabila nilai transaminase hati telah kembali normal.
Pada pesakit yang mengalami gejala disfungsi hepatik, seperti mual, muntah yang tidak dapat dijelaskan, sakit perut, keletihan, anoreksia, penyakit kuning dan / atau urin gelap, tahap enzim hati harus dinilai; jika kecederaan hepatik yang ketara disahkan (mis. tahap transaminase hepatik yang melebihi had atas julat normal lebih daripada 5 kali dan / atau peningkatan tahap bilirubin serum), rawatan dengan Gilenya harus dihentikan. Pemulihan terapi akan bergantung pada apakah penyebab lain dari kecederaan hati dikenal pasti dan manfaat pesakit dalam meneruskan terapi berbanding risiko disfungsi hati berulang.
Walaupun tidak ada data untuk membuktikan bahwa pasien dengan penyakit hati yang sudah ada memiliki risiko yang lebih tinggi untuk mengembangkan tes fungsi hati yang tinggi, harus berhati-hati ketika memberikan Gilenya pada pasien dengan riwayat penyakit hati yang signifikan.
Gangguan dengan ujian serologi
Oleh kerana fingolimod mengurangkan jumlah limfosit darah dengan pengagihan semula ke organ limfoid sekunder, ia tidak boleh digunakan untuk menilai status limfosit pesakit yang dirawat dengan Gilenya. Ujian makmal yang melibatkan penggunaan sel mononuklear yang beredar memerlukan jumlah darah yang lebih tinggi kerana pengurangan jumlah limfosit yang beredar.
Kesan pada tekanan darah
Pesakit dengan hipertensi tanpa ubat dikecualikan daripada ujian klinikal sebelum pemasaran Gilenya; oleh itu, perhatian khusus disyorkan jika pesakit dengan hipertensi yang tidak terkawal dirawat dengan Gilenya.
Dalam kajian klinikal pada pesakit dengan sklerosis berganda, rawatan dengan fingolimod 0,5 mg dikaitkan dengan peningkatan rata-rata sekitar 3 mmHg dalam tekanan darah sistolik dan kira-kira 1 mmHg tekanan darah diastolik: kenaikan ini berlaku kira-kira 1 bulan kemudian. Permulaan rawatan dan berlanjutan dengan rawatan berterusan dalam kajian terkawal plasebo selama dua tahun, hipertensi dilaporkan sebagai kejadian buruk pada 6.5% pesakit yang dirawat dengan Gilenya 0.5 mg dan pada 3.3% pesakit yang dirawat dengan plasebo. Oleh itu tekanan darah anda harus diperiksa secara berkala semasa rawatan dengan Gilenya.
Kesan pada sistem pernafasan
Penurunan bergantung sedikit dos dalam jumlah ekspirasi paksa (FEV1) dan kapasiti penyebaran untuk karbon monoksida (Dlco) diperhatikan semasa rawatan dengan Gilenya, penurunan yang berlaku pada bulan pertama dan tetap stabil sepanjang rawatan. Gilenya harus digunakan dengan berhati-hati pada pasien dengan gangguan pernafasan yang teruk, fibrosis paru dan penyakit paru obstruktif kronik (lihat bahagian 4.8).
Sindrom ensefalopati terbalik posterior
Kes-kes jarang sindrom ensefalopati reversibel posterior (PRES) telah dilaporkan dalam ujian klinikal dan pengalaman selepas pemasaran dengan dos 0,5 mg (lihat bahagian 4.8). Gejala yang dilaporkan termasuk permulaan sakit kepala yang teruk secara tiba-tiba, mual, muntah, perubahan status mental, visual gangguan dan sawan. Gejala PRES biasanya boleh dipulihkan tetapi boleh menjadi strok iskemia atau pendarahan serebrum. Kelewatan diagnosis dan rawatan boleh menyebabkan akibat neurologi kekal. Sekiranya kehadiran disyaki. PRES, rawatan dengan Gilenya harus dihentikan.
Rawatan sebelumnya dengan terapi imunosupresif atau imunomodulator
Tidak ada kajian yang dilakukan untuk menilai keberkesanan dan keselamatan Gilenya ketika pesakit beralih dari teriflunomide, dimethyl fumarate atau alemtuzumab ke Gilenya. Ketika pesakit beralih dari terapi lain. pengubahsuaian penyakit di Gilenya, jangka hayat dan mekanisme tindakan terapi lain mesti diambil kira untuk mengelakkan kesan tambahan pada sistem imun dan, pada masa yang sama, meminimumkan risiko pengaktifan semula penyakit. Disarankan untuk menilai jumlah darah yang lengkap sebelum memulakan rawatan dengan Gilenya untuk memastikan bahawa kesan pada sistem imun yang disebabkan oleh terapi sebelumnya (mis. sitopenia) telah hilang.
Rawatan Gilenya secara amnya dapat dimulakan segera setelah penghentian terapi interferon atau glatiramer asetat.
Dalam kes dimetil fumarate, tempoh pencucian ia mesti mencukupi untuk mengembalikan jumlah darah yang mencukupi sebelum memulakan rawatan dengan Gilenya.
Kerana jangka hayat natalizumab yang panjang, penghapusan biasanya memakan masa hingga 2-3 bulan setelah menghentikan rawatan. Teriflumonide juga perlahan dikeluarkan dari plasma. Tanpa prosedur penghapusan yang dipercepat, pembersihan teriflunomide dari plasma dapat berlangsung dari beberapa bulan hingga 2 tahun. Dianjurkan untuk melakukan prosedur penghapusan dipercepat seperti yang dijelaskan dalam ringkasan ciri produk untuk teriflunomide, atau sebagai alternatif masa pencucian tidak boleh kurang dari 3,5 bulan. Perhatian harus diberikan semasa menukar pesakit dari terapi natalizumab atau teriflunomide ke Gilenya mengenai kemungkinan kesan bersamaan pada sistem imun.
Alemtuzumab mempunyai kesan imunosupresif yang kuat dan berpanjangan. Oleh kerana jangka masa sebenar kesan ini tidak diketahui, disarankan untuk tidak memulakan rawatan dengan Gilenya berikutan alemtuzumab kecuali manfaat rawatan untuk setiap pesakit jelas melebihi risiko.
Keputusan untuk bersama-sama menguruskan rawatan kortikosteroid berpanjangan mesti dibuat setelah dipertimbangkan dengan teliti.
Pentadbiran serentak dengan pemacu CYP450 yang kuat
Fingolimod harus digunakan dengan berhati-hati dalam kombinasi dengan pemicu CYP450 yang kuat. Dianjurkan untuk tidak mentadbir wort St. John secara bersamaan (lihat bahagian 4.5).
Penamatan terapi
Berdasarkan jangka hayat ubat, jika keputusan dibuat untuk menghentikan rawatan dengan Gilenya, selang 6 minggu tanpa terapi harus ditinggalkan untuk membolehkan fingolimod dibersihkan dari darah (lihat bahagian 5.2). Jumlah limfosit secara progresif kembali ke nilai normal dalam 1-2 bulan setelah pemberhentian terapi (lihat bahagian 5.1). Memulakan terapi lain selama selang waktu ini mengakibatkan pendedahan bersama dengan fingolimod. Penggunaan ubat imunosupresif sejurus selepas pemberhentian pemberian Gilenya mungkin memberi kesan tambahan pada sistem imun dan oleh itu berhati-hati disyorkan.
04.5 Interaksi dengan produk ubat lain dan bentuk interaksi lain
Terapi antineoplastik, imunomodulator atau imunosupresif
Terapi antineoplastik, imunomodulator atau imunosupresif tidak boleh diberikan bersamaan kerana risiko kesan tambahan pada sistem imun (lihat bahagian 4.3 dan 4.4).
Perhatian juga harus diberikan ketika pesakit memulai terapi Gilenya setelah menghentikan rawatan dengan terapi jangka panjang dengan kesan pada sistem kekebalan tubuh, seperti natalizumab atau mitoxantrone (lihat bahagian 4.4). Dalam percubaan klinikal pada sklerosis. Rawatan berulang berulang berulang dengan jangka pendek kortikosteroid tidak dikaitkan dengan peningkatan kadar jangkitan.
Vaksinasi
Vaksinasi mungkin kurang berkesan semasa rawatan dan hingga dua bulan setelah menghentikan rawatan dengan Gilenya. Penggunaan vaksin yang dilemahkan secara langsung boleh menimbulkan risiko jangkitan dan oleh itu harus dielakkan (lihat bahagian 4.4 dan 4.8).
Bahan yang menyebabkan bradikardia
Fingolimod dikaji bersama dengan atenolol dan diltiazem. Apabila fingolimod diberikan dengan atenolol dalam kajian interaksi pada sukarelawan yang sihat, terdapat penurunan penurunan kadar jantung sebanyak 15% semasa memulakan rawatan; kesan ini tidak diperhatikan dengan diltiazem. Oleh kerana kesan tambahan yang berpotensi. Degup jantung, rawatan Gilenya seharusnya tidak dimulakan pada pesakit yang mengambil beta-blocker atau ubat lain yang dapat menurunkan kadar jantung, seperti kelas Ia dan III antiarrhythmics, penyekat saluran kalsium (seperti ivabradine, verapamil atau diltiazem), digoxin, anticholinesterases atau pilocarpine (lihat bahagian 4.4 dan 4.8 Jika rawatan dengan Gilenya dipertimbangkan untuk pasien ini, seorang ahli kardiologi harus berkonsultasi untuk mempertimbangkan beralih ke produk ubat lain yang tidak menyebabkan penurunan kadar jantung atau untuk menentukan pemantauan yang memadai pada awal rawatan. Sekiranya tidak dapat menghentikan rawatan dengan ubat-ubatan yang menurunkan kadar denyutan jantung, pemantauan disarankan sekurang-kurangnya hingga keesokan harinya.
Perubahan farmakokinetik fingolimod disebabkan oleh bahan lain
Fingolimod terutama dimetabolisme oleh CYP4F2. Enzim lain seperti CYP3A4 juga mungkin terlibat dalam metabolisme, terutama dalam hal induksi kuat CYP3A4. Inhibitor protein pembawa yang berpotensi tidak dijangka mempengaruhi tingkah laku fingolimod. Pemberian bersama fingolimod dengan ketoconazole menghasilkan peningkatan pendedahan (AUC) sebanyak 1.7 kali ganda terhadap fingolimod dan fingolimod fosfat melalui penghambatan CYP4F2.Hati-hati harus diberikan semasa memberikan fingolimod dengan bahan yang boleh menghambat CYP3A4 (inhibitor protease, antijamur azole, beberapa makrolida seperti clarithromycin atau telithromycin).
Pemberian karbamazepin 600 mg bersamaan dua kali sehari, mencapai keadaan stabil, dan dos tunggal fingolimod 2 mg mengurangkan AUC fingolimod dan metabolitnya sekitar 40%. Pengaruh kuat enzim CYP3A4 lain, seperti rifampicin, phenobarbital, phenytoin, efavirenz dan St. John's wort, boleh menyebabkan pengurangan AUC fingolimod dan metabolitnya sekurang-kurangnya sebesar ini. Oleh kerana ini berpotensi menjejaskan keberkesanannya, berhati-hati harus diberikan ketika memberikan secara kombinasi.
Perubahan dalam farmakologi bahan lain yang disebabkan oleh fingolimod
Fingolimod tidak mungkin berinteraksi dengan bahan yang dimetabolisme terutamanya oleh enzim CYP450 atau substrat protein pembawa utama.
Pemberian bersama fingolimod dengan siklosporin tidak menyebabkan perubahan pendedahan kepada siklosporin atau fingolimod. Oleh itu, fingolimod tidak diharapkan dapat mengubah farmakokinetik produk ubat-ubatan yang merupakan substrat CYP3A4.
Pemberian bersama fingolimod dengan kontraseptif oral (etinil estradiol dan levonorgestrel) tidak menyebabkan perubahan pendedahan kontraseptif oral, pendedahan kepada ubat-ubatan tersebut.
04.6 Kehamilan dan penyusuan
Wanita berpotensi melahirkan anak / Kontrasepsi pada wanita
Sebelum memulakan rawatan dengan Gilenya, wanita yang berpotensi melahirkan anak harus diberitahu tentang kemungkinan risiko serius pada janin dan tentang perlunya menggunakan langkah-langkah kontraseptif yang berkesan semasa rawatan dengan Gilenya. Oleh kerana mengambil masa kira-kira dua bulan setelah menghentikan rawatan untuk membersihkan jari jari dari badan (lihat bahagian 4.4), kemungkinan risiko terhadap janin mungkin ada dan oleh itu langkah-langkah kontraseptif mesti diteruskan selama waktu itu.
Kehamilan
Ujian kehamilan negatif mesti ada sebelum memulakan rawatan pada wanita yang berpotensi melahirkan anak. Wanita tidak boleh hamil semasa rawatan dan disyorkan kontraseptif yang berkesan. Sekiranya seorang wanita hamil semasa mengambil Gilenya, penghentian rawatan adalah disyorkan.
Kajian pada haiwan menunjukkan ketoksikan pembiakan, termasuk kehilangan janin dan kecacatan organ, terutamanya batang arteri yang berterusan dan kecacatan septum ventrikel (lihat bahagian 5.3). Selanjutnya, reseptor di mana fingolimod bertindak (sphingosine 1-fosfat) terlibat dalam pembentukan vaskular semasa embriogenesis. Terdapat data yang sangat terhad dari penggunaan fingolimod pada wanita hamil.
Tidak ada data mengenai kesan fingolimod pada persalinan dan kelahiran.
Masa makan
Fingolimod diekskresikan dalam susu haiwan yang menyusui pada kepekatan 2-3 kali lebih tinggi daripada yang terdapat dalam plasma ibu (lihat bahagian 5.3). Oleh kerana berpotensi untuk reaksi buruk serius terhadap fingolimod pada bayi yang disusui, wanita yang tidak mendapat rawatan dengan Gilenya tidak boleh menyusu.
Kesuburan
Data dari kajian praklinikal tidak menunjukkan bahawa fingolimod dikaitkan dengan peningkatan risiko kesuburan terganggu (lihat bahagian 5.3).
04.7 Kesan terhadap kemampuan memandu dan menggunakan mesin
Gilenya tidak mempunyai atau tidak dapat mempengaruhi kemampuan memandu atau menggunakan mesin.
Walau bagaimanapun, kadang-kadang pening atau rasa mengantuk mungkin berlaku semasa memulakan rawatan dengan Gilenya. Sebaiknya pesakit diperhatikan selama 6 jam ketika memulakan rawatan dengan Gilenya (lihat bahagian 4.4 Bradyarrhythmia).
04.8 Kesan yang tidak diingini
Ringkasan profil keselamatan
Populasi keselamatan Gilenya berasal dari dua ujian klinikal terkawal plasebo fasa III dan satu percubaan klinikal fasa III yang dikendalikan aktif yang dijalankan pada pesakit dengan sklerosis berulang. Ia merangkumi sejumlah 2.431 pesakit yang dirawat dengan Gilenya (0.5 atau 1.25 mg). Dalam kajian klinikal D2301 (FREEDOMS) 2 tahun yang dikendalikan plasebo, 854 pesakit (plasebo: 418 pesakit) dirawat dengan fingolimod. Dalam 2 tahun, kajian terkawal plasebo D2309 (FREEDOMS II), 728 pesakit dengan sklerosis berganda (plasebo: 355 pesakit) dirawat dengan fingolimod. Hasil kajian dari kedua kajian ini menunjukkan bahawa reaksi buruk yang paling serius yang berlaku dengan Gilenya 0,5 mg adalah jangkitan, edema makula dan blok atrioventrikular sementara pada permulaan rawatan. Reaksi buruk yang paling kerap (kejadian ≥ 10%) yang berlaku dengan Gilenya 0.5 mg adalah selesema, sinusitis, sakit kepala, cirit-birit, sakit belakang, peningkatan enzim hati dan batuk. Reaksi buruk yang paling kerap dengan Gilenya 0,5 mg yang menyebabkan "penghentian rawatan adalah" peningkatan kadar ALT darah (2,2%). Dalam kajian 1 tahun D2302 (TRANSFORMS) yang melibatkan 849 pesakit yang dirawat dengan fingolimod dan menggunakan interferon beta-1α sebagai kawalan, tindak balas buruk yang berlaku umumnya serupa dengan yang dilakukan dalam kajian terkawal plasebo, dengan mengambil kira tempoh kajian yang berbeza.
Reaksi buruk yang dilaporkan untuk Gilenya 0,5 mg dalam kajian D2301 (KEBEBASAN) dan D2309 (KEBEBASAN II) disenaraikan di bawah. Kategori frekuensi ditakrifkan menggunakan konvensyen berikut: sangat biasa (≥1 / 10); biasa (≥1 / 100,
Jadual ringkasan tindak balas buruk
* Tidak dilaporkan dalam kajian FREEDOMS, FREEDOMS II, dan TRANSFORMS. Pengkategorian frekuensi kejadian berdasarkan pada anggaran "pendedahan fingolimod kira-kira 10,000 pesakit di semua ujian klinikal."
Penerangan mengenai beberapa reaksi buruk tertentu
Jangkitan
Dalam ujian klinikal pada pesakit dengan sklerosis berganda, kadar keseluruhan jangkitan (65.1%) yang dilaporkan dengan dos 0.5 mg adalah serupa dengan yang dilihat dengan plasebo. Walau bagaimanapun, jangkitan saluran pernafasan bawah, terutamanya bronkitis dan, pada tahap yang lebih rendah, jangkitan herpetic dan radang paru-paru, lebih kerap berlaku pada pesakit yang dirawat dengan Gilenya.
Beberapa kes jangkitan herpetic yang disebarkan, termasuk kes yang membawa maut, telah dilaporkan walaupun dengan dos 0.5 mg.
Edema makula
Dalam kajian klinikal pada pesakit dengan sklerosis berganda edema makula terjadi pada 0,5% pesakit yang dirawat dengan dos yang disyorkan 0,5 mg dan pada 1,1% pesakit dirawat dengan dos yang lebih tinggi (1, 25 mg). Sebilangan besar kes berlaku dalam 3-4 bulan pertama terapi. Beberapa pesakit melaporkan penglihatan kabur dan penurunan ketajaman penglihatan; yang lain tidak simptomatik dan diagnosis dibuat semasa lawatan rutin mata. Edema makula secara amnya bertambah baik atau diselesaikan secara spontan setelah penghentian rawatan. Risiko berulang selepas pendedahan semula terhadap rawatan belum dipelajari. .
Kejadian edema makula meningkat pada pesakit sklerosis berganda dengan riwayat uveitis (17% dengan riwayat uveitis berbanding 0,6% tanpa riwayat uveitis). Gilenya belum dikaji pada pesakit dengan sklerosis berganda dan diabetes mellitus. penyakit yang berkaitan dengan peningkatan risiko edema makula (lihat bahagian 4.4). Dalam kajian klinikal pada pesakit transplantasi ginjal termasuk pesakit diabetes mellitus, rawatan dengan fingolimod 2,5 mg dan 5 mg mengakibatkan peningkatan dua kali kejadian edema makula.
Bradyarrhythmia
Permulaan rawatan dengan Gilenya mengakibatkan penurunan kadar denyutan jantung sementara dan mungkin juga dikaitkan dengan kelewatan dalam konduksi atrioventricular. Dalam ujian klinikal pada pesakit dengan sklerosis berganda, penurunan kadar denyut jantung maksimum diperhatikan dalam 6 jam pertama setelah operasi. " permulaan rawatan, dengan penurunan frekuensi rata-rata 12-13 denyutan seminit semasa rawatan dengan Gilenya 0,5 mg. Penurunan kadar denyutan jantung di bawah 40 denyutan seminit jarang dilihat pada pesakit yang dirawat dengan Gilenya 0,5 mg. Denyut jantung rata-rata kembali ke tahap awal dalam 1 bulan setelah rawatan berterusan. Bradikardia secara amnya tidak simptomatik, tetapi beberapa pesakit mengalami gejala ringan hingga sederhana, termasuk hipotensi, pening, keletihan dan / atau berdebar-debar, yang hilang dalam 24 jam pertama setelah permulaan rawatan (lihat juga bahagian 4.4 dan 5.1.).
Dalam kajian klinikal pada pesakit dengan sklerosis berganda, blok atrioventricular darjah pertama (pemanjangan "selang PR hingga ECG") diperhatikan pada 4.7% pesakit yang dirawat dengan fingolimod 0.5 mg, pada 2.8% pesakit. Pesakit yang dirawat dengan interferon intramuskular beta- 1α dan pada 1.6% pesakit dirawat plasebo. Blok atrioventrikular tahap kedua telah dilaporkan pada kurang dari 0.2% pesakit yang dirawat dengan Gilenya 0.5 mg. Dalam pengalaman pasca pemasaran, episod sementara yang terpencil, yang secara spontan dapat menyelesaikan sekatan atrioventrikular lengkap telah dilaporkan dalam tempoh pemantauan 6 jam berikutan dos pertama Gilenya. Pengalaman pasca pemasaran, biasanya bersifat sementara, tanpa gejala, dan diselesaikan dalam tempoh 24 berjam-jam permulaan rawatan.Walaupun tidak diperlukan campur tangan perubatan untuk kebanyakan pesakit, satu pesakit yang dirawat dengan Gilenya 0, 5 mg diberikan isoprenalin setelah sekatan atrioventrikular Mobitz jenis 1 tahap kedua tanpa gejala.
Dalam pengalaman pasca pemasaran, kejadian terpencil dengan onset terlambat, termasuk asistol sementara dan kematian yang tidak dapat dijelaskan, telah berlaku dalam masa 24 jam setelah pemberian dos pertama. Penilaian kes-kes ini rumit dengan adanya ubat-ubatan bersamaan dan / atau perubatan yang sudah ada Hubungan peristiwa ini dengan Gilenya tidak dapat dipastikan.
Tekanan darah
Dalam kajian klinikal pada pesakit dengan sklerosis berganda, rawatan dengan Gilenya 0,5 mg dikaitkan dengan peningkatan rata-rata tekanan darah sistolik sekitar 3 mmHg dan tekanan darah diastolik sekitar 1 mmHg: kenaikan ini terjadi kira-kira 1 bulan kemudian. rawatan berterusan. Hipertensi dilaporkan pada 6.5% pesakit yang dirawat dengan fingolimod 0.5 mg dan pada 3.3% pesakit yang dirawat dengan plasebo. kes hipertensi yang mungkin memerlukan rawatan dengan ubat antihipertensi atau penghentian Gilenya telah dilaporkan dalam bulan pertama dan pada hari pertama rawatan (lihat juga bahagian 4.4 Kesan tekanan darah).
Fungsi hati
Peningkatan enzim hati telah dilaporkan pada pesakit dengan sklerosis berganda yang dirawat dengan Gilenya. Dalam kajian klinikal, peningkatan paras ALT darah tanpa gejala ≥3 kali dan ≥5 kali had atas julat normal (ULN) diperhatikan pada 8.0% dan 1.8% pesakit yang masing-masing dirawat dengan Gilenya, 0.5 mg. Pada beberapa pesakit rawatan selepas penghentian, peningkatan transaminase hepatik berulang, mengesahkan hubungan antara peningkatan ini dan ubat. Dalam ujian klinikal peningkatan transaminase hepatik berlaku pada bila-bila masa semasa rawatan, walaupun paling banyak berlaku pada 12 bulan pertama. Tahap ALT kembali normal kira-kira 2 bulan setelah menghentikan rawatan dengan Gilenya. Dalam sebilangan kecil pesakit (N = 10 pada dosis 1,25 mg, N = 2 pada dos 0,5 mg), yang mengalami peningkatan ALT ≥5 kali batas atas julat normal dan yang meneruskan terapi dengan Gilenya, nilai ALT kembali normal dalam masa lebih kurang 5 bulan (lihat juga bahagian 4.4 Fungsi hepatik).
Gangguan sistem saraf
Dalam kajian klinikal, kejadian yang jarang berlaku yang melibatkan sistem saraf, termasuk strok iskemia dan hemoragik dan gangguan neurologi atipikal, seperti contohnya kejadian yang serupa dengan ensefalomielitis disebarkan akut (EAD).
Patologi vaskular
Kes penyakit arteri perifer jarang berlaku pada pesakit yang dirawat dengan fingolimod pada dos yang lebih tinggi (1,25 mg).
Sistem pernafasan
Penurunan bergantung sedikit dos dalam jumlah ekspirasi paksa (FEV1) dan kapasiti penyebaran untuk karbon monoksida (Dlco) diperhatikan semasa rawatan dengan Gilenya, penurunan yang berlaku pada bulan pertama dan tetap stabil sepanjang rawatan. Pada bulan 24, pengurangan peratusan dari awal dalam FEV1 yang diramalkan adalah 2.7% untuk fingolimod 0.5 mg dan 1.2% untuk plasebo, perbezaan yang dapat diselesaikan setelah rawatan dihentikan. Pengurangan Dlco pada bulan 24 adalah 3.3% untuk fingolimod 0.5 mg dan 2.7% untuk plasebo.
Limfoma
Kes pelbagai jenis limfoma telah dilaporkan dalam kedua-dua ujian klinikal dan pengalaman pasca pemasaran, termasuk kes kematian limfoma sel B positif virus Epstein-Barr (EBV). Kejadian kes limfoma (sel-B dan sel-T ) lebih tinggi dalam kajian klinikal daripada yang dijangkakan pada populasi umum.
Sindrom hemofagositik
Kes sindrom haemophagocytic sangat jarang berlaku (Sindrom Haemophagocytic, HPS) dengan hasil maut pada pesakit yang dirawat dengan fingolimod dalam konteks "jangkitan." HPS adalah keadaan yang jarang dijelaskan berkaitan dengan jangkitan, imunosupresi dan pelbagai penyakit autoimun.
Melaporkan tindak balas buruk yang disyaki
Pelaporan tindak balas buruk yang disyaki berlaku setelah kebenaran produk ubat adalah penting kerana memungkinkan pemantauan berterusan terhadap keseimbangan manfaat / risiko produk ubat tersebut. Profesional penjagaan kesihatan diminta untuk melaporkan sebarang reaksi buruk yang disyaki melalui sistem pelaporan nasional. Dalam "Lampiran V .
04.9 Overdosis
Dosis tunggal sehingga 80 kali dos yang disyorkan (0,5 mg) dapat diterima dengan baik pada sukarelawan yang sihat. Pada dos 40 mg, 5 daripada 6 subjek melaporkan kelemahan sesak dada atau malaise yang berkaitan dengan kereaktifan saluran udara.
Fingolimod boleh menyebabkan bradikardia pada awal rawatan. Penurunan kadar denyutan jantung biasanya berlaku dalam satu jam dari dos pertama dan maksimum dalam 6 jam pertama. Kesan kronotropik negatif Gilenya berterusan melebihi 6 jam dan secara beransur-ansur hilang pada hari-hari rawatan berikutnya (lihat bahagian 4.4 untuk keterangan lebih lanjut). Terdapat laporan pengurangan konduksi atrioventrikular, dengan laporan tersekat blok atrioventrikular. Penyelesaian lengkap, sementara dan spontan (lihat bahagian 4.4 dan 4.8).
Sekiranya overdosis bertepatan dengan pendedahan pertama kepada Gilenya, adalah penting untuk memantau pesakit secara berterusan (masa nyata) elektrokardiografi dengan pengukuran kadar denyutan jantung dan tekanan darah setiap jam, sekurang-kurangnya selama 6 jam pertama (lihat bahagian 4.4).
Pemantauan tambahan juga diperlukan (sekurang-kurangnya hingga keesokan harinya dan dalam kes apa pun sehingga gejala diselesaikan) jika, setelah 6 jam dari pemberian dos pertama, kadar denyutan jantung adalah
Fingolimod tidak dihilangkan dengan dialisis atau plasmapheresis.
05.0 HARTA FARMAKOLOGI
05.1 Sifat farmakodinamik
Kumpulan farmakoterapeutik: imunosupresan selektif.
Kod ATC: L04AA27.
Mekanisme tindakan
Fingolimod adalah modulator reseptor sphingosine-1-fosfat (S1P). Melalui spingosin kinase fingolimod diubah menjadi metabolit aktif fingolimod fosfat yang mengikat, pada kepekatan nanomolar rendah, ke reseptor S1P1 yang terletak di permukaan limfosit, dan dengan mudah melintasi penghalang darah-otak untuk mengikat reseptor di saraf pusat sistem S1P1 diletakkan pada sel-sel sistem saraf pusat. Fingolimod fosfat, bertindak sebagai antagonis fungsional reseptor S1P yang dinyatakan pada limfosit, menghalang keupayaan limfosit untuk melepaskan diri dari kelenjar getah bening, yang mengakibatkan pengagihan semula daripada pemusnahan limfosit. Pengagihan semula ini mengurangkan penyusupan limfosit patogen ke sistem saraf pusat, di mana mereka terlibat dalam keradangan saraf dan kerosakan tisu. Kajian dan eksperimen haiwan secara in vitro menunjukkan bahawa fingolimod juga boleh bertindak dengan berinteraksi dengan reseptor S1P yang dinyatakan pada sel-sel sistem saraf pusat.
Kesan farmakodinamik
Dalam masa 4-6 jam selepas pemberian pertama fingolimod 0,5 mg, jumlah limfosit dalam darah periferal menurun kepada kira-kira 75% dari nilai awal. Melanjutkan dengan pemberian harian, jumlah limfosit terus menurun selama dua minggu, mencapai nilai minimum sekitar 500 sel / mikroliter, atau sekitar 30% dari nilai awal. 18% pesakit mencapai nilai minimum di bawah 200 sel / mikroliter sekurang-kurangnya sekali. Dengan rawatan harian yang berterusan, bilangan limfosit tetap rendah. Sebilangan besar limfosit T dan B secara berkala berhijrah ke organ limfoid: fingolimod bertindak terutamanya pada sel-sel ini. Kira-kira 15-20% limfosit T mempunyai fenotip TEM (memory effector): sel-sel ini penting untuk pengawasan imun periferal. Oleh kerana limfosit jenis ini umumnya tidak berhijrah ke organ limfoid, fingolimod tidak bertindak pada sel-sel ini. Peningkatan bilangan limfosit periferal terbukti pada hari-hari selepas penghentian rawatan dengan fingolimod; bilangan limfosit biasanya kembali normal dalam satu hingga dua bulan. Pentadbiran kronik fingolimod mengakibatkan sedikit penurunan bilangan neutrofil sama dengan kira-kira 80% dari nilai asas.Fingolimod tidak bertindak pada monosit.
Fingolimod menyebabkan penurunan kadar jantung sementara dan penurunan konduksi atrioventrikular semasa memulakan rawatan (lihat bahagian 4.4. Dan 4.8). Pengurangan maksimum kadar denyutan jantung diperhatikan dalam masa 6 jam selepas pentadbiran, dengan 70% kesan kronotropik negatif. Dengan pentadbiran seterusnya, degupan jantung kembali ke tahap awal dalam satu bulan. Penurunan kadar denyutan jantung yang disebabkan oleh fingolimod dapat dibalikkan dengan pemberian atropin atau isoprenalin parenteral. Salmeterol yang dihirup juga terbukti mempunyai kesan kronotropik positif yang sederhana. Semasa memulakan rawatan dengan fingolimod terdapat peningkatan kontraksi atrium pramatang, tetapi tidak ada peningkatan kadar fibrilasi atrium / flutter atau aritmia ventrikel atau ektopia. Rawatan dengan fingolimod tidak mengakibatkan penurunan output jantung, dan tidak mempengaruhi tindak balas simpatomimetik jantung, termasuk variasi denyut jantung diurnal dan tindak balas terhadap aktiviti.
Rawatan dengan fingolimod, dos tunggal atau berulang 0,5 mg dan 1,25 mg selama dua minggu, tidak menghasilkan peningkatan rintangan saluran udara yang dapat dilihat sebagai FEV1 dan Aliran Ekspirasi Paksa (FEF) 25-75. Walau bagaimanapun, dengan dos tunggal fingolimod ≥5 mg (10 kali ganda daripada dos yang disyorkan), peningkatan rintangan saluran udara bergantung pada dos berlaku. Rawatan dengan dos berulang fingolimod 0,5 mg, 1,25 mg, atau 5 mg tidak menyebabkan terjadinya gangguan oksigenasi atau desaturasi oksigen semasa latihan atau peningkatan tindak balas saluran udara terhadap metakolin. Individu yang menerima fingolimod bertindak balas dengan bronkodilasi normal kepada beta-agonis yang dihirup.
Keberkesanan dan keselamatan klinikal
Keberkesanan Gilenya ditunjukkan dalam dua kajian yang menilai pemberian fingolimod 0,5 mg dan 1,25 mg sekali sehari pada pesakit dengan sklerosis berulang (RRMS). Kedua-dua kajian adalah pesakit yang mendaftar ≥ 2 kambuh dalam 2 tahun sebelumnya atau ≥1 berulang pada tahun sebelumnya. Skor pada Skala Status Kecacatan Terluas (EDSS) adalah 0-5.5. Kajian ketiga yang dilakukan pada populasi pesakit yang sama diselesaikan setelah pendaftaran Gilenya.
Dalam kajian D2301 (KEBEBASAN) yang dikendalikan secara rawak, buta double-blind D2301, 272 pesakit dimasukkan (n = 425 dirawat dengan fingolimod 0,5 mg, 429 dengan fingolimod 1,25 mg, 418 dengan plasebo). Nilai median ciri asas adalah: umur 37 tahun, tempoh penyakit 6.7 tahun, skor EDSS 2.0. Hasilnya ditunjukkan dalam Jadual 1. Tidak ada perbezaan yang signifikan antara dos 0,5 mg dan 1,25 mg untuk semua titik akhir.
Jadual 1: Kajian D2301 (KEBEBASAN): Hasil utama
† Perkembangan kecacatan yang ditakrifkan sebagai peningkatan EDSS 1 mata disahkan pada 3 bulan
** p
Semua titik akhir klinikal dinilai dengan analisis niat untuk merawat. Analisis yang berkaitan dengan data MRI menggunakan set data yang dapat dinilai.
Pesakit yang telah menyelesaikan fasa teras dari kajian KEBEBASAN 24 bulan dapat memasuki fasa pemanjangan dos-buta (D2301E1) dan menerima fingolimod. Sebanyak 920 pesakit masuk (n = 331 dilanjutkan pada dos 0,5 mg, 289 pada dos 1,25 mg, 155 beralih dari plasebo menjadi 0,5 mg dan 145 dari plasebo menjadi 1,25 mg). Selepas 12 bulan (bulan 36), 856 pesakit (93%) masih mendaftar. Antara bulan 24 dan bulan 36, kadar kambuhan tahunan (ARR) untuk pesakit yang menerima fingolimod 0,5 mg dalam fasa teras kajian dan yang telah melanjutkan dosis yang sama (0,5 mg) adalah 0,17 (0,21 dalam fasa teras kajian). Kadar kambuh tahunan untuk pesakit yang beralih dari plasebo ke fingolimod 0,5 mg adalah 0,22 (0,42 dalam fasa teras kajian).
Hasil yang serupa diperoleh dalam kajian Tahap III, 2 tahun, rawak, double-blind, plasebo yang dikendalikan (D2309; KEBEBASAN 2) yang dilakukan pada 1,083 pesakit dengan sklerosis berulang-kembalinya (n = 358 dirawat dengan fingolimod 0, 5 mg , 370 dengan fingolimod 1.25 mg, 355 dengan plasebo). Nilai median ciri asas adalah: umur 41 tahun, tempoh penyakit 8.9 tahun, skor EDSS 2.5.
Jadual 2: Kajian D2309 (KEBEBASAN 2): Hasil utama
† Perkembangan kecacatan yang ditakrifkan sebagai peningkatan 1 mata dalam EDSS disahkan pada 3 bulan
** p
Semua titik akhir klinikal dinilai dengan analisis niat untuk merawat. Analisis yang berkaitan dengan data MRI menggunakan set data yang dapat dinilai.
Dalam kajian D2302 (TRANSFORMS), fasa III, berlangsung 1 tahun, rawak, double-blind terkawal dan double-dummy berbanding ubat aktif (interferon beta-1α) 1280 pesakit dimasukkan (n = 429 dirawat dengan fingolimod 0,5 mg, 420 dengan fingolimod 1,25 mg, 431 dengan suntikan intramuskular interferon beta-1α pada dos 30 mikrogram sekali seminggu). Nilai median ciri asas adalah: umur 36 tahun, tempoh penyakit 5.9 tahun, skor EDSS 2.0. Hasil kajian disajikan dalam Jadual 3. Tidak ada perbezaan yang signifikan antara dos 0,5 mg dan 1,25 mg sehubungan dengan titik akhir kajian.
Jadual 3: Kajian D2302 (TRANSFORMS): Hasil utama
† Perkembangan kecacatan yang ditakrifkan sebagai peningkatan 1 mata dalam EDSS disahkan pada 3 bulan
** p
Semua titik akhir klinikal dinilai dengan analisis niat untuk merawat. Analisis yang berkaitan dengan data MRI menggunakan set data yang dapat dinilai.
Pesakit yang telah menyelesaikan fasa teras dari kajian TRANSFORMS 12 bulan dapat memasuki fasa pemanjangan dos-buta (D2302E1) dan menerima fingolimod. Sebanyak 1.030 pesakit masuk, namun 3 di antaranya tidak mendapat rawatan (n = 356 dilanjutkan pada dos 0.5 mg, 330 pada dos 1.25 mg, 167 beralih dari interferon beta-1α menjadi 0, 5 mg dan 174 dari interferon beta -1α pada kadar 1.25 mg). Selepas 12 bulan (bulan 24), 882 pesakit (86%) masih mendaftar. Antara bulan 12 dan 24, kadar kambuhan tahunan (ARR) untuk pesakit yang menerima fingolimod 0,5 mg dalam fasa teras kajian dan yang melanjutkan pada dos yang sama (0,5 mg) adalah 0,20 (0,19 dalam fasa teras kajian). Kadar kambuh tahunan untuk pesakit yang beralih dari interferon beta-1α ke fingolimod 0,5 mg adalah 0,33 (0,48 dalam fasa teras kajian).
Hasil yang dikumpulkan dari kajian D2301 dan D2302 menunjukkan penurunan yang konsisten dan statistik dari kawalan kadar kambuhan tahunan dalam subkumpulan yang ditentukan oleh jantina, usia, terapi MS sebelumnya, aktiviti penyakit atau kecacatan pada awal.
Analisis lebih lanjut hasil percubaan klinikal menunjukkan kesan rawatan yang signifikan pada subkumpulan pesakit dengan sklerosis berulang yang sangat aktif.
Agensi Ubat-ubatan Eropah telah menangguhkan kewajiban untuk menyerahkan hasil kajian dengan Gilenya dalam satu atau lebih subkumpulan populasi anak dalam sklerosis berganda (lihat bahagian 4.2 untuk maklumat mengenai penggunaan pediatrik).
05.2 "Sifat farmakokinetik
Data farmakokinetik diperoleh pada sukarelawan yang sihat, pesakit transplantasi ginjal dan pesakit dengan sklerosis berganda.
Metabolit aktif farmakologi yang bertanggungjawab untuk keberkesanannya adalah fingolimod fosfat.
Penyerapan
Penyerapan fingolimod berlaku secara perlahan (Tmax 12-16 jam) dan luas (≥85%). Ketersediaan bio mutlak yang jelas berikutan pemberian oral adalah 93% (selang keyakinan: 79-111%). keadaan mantap tahap dicapai dalam 1-2 bulan selepas pemberian dos harian tunggal pada tahap fingolimod dan allo keadaan mantap mereka kira-kira 10 kali lebih tinggi daripada yang dilihat dengan dos permulaan.
Pengambilan makanan tidak mengubah nilai kepekatan puncak (Cmax) atau pendedahan sistemik (AUC) fingolimod. Fingolimod fosfat Cmax sedikit meningkat sebanyak 34% sementara AUC tidak berubah.Oleh itu Gilenya boleh diambil sama ada semasa perut penuh atau kosong (lihat bahagian 4.2).
Pembahagian
Fingolimod menyebar dengan cepat dalam sel darah merah, dan terdapat dalam 86% sel darah. Fingolimod fosfat mempunyai taburan sel darah merah 17% lebih rendah. Pengikatan protein plasma dari fingolimod dan phospholimod fosfat tinggi (> 99%).
Fingolimod diedarkan secara meluas dalam tisu dengan jumlah pengedaran kira-kira 1,200 ± 260 liter.
Biotransformasi
Pada manusia, fingolimod dimetabolisme oleh fosforilasi stereoselektif terbalik dengan pembentukan aktif (S) -enantiomer fosfat fosfat farmakologi. Fingolimod dihilangkan oleh biotransformasi oksidatif, yang dikatalisis terutamanya oleh CYP4F2 dan mungkin isoenzim lain, dan penurunan seterusnya kepada metabolit yang tidak aktif, serupa dengan asid lemak. Pembentukan analog ceramide polar tidak aktif secara farmakologi dari fingolimod juga diperhatikan. Enzim utama yang terlibat dalam metabolisme fingolimod sebahagiannya dikenal pasti dan mungkin CYP4F2 atau CYP3A4.
Berikutan penggunaan oral fingolimod tunggal [14C], komponen utama yang berkaitan dengan fingolimod, yang dikesan dalam darah oleh sumbangannya kepada AUC sehingga 34 hari selepas pentadbiran keseluruhan komponen yang dilabelkan dengan radiolabel, adalah fingolimod itu sendiri (23%), fingolimod fosfat ( 10%) dan beberapa metabolit tidak aktif (metabolit asid karboksilat M3 (8%), metabolit ceramide M29 (9%) dan metabolit ceramida M30 (7%)).
Penghapusan
Pelepasan darah fingolimod adalah 6,3 ± 2,3 L / jam dan min jangka hayat penghapusan terminal (t1 / 2) adalah 6-9 hari. Tahap darah fingolimod dan fingolimod fosfat menurun selari dalam fasa terminal, sehingga menghasilkan separuh yang serupa -kehidupan untuk kedua-dua molekul.
Selepas pemberian oral kira-kira 81% daripada dos perlahan dikeluarkan dalam air kencing sebagai metabolit yang tidak aktif. Fingolimod dan fingolimod fosfat tidak diekskresikan tidak berubah dalam air kencing tetapi terdapat sebagai komponen utama dalam tinja, dengan jumlah masing-masing mewakili kurang daripada 2.5% dos Selepas 34 hari pemulihan dos yang diberikan adalah 89%.
Lineariti
Kepekatan fingolimod dan fingolimod fosfat meningkat secara proporsional dengan dos selepas pemberian dos harian tunggal sebanyak 0.5 mg atau 1.25 mg.
Ciri-ciri dalam populasi tertentu
Farmakokinetik fingolimod dan fingolimod fosfat tidak dibezakan antara lelaki dan wanita, pada pesakit yang berlainan etnik atau pada pesakit dengan gangguan ginjal ringan hingga teruk.
Pada subjek dengan gangguan hepatik ringan, sederhana atau teruk (Child-Pugh kelas A, B dan C) tidak ada perubahan pada jari jari Cmax, sementara AUC fingolimod meningkat 12%, 44% dan 103%. Pada pesakit dengan gangguan hati yang teruk ( Child-Pugh kelas C), Cmax fosfat fingolimod menurun sebanyak 22% dan AUC tidak banyak berubah. Farmakokinetik fosfat fingolimod belum dinilai pada pesakit dengan gangguan hepatik ringan hingga sederhana. Waktu paruh penghapusan fingolimod tidak berubah pada subjek dengan gangguan hepatik ringan, sementara itu meningkat sekitar 50% pada pesakit dengan gangguan hepatik sederhana atau teruk.
Fingolimod tidak boleh digunakan pada pesakit dengan gangguan hati yang teruk (Child-Pugh kelas C) (lihat bahagian 4.3). Terapi Fingolimod harus dimulakan dengan berhati-hati pada pasien dengan gangguan hati ringan dan sederhana (lihat bahagian 4.2).
Pengalaman klinikal dan data farmakokinetik pada pesakit berusia lebih dari 65 tahun adalah terhad.Gilenya harus digunakan dengan berhati-hati pada pesakit berusia 65 tahun ke atas (lihat bahagian 4.2).
Populasi kanak-kanak
Data dari kajian pemindahan buah pinggang termasuk 7 kanak-kanak berumur lebih dari 11 tahun adalah terhad (kajian FTY720A0115). Perbandingan data ini dengan data sukarelawan dewasa yang sihat tidak relevan dan tidak ada kesimpulan yang bermakna mengenai sifat farmakokinetik fingolimod pada kanak-kanak.
05.3 Data keselamatan praklinikal
Profil keselamatan preklinikal fingolimod dinilai pada tikus, tikus, anjing dan monyet. Organ sasaran utama adalah sistem limfoid (limfopenia dan atrofi limfoid), paru-paru (kenaikan berat badan, hipertrofi otot licin di persimpangan bronkioloalveolar), dan dalam pelbagai spesies jantung (kesan kronotropik negatif, peningkatan tekanan darah, perubahan perivaskular dan miokardium) kemerosotan); dalam kajian 2 tahun, fingolimod aktif pada saluran darah (vasculopathy) hanya pada tikus pada dos 0.15 mg / kg dan ke atas, bersamaan dengan kira-kira 4 kali pendedahan sistemik manusia (AUC) pada dos harian 0., 5 mg.
Tidak ada bukti karsinogenisitas yang diamati dalam kajian 2 tahun pada tikus dengan dos oral fingolimod hingga dos toleransi maksimum 2.5 mg / kg, yang mewakili margin kira-kira 50 kali pendedahan sistemik manusia (AUC) pada dos 0,5 mg. Walau bagaimanapun, dalam kajian 2 tahun pada tikus, kejadian limfoma ganas yang lebih tinggi diperhatikan pada dos 0.25 mg / kg dan lebih tinggi, bersamaan dengan kira-kira 6 kali pendedahan manusia. Sistemik (AUC) pada dos harian 0.5 mg.
Dalam kajian haiwan, fingolimod tidak ditemukan mutagenik atau klastogenik.
Fingolimod tidak berpengaruh pada jumlah / motilitas sperma atau kesuburan tikus jantan dan betina hingga dos maksimum yang diuji (10 mg / kg), yang mewakili margin kira-kira 150 kali pendedahan sistemik manusia (AUC) pada dos harian 0.5 mg.
Fingolimod terbukti teratogenik pada tikus apabila diberikan pada dos 0.1 mg / kg atau lebih tinggi. Malformasi viseral janin yang paling biasa termasuk batang arteri yang berterusan dan kecacatan septum ventrikel. Potensi teratogenik pada arnab tidak dapat dinilai sepenuhnya, namun peningkatan kematian embrio-janin diperhatikan pada dos 1.5 mg / kg dan ke atas, dan penurunan janin yang layak serta penundaan pertumbuhan janin pada dos 5 mg / kg. Kg.
Pada tikus, kelangsungan hidup generasi F1 anak anjing menurun pada awal masa selepas bersalin pada dos yang tidak menyebabkan ketoksikan ibu. Walau bagaimanapun, generasi F1 tidak terpengaruh dengan rawatan fingolimod berkaitan dengan berat badan, perkembangan, tingkah laku dan kesuburan.
Fingolimod diekskresikan dalam susu haiwan menyusui yang dirawat.Fingolimod dan metabolitnya melintasi penghalang plasenta pada arnab hamil.
Penilaian Risiko Alam Sekitar (Penilaian Risiko Alam Sekitar, ADA)
Tidak dijangkakan risiko persekitaran dari penggunaan Gilenya oleh pesakit dengan sklerosis berulang.
06.0 MAKLUMAT FARMASI
06.1 Eksipien
Kandungan kapsul:
Magnesium stearat
Mannitol
Cangkang kapsul:
Oksida besi kuning (E172)
Titanium dioksida (E171)
Jeli
Dakwat:
Lacquer (E904)
Alkohol kering
Alkohol Isopropil
Butil alkohol
Propilena glikol
Air yang disucikan
Larutan ammonia pekat
Kalium hidroksida
Oksida besi hitam (E172)
Oksida besi kuning (E172)
Titanium dioksida (E171)
Dimethicone
06.2 Ketidaksesuaian
Tidak relevan.
06.3 Tempoh sah
2 tahun.
06.4 Langkah berjaga-jaga khas untuk penyimpanan
Jangan simpan di atas 25 ° C.
Simpan dalam bungkusan asal untuk melindungi ubat daripada kelembapan.
06.5 Sifat pembungkusan segera dan kandungan bungkusan
Pek yang mengandungi 7, 28 atau 98 kapsul keras atau berbungkus yang mengandungi 84 (3 pek 28) dalam lepuh PVC / PVDC / aluminium.
Pek yang mengandungi 7 x 1 kapsul keras dalam lepuh dos unit berlubang dalam PVC / PVDC / aluminium.
Tidak semua saiz pek boleh dipasarkan.
06.6 Arahan penggunaan dan pengendalian
Tiada arahan khas.
07.0 PEMEGANG KEBENARAN PEMASARAN
Novartis Europharm Limited
Jalan Wimblehurst
Horsham
Sussex Barat, RH12 5AB
UK
08.0 NOMBOR KEBENARAN PEMASARAN
EU / 1/11/677 / 001-006
040949012
040949024
040949036
040949048
040949051
09.0 TARIKH KEBENARAN ATAU PEMBAHARUAN KEBENARAN
17.03.2011
10.0 TARIKH SEMAKAN TEKS
Jun 2014