Bahan aktif: Magaldrato
RIOPAN 800 mg tablet kunyah
Sisip pakej Riopan tersedia untuk saiz pek:- RIOPAN 800 mg tablet kunyah
- Gel oral RIOPAN 80 mg / ml
Mengapa Riopan digunakan? Untuk apa itu?
Kumpulan farmakoterapeutik
RIOPAN adalah antasid.
Tindakan bahan aktifnya magaldrate dilakukan dengan meneutralkan asid gastrik.
Petunjuk terapeutik
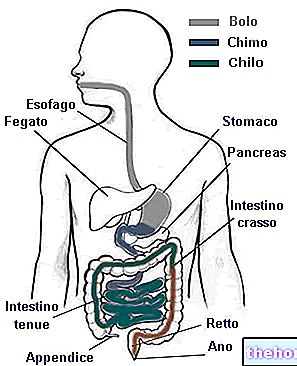
RIOPAN digunakan untuk rawatan ulser duodenum dan gastrik dan esofagitis refluks.
Ia juga digunakan dalam rawatan gejala gastritis dan gastro-duodenitis pelbagai jenis yang dicirikan oleh hiperasiditas.
Kontraindikasi Apabila Riopan tidak boleh digunakan
- Hipersensitiviti terhadap bahan aktif dan / atau salah satu daripada eksipien
- Porphyria
- Hipofosfatemia
- Kegagalan buah pinggang yang teruk
- Kontraindikasi pada usia pediatrik
- Keadaan cachexia
Langkah berjaga-jaga untuk penggunaan Apa yang perlu anda ketahui sebelum mengambil Riopan
RIOPAN tidak boleh digunakan pada kanak-kanak di bawah usia 12 tahun kerana pengalaman rawatan terhad pada kumpulan usia ini.
Pada pesakit dengan fungsi ginjal yang terganggu (pelepasan kreatinin <30 ml / min) RIOPAN hanya boleh digunakan di bawah pemantauan kadar magnesium dan aluminium serum secara berkala. Tahap aluminium serum tidak boleh melebihi 40 ng / mL.
Perhatian khusus harus diberikan pada pesakit yang menjalani dialisis kerana kemungkinan terdapat hubungan antara tahap aluminium serum yang tinggi dan perkembangan ensefalopati.
Tahap peningkatan serum aluminium serum kadang-kadang diperhatikan pada subjek dengan fungsi ginjal yang normal.
Penggunaan antasid yang mengandungi aluminium secara berpanjangan dapat mengurangkan penyerapan fosfat.
Interaksi Dadah atau makanan mana yang boleh mengubah kesan Riopan
Oleh kerana antasid dapat mempengaruhi penyerapan ubat lain yang diambil pada masa yang sama, 1-2 jam harus berlalu antara pengambilan RIOPAN dan pengambilan ubat lain.
Khususnya, semasa penggunaan antasid, pengurangan ketara dalam penyerapan tetrasiklin dan turunan quinolone seperti ciprofloxacin, ofloxacin dan norfloxacin diperhatikan.
Pengurangan penyerapan digoxin, isoniazid, sediaan besi dan klorpromazin yang sederhana dapat diperhatikan apabila diberikan bersamaan dengan RIOPAN.
Kemungkinan peningkatan kesan antikoagulan derivatif kumarin dapat dikesan.
Pengambilan antasid yang mengandungi aluminium dengan minuman berasid (jus buah, anggur, dll.) Atau dengan tablet effervescent yang mengandungi asid sitrik atau tartarik meningkatkan penyerapan aluminium usus. RIOPAN boleh mempengaruhi penyerapan benzodiazepin, indometasin dan asid cheno dan ursodeoxycholic.
Beritahu doktor atau ahli farmasi anda jika anda mengambil atau baru-baru ini mengambil ubat lain, walaupun ubat-ubatan tanpa preskripsi.
Amaran Penting untuk mengetahui bahawa:
Pada kanak-kanak, kemungkinan intoleransi fruktosa keturunan yang tidak dikenali harus dipertimbangkan.
Setiap tablet kunyah mengandung 0,774 g sorbitol. Oleh itu, dos yang disyorkan boleh diambil sehingga 6,2 g sorbitol sehari. Sekiranya terdapat intoleransi terhadap beberapa gula, berjumpa dengan doktor anda sebelum mengambil ubat ini.
Oleh kerana tablet kunyah memiliki kandungan natrium yang rendah, tablet ini juga dapat digunakan oleh pesakit dengan tekanan darah tinggi.
Amaran untuk pesakit diabetes: Satu tablet kunyah mengandungi 0,07 unit roti.
Kehamilan dan penyusuan
Minta nasihat doktor atau ahli farmasi anda sebelum mengambil sebarang ubat
Penggunaan semasa kehamilan tidak digalakkan.
Tidak ada data yang mencukupi mengenai penggunaan RIOPAN pada kehamilan.
Dalam kajian haiwan, pemberian garam aluminium memberi kesan buruk kepada keturunan. Potensi risiko untuk manusia tidak diketahui.
Sebatian aluminium masuk ke dalam susu ibu. Kerana penyerapan yang rendah, dipercayai bahawa tidak ada risiko pada bayi baru lahir.
Maklumat penting mengenai beberapa ramuan
Sekiranya anda diberitahu oleh doktor bahawa anda mempunyai intoleransi terhadap beberapa gula, hubungi doktor anda sebelum mengambil produk ubat ini.
Memandu dan menggunakan mesin
Tidak ada kesan RIOPAN yang diketahui terhadap kemampuan memandu dan menggunakan mesin. Walau bagaimanapun, ubat tersebut tidak mungkin mengganggu kemampuan anda untuk memandu dan / atau menggunakan mesin.
Dos dan kaedah penggunaan Cara menggunakan Riopan: Dos
Kecuali ditetapkan lain, satu tablet RIOPAN 800 mg akan diambil empat kali sehari, satu jam selepas makan utama dan tepat sebelum tidur. Tablet harus dikunyah atau dihisap.
Dos yang lebih tinggi jika diperlukan boleh digunakan dengan preskripsi dan di bawah pengawasan perubatan yang ketat; dalam semua kes, secepat mungkin, dos harus dikurangkan hingga mencukupi untuk mengawal gejala.
Dos harian 6400 mg tidak boleh melebihi.
Tempoh rawatan
Rawatan harus diteruskan sekurang-kurangnya 4 minggu walaupun gejala telah hilang.
Sekiranya gejala berterusan selama lebih dari 2 minggu selama rawatan, pemeriksaan klinikal harus dilakukan untuk mengesampingkan penyakit ganas.
Kumpulan pesakit tertentu
Pesakit Pediatrik: Jangan gunakan pada kanak-kanak di bawah umur 12 tahun kerana pengalaman rawatan terhad pada kumpulan umur ini.
Overdosis Apa yang perlu dilakukan jika anda mengambil terlalu banyak Riopan
Tindakan yang perlu diambil sekiranya berlaku overdosis
Tidak ada fenomena mabuk akut yang diketahui. Pengalaman dengan overdosis yang disengajakan sangat terhad. Kes overdosis dengan garam aluminium lebih cenderung berlaku pada pesakit dengan kegagalan buah pinggang kronik yang teruk dengan gejala berikut: ensefalopati, sawan dan demensia. Seperti semua kes overdosis, rawatan harus bersifat simptomatik, mengambil generik langkah-langkah sokongan.
Sekiranya pengambilan / pengambilan dos berlebihan RIOPAN secara tidak sengaja, beritahu doktor anda dengan segera atau pergi ke hospital terdekat.
Kelakuan yang harus dipatuhi sekiranya satu atau lebih dos dihilangkan
Jangan berikan dos berganda untuk menebus dos RIOPAN yang dilupakan. Sekiranya anda mempunyai pertanyaan lebih lanjut mengenai penggunaan RIOPAN, tanyakan kepada doktor atau ahli farmasi anda.
Kesan Sampingan Apakah kesan sampingan Riopan
Seperti semua ubat, Riopan boleh menyebabkan kesan sampingan, walaupun tidak semua orang mengalaminya.
Sangat biasa (≥ 1/10), biasa (≥ 1/100 - <1/10), tidak biasa (≥ 1/1000 - <1/100), jarang (≥ 1/10000 - <1/1000), sangat jarang termasuk kes terpencil (≤ 1/10000), tidak diketahui (frekuensi tidak dapat dianggarkan dari data yang ada).
Gangguan sistem imun
Kekerapan tidak diketahui: reaksi hipersensitiviti.
Gangguan saluran gastrousus
Sangat biasa: najis longgar
Sangat jarang berlaku: cirit-birit
Kekerapan tidak diketahui: loya dan muntah
Sorbitol, komponen tablet kunyah RIOPAN, boleh menyebabkan sakit perut dan cirit-birit.
Pada pesakit dengan kekurangan buah pinggang dan selama penggunaan yang berpanjangan pada dosis tinggi, aluminium dapat disimpan, terutama pada tisu saraf dan tulang, dan penipisan fosfat mungkin terjadi.
Mematuhi arahan yang terdapat dalam risalah bungkusan mengurangkan risiko kesan yang tidak diingini.
Sekiranya ada kesan sampingan yang serius, atau jika anda melihat kesan sampingan yang tidak disenaraikan dalam risalah ini, sila beritahu doktor atau ahli farmasi anda.
Tamat Tempoh dan Pengekalan
Luput: lihat tarikh luput yang dicetak pada bungkusan
Tarikh luput merujuk kepada produk dalam bungkusan yang disimpan dengan betul dan betul. Amaran: Jangan gunakan ubat selepas tarikh luput yang tertera pada bungkusan
Simpan pada suhu di bawah 30 ° C
Ubat tidak boleh dibuang melalui air sisa atau sampah isi rumah. Tanya ahli farmasi anda bagaimana membuang ubat yang tidak lagi anda gunakan. Ini akan membantu melindungi alam sekitar.
Jauhkan ubat ini dari jarak dan jangkauan kanak-kanak
Bentuk komposisi dan farmaseutikal
Komposisi
Satu tablet kunyah mengandungi:
Bahan aktif: magaldrate anhidrat 800 mg
Eksipien: macrogol 4000, rasa karamel, kalsium kacang, rasa krim, maltol, sorbitol.
Bentuk dan kandungan farmaseutikal
Tablet kunyah atau larut di dalam mulut. Kotak 40 tablet
Produk ini juga terdapat dalam gel oral, botol 250 ml dan 10 ml sachet.
Risalah Pakej Sumber: AIFA (Badan Perubatan Itali). Kandungan yang diterbitkan pada Januari 2016. Maklumat yang ada mungkin tidak terkini.
Untuk mempunyai akses ke versi paling terkini, disarankan untuk mengakses laman web AIFA (Badan Perubatan Itali). Penafian dan maklumat berguna.
01.0 NAMA PRODUK PERUBATAN
RIOPAN
02.0 KOMPOSISI KUALITATIF DAN KUANTITATIF
RIOPAN 800 mg tablet kunyah
Satu tablet mengandungi: anhidrat magaldrate 800.0 mg
Eksipien: sorbitol
Untuk senarai lengkap eksipien, lihat bahagian 6.1
Gel oral RIOPAN 80 mg / ml
1 ml gel mengandungi: anhidrat magaldrate 80.0 mg
Eksipien: maltol
Untuk senarai lengkap eksipien, lihat bahagian 6.1
03.0 BORANG FARMASI
Tablet untuk mengunyah atau larut di dalam mulut.
Gel oral
04.0 MAKLUMAT KLINIKAL
04.1 Petunjuk terapeutik
Rawatan ulser duodenum dan gastrik dan esofagitis refluks; rawatan simptomatik gastritis dan gastro-duodenitis pelbagai etiologi yang dicirikan oleh hiperasidensi.
04.2 Posologi dan kaedah pentadbiran
RIOPAN 800 mg tablet kunyah
Melainkan ditetapkan, satu tablet RIOPAN 800 mg akan diambil empat kali sehari, satu jam selepas makan utama dan tepat sebelum tidur.
Tablet mesti dikunyah atau dilarutkan di dalam mulut.
Gel oral RIOPAN 80 mg / ml
Kecuali dinyatakan lain, 10 ml (sepadan dengan dua sudu teh) atau kandungan satu sachet gel RIOPAN, empat kali sehari, satu "jam selepas makan utama dan tepat sebelum tidur.
Untuk kegunaan: goncangkan botol dengan kuat atau homogenkan kandungan sachet, memanipulasinya sebelum membukanya.
Dosis yang lebih tinggi, jika diperlukan, dari kedua-dua tablet dan gel, boleh digunakan berdasarkan resep atau di bawah pengawasan perubatan yang ketat: dalam semua kes, secepat mungkin, dos akan dikurangkan hingga mencukupi untuk mengawal gejala.
Dos harian 6400 mg tidak boleh melebihi.
Rawatan harus diteruskan sekurang-kurangnya 4 minggu walaupun gejala telah hilang. Sekiranya gejala berterusan selama lebih dari 2 minggu selama rawatan, pemeriksaan klinikal harus dilakukan untuk mengesampingkan penyakit ganas.
Pesakit Pediatrik: Jangan gunakan pada kanak-kanak di bawah umur 12 tahun kerana pengalaman rawatan terhad pada kumpulan umur ini.
04.3 Kontraindikasi
• Hipersensitiviti terhadap bahan aktif dan / atau salah satu daripada eksipien
• Porphyria
• Hipofosfatemia
• Kekurangan buah pinggang yang teruk (lihat bahagian 4.4)
• Kontraindikasi pada usia pediatrik
• Keadaan cachexia
04.4 Amaran khas dan langkah berjaga-jaga yang sesuai untuk digunakan
RIOPAN tidak boleh digunakan pada kanak-kanak di bawah usia 12 tahun kerana pengalaman rawatan terhad pada kumpulan usia ini.
Pada pesakit dengan fungsi ginjal yang terganggu (pelepasan magnesium dan aluminium serum kreatinin. Tahap serum aluminium tidak boleh melebihi 40 ng / ml.
Perhatian khusus harus diberikan pada pesakit yang menjalani dialisis kerana kemungkinan terdapat hubungan antara tahap aluminium serum yang tinggi dan perkembangan ensefalopati.
Tahap aluminium serum yang cukup tinggi kadang-kadang diperhatikan pada subjek dengan fungsi ginjal normal (lihat bahagian 5.2 Sifat farmakokinetik).
Penggunaan antasid aluminium yang berpanjangan dapat mengurangkan penyerapan fosfat.
Untuk tablet kunyah RIOPAN:
Pada kanak-kanak, kemungkinan intoleransi fruktosa keturunan yang tidak dikenali harus dipertimbangkan.
Setiap tablet kunyah mengandung 0,774 g sorbitol.Oleh itu, dos yang disyorkan boleh diambil sehingga 6,2 g sorbitol sehari. Pesakit dengan masalah keturunan yang jarang berlaku kerana intoleransi sorbitol tidak boleh mengambil ubat ini.
Oleh kerana tablet kunyah memiliki kandungan natrium yang rendah, tablet ini juga dapat digunakan oleh pesakit dengan tekanan darah tinggi.
Amaran untuk pesakit diabetes: Satu tablet kunyah mengandungi 0,07 unit roti.
Gel oral RIOPAN 80 mg / ml
Goncangkan botol dengan kuat sebelum digunakan.
Homogenkan kandungan sachet dengan memanipulasinya sebelum membukanya.
04.5 Interaksi dengan produk ubat lain dan bentuk interaksi lain
Oleh kerana antasid dapat mempengaruhi penyerapan ubat lain yang diambil pada masa yang sama, 1-2 jam harus berlalu antara pengambilan RIOPAN dan pengambilan ubat lain.
Khususnya, semasa penggunaan antasid, pengurangan ketara dalam penyerapan tetrasiklin dan turunan quinolone, seperti ciprofloxacin, ofloxacin dan norfloxacin, telah diperhatikan.
Pengurangan penyerapan digoxin, isoniazid, sediaan besi dan klorpromazin yang sederhana dapat diperhatikan apabila diberikan bersamaan dengan RIOPAN.
Kemungkinan peningkatan kesan antikoagulan derivatif kumarin dapat dikesan.
Pengambilan antasid yang mengandungi aluminium dengan minuman berasid (jus buah, anggur dll) atau dengan tablet effervescent yang mengandungi asid sitrik atau tartarik meningkatkan penyerapan aluminium usus. RIOPAN boleh mempengaruhi penyerapan benzodiazepin, indometasin dan asid cheno dan ursodeoxycholic.
04.6 Kehamilan dan penyusuan
Penggunaan semasa kehamilan tidak digalakkan.
Tidak ada data yang mencukupi mengenai penggunaan RIOPAN pada kehamilan.
Dalam kajian haiwan, pemberian garam aluminium memberi kesan buruk kepada keturunan. Potensi risiko untuk manusia tidak diketahui.
Sebatian aluminium masuk ke dalam susu ibu. Kerana penyerapan yang rendah, dipercayai bahawa tidak ada risiko pada bayi baru lahir.
04.7 Kesan terhadap kemampuan memandu dan menggunakan mesin
Tidak ada kesan RIOPAN yang diketahui terhadap kemampuan memandu dan menggunakan mesin. Walau bagaimanapun, ubat tersebut tidak mungkin mengganggu kemampuan anda untuk memandu dan / atau menggunakan mesin.
04.8 Kesan yang tidak diingini
Sangat biasa (≥1 / 10),
biasa (≥1 / 100 -
tidak biasa (≥1 / 1000 -
jarang berlaku (≥1 / 10,000 -
sangat jarang berlaku termasuk kes terpencil (≤1 / 10,000),
tidak diketahui (frekuensi tidak dapat dianggarkan dari data yang ada).
Gangguan sistem imun
Kekerapan tidak diketahui: reaksi hipersensitiviti
Gangguan saluran gastrousus
Sangat biasa: Najis longgar
Sangat jarang berlaku: Cirit-birit
Kekerapan tidak diketahui: loya dan muntah
Sorbitol, komponen tablet kunyah RIOPAN, boleh menyebabkan sakit perut dan cirit-birit. Pada pesakit dengan kekurangan buah pinggang dan selama penggunaan yang berpanjangan pada dosis tinggi, aluminium dapat disimpan, terutama pada tisu saraf dan tulang, dan penipisan fosfat mungkin terjadi.
04.9 Overdosis
Tidak ada fenomena mabuk akut yang diketahui. Pengalaman dengan overdosis yang disengajakan sangat terhad. Kes overdosis dengan garam aluminium lebih cenderung berlaku pada pesakit dengan kekurangan buah pinggang kronik yang teruk dengan gejala berikut: ensefalopati, sawan dan demensia. Seperti dalam semua kes overdosis, rawatan harus tanpa gejala, berlaku langkah-langkah sokongan generik.
05.0 HARTA FARMAKOLOGI
05.1 Sifat farmakodinamik
ATC: A02AD02: antasid
Tindakan magaldrate dilakukan melalui peneutralan asid gastrik. Ia juga mempunyai ikatan yang bergantung pada dos dan bergantung pada pH dengan asid hempedu dan lysolecithin. Aktiviti antasid dikaitkan dengan pengikatan proton dengan ion sulfat dan hidroksida lapisan interstisial, sehingga struktur kisi terbelah semasa peneutralan.
800 mg magaldrate meneutralkan kira-kira 18-25 mEq asid hidroklorik.
05.2 Sifat farmakokinetik
- Am
Magaldrato tidak diserap dari saluran gastrointestinal. Semasa proses peneutralan, ion magnesium dan aluminium dalam kuantiti kecil dibebaskan yang, semasa transit usus, diubah menjadi fosfat larut terhad dan diekskresikan dalam tinja. Sebilangan kation diserap. Tahap peningkatan serum aluminium serum kadang-kadang diperhatikan pada subjek dengan fungsi ginjal yang normal. Penggunaan antasid aluminium yang berpanjangan dapat mengurangkan penyerapan fosfat.
- Ciri-ciri pada pesakit / kumpulan mata pelajaran khas
Oleh kerana terdapat kemungkinan korelasi antara peningkatan kadar aluminium serum dan perkembangan ensefalopati, perlu diberi perhatian khusus pada pesakit yang menjalani dialisis.
Dalam rawatan jangka panjang, kepekatan aluminium dalam darah harus dipantau secara berkala dan tidak boleh melebihi 40 ng / ml.
Pada pesakit dengan fungsi ginjal yang terganggu, pengumpulan plasma dan tisu (kerana aluminium terkumpul terutamanya pada tisu saraf dan tulang) dan fenomena overdosis mungkin berlaku.
05.3 Data keselamatan praklinikal
Ketoksikan akut belum dapat ditentukan kerana penyerapan rendah (10% untuk magnesium dan kira-kira 1% untuk aluminium) dan perkumuhan buah pinggang yang agak cepat.
Potensi mutagenik magaldrate belum diselidiki dengan secukupnya. Untuk sebatian aluminium tidak ada bukti potensi mutagenik yang relevan.
Tidak ada kajian karsinogenik dengan magaldrate.
Tidak ada kajian embryotoxicity pada haiwan. Tidak ada bukti risiko kecacatan pada manusia. Kesan embriooksik dan foetotoksik telah diperhatikan dalam kajian dengan sebatian aluminium lain. Kajian pada tikus menunjukkan peningkatan kematian selepas bersalin dan kelewatan perkembangan neuromotor janin.
06.0 MAKLUMAT FARMASI
06.1 Eksipien
RIOPAN 800 mg tablet kunyah
Macrogol 4000, rasa karamel, kalsium kacang, rasa krim, maltol, sorbitol
Gel oral RIOPAN 80 mg / ml
Gum arabic, hypromellose, maltol, karamel esen, esen krim, simethicone emulsi, sodium cyclamate, 20% chlorhexidine digluconate, silver sulfate, air purified.
06.2 Ketidaksesuaian
Tiada
06.3 Tempoh sah
RIOPAN 800 mg tablet kunyah: 3 tahun
Gel oral RIOPAN 80 mg / ml: 5 tahun
Botol gel oral Riopan 250 ml: kestabilan kimia dan fizikal semasa penggunaan telah ditunjukkan selama 6 bulan.Dari sudut mikrobiologi, setelah dibuka, produk dapat disimpan hingga 6 bulan.
06.4 Langkah berjaga-jaga khas untuk penyimpanan
RIOPAN 800 mg tablet kunyah: simpan di bawah 30 ° C.
Gel oral RIOPAN 80 mg / ml: jangan sejukkan atau beku.
06.5 Sifat pembungkusan segera dan kandungan bungkusan
RIOPAN 800 mg tablet kunyah: Lepuh PVC-PVDC-aluminium masing-masing 10 tablet.
Gel oral RIOPAN 80 mg / ml:
a) botol 250 ml polipropilena putih dengan penutup polietilena putih dan kolar jaminan
b) 10 ml sachet dalam lamina aluminium-poliena.
06.6 Arahan penggunaan dan pengendalian
Tiada arahan khas
07.0 PEMEGANG KEBENARAN PEMASARAN
Takeda Italia SpA - Via Elio Vittorini 129 - 00144 Rome
08.0 NOMBOR KEBENARAN PEMASARAN
RIOPAN 800 mg tablet kunyah, 40 tablet: A.I.C. n. 027103023
RIOPAN 80 mg / ml gel oral, botol 250 ml: A.I.C. n. 027103047
RIOPAN 80 mg / ml oral gel, 40 sachet 10 ml: A.I.C. n. 027103035
09.0 TARIKH KEBENARAN ATAU PEMBAHARUAN KEBENARAN
Pembaharuan: Jun 2010.
10.0 TARIKH SEMAKAN TEKS
September 2013