Bahan aktif: Febuxostat
Tablet bersalut filem ADENURIC 80 mg
Tablet bersalut filem ADENURIC 120 mg
Mengapa Adenuric digunakan? Untuk apa itu?
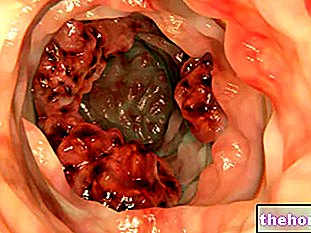
Tablet ADENURIC mengandungi zat aktif febuxostat dan digunakan untuk merawat gout, penyakit yang berkaitan dengan terlalu banyak asid urik (urat) di dalam badan. Pada sesetengah orang, jumlah asid urik yang terkumpul dalam darah boleh menjadi terlalu banyak. tetap dalam larutan. Dalam kes ini, kristal urat boleh terbentuk di dalam dan sekitar sendi dan buah pinggang. Kristal ini boleh menyebabkan kesakitan, kemerahan, kehangatan dan pembengkakan pada sendi (serangan gout) secara tiba-tiba. Sekiranya tidak dirawat, deposit yang lebih besar, yang disebut tophi, dapat terbentuk di dalam dan di sekitar sendi. Tophi boleh merosakkan sendi dan tulang.
ADENURIC berfungsi dengan mengurangkan kadar asid urik. Mengekalkan kadar asid urik yang rendah dengan mengambil ADENURIC sekali sehari mencegah pengumpulan kristal, dan dari masa ke masa mengurangkan gejala. Sekiranya tahap asid urik disimpan rendah untuk jangka masa yang panjang, tophi juga dapat diserap semula.
Tablet ADENURIC 120 mg juga digunakan untuk rawatan dan pencegahan kadar asid urik dalam darah tinggi yang mungkin berlaku dalam kes kemoterapi untuk barah darah. Sel-sel kanser musnah semasa rawatan kemoterapi dan kadar asid urik dalam darah meningkat kecuali pembentukan asid ini dapat dicegah.
ADENURIC adalah untuk orang dewasa.
Kontraindikasi Apabila Adenuric tidak boleh digunakan
Jangan mengambil ADENURIC:
- Sekiranya anda alah kepada febuxostat atau bahan-bahan lain dari ubat ini
Langkah berjaga-jaga untuk penggunaan Apa yang perlu anda ketahui sebelum mengambil Adenuric
Bercakap dengan doktor anda sebelum mengambil ADENURIC:
- Sekiranya anda pernah atau pernah mengalami kegagalan jantung atau masalah jantung yang lain
- Sekiranya anda pernah atau pernah menghidapi penyakit buah pinggang dan / atau reaksi alergi yang teruk terhadap allopurinol (ubat yang digunakan untuk merawat gout)
- Sekiranya anda pernah atau pernah mengalami penyakit hati atau kelainan ujian fungsi hati
- Sekiranya anda mempunyai tahap asid urik yang tinggi kerana sindrom Lesch-Nyhan (keadaan yang jarang diwarisi di mana terdapat terlalu banyak asid urik dalam darah)
- Sekiranya anda mempunyai masalah tiroid.
Sekiranya reaksi alergi terhadap ADENURIC berlaku, hentikan pengambilan ubat. Kemungkinan gejala tindak balas alahan adalah:
- ruam termasuk bentuk yang teruk (mis. lepuh, benjolan, ruam gatal, ruam pengelupasan), gatal-gatal
- bengkak anggota badan atau muka
- kesukaran bernafas
- demam dengan kelenjar getah bening yang membengkak
- tetapi juga keadaan alahan yang teruk dan mengancam nyawa dengan serangan jantung dan peredaran darah.
Doktor anda mungkin memutuskan untuk menghentikan rawatan Adenurik anda secara kekal.
Ruam kulit yang jarang dan mengancam nyawa (sindrom Stevens-Johnson) telah dilaporkan dengan penggunaan ADENURIC dan pada mulanya muncul di bagasi sebagai tompok kemerahan atau tompok bulat sering dengan lepuh pusat. Mereka juga boleh merangkumi bisul. Di mulut, tekak, hidung, alat kelamin dan konjungtivitis (mata merah dan bengkak). Ruam boleh menyebabkan lecet atau pengelupasan kulit yang meluas.
Sekiranya anda menghidapi sindrom Stevens-Johnson dengan penggunaan febuxostat, rawatan dengan ADENURIC tidak boleh dimulakan lagi. Sekiranya anda mengalami ruam atau gejala kulit ini, segera berjumpa doktor dan beritahu dia bahawa anda sedang dirawat dengan ubat ini. .
Sekiranya anda sedang mengalami serangan gout (tiba-tiba rasa sakit yang teruk, kelembutan, kemerahan, kehangatan dan bengkak pada satu sendi), tunggu sehingga serangan gout berhenti sebelum memulakan terapi dengan ADENURIC.
Pada sesetengah orang, serangan gout dapat meletus pada awal terapi tertentu yang digunakan untuk mengawal kadar asid urik. Tidak semua orang mengalami eksaserbasi, tetapi anda juga mungkin mengalami eksaserbasi ketika mengambil ADENURIC, terutama pada beberapa minggu atau bulan pertama terapi. Penting untuk anda terus mengambil ADENURIC walaupun anda mengalami peningkatan, kerana ADENURIC terus berusaha menurunkan kadar asid urik anda. Sekiranya anda terus mengambil ADENURIC setiap hari, dari masa ke masa, timbulnya kemerosotan lebih jarang dan akan menjadi kurang dan tidak menyakitkan.
Doktor anda akan sering menetapkan ubat-ubatan lain, jika diperlukan, untuk membantu mencegah atau merawat gejala-gejala flare-up (seperti sakit dan bengkak pada 'sendi').
Pada pesakit dengan kadar urat yang sangat tinggi (contohnya pesakit yang menjalani kemoterapi), rawatan dengan ubat-ubatan yang menurunkan kadar asid urik boleh menyebabkan xanthine berkumpul di saluran kencing dengan kemungkinan pembentukan batu, walaupun ini belum diperhatikan. Pada pesakit yang dirawat dengan ADENURIC untuk Tumor Sindrom Lisis.
Doktor anda mungkin memerintahkan ujian darah untuk memeriksa bahawa hati anda berfungsi dengan normal.
Kanak-kanak dan remaja
Jangan berikan ubat ini kepada kanak-kanak di bawah usia 18 tahun kerana keselamatan dan keberkesanannya belum dapat dipastikan.
Interaksi Ubat atau makanan mana yang boleh mengubah kesan Adenuric
Beritahu doktor atau ahli farmasi anda jika anda mengambil, baru-baru ini mengambil, atau mungkin mengambil ubat lain, walaupun ubat yang diperoleh tanpa preskripsi.
Adalah sangat penting anda memberitahu doktor atau ahli farmasi anda jika anda mengambil ubat yang mengandungi bahan berikut, kerana ini mungkin berinteraksi dengan ADENURIC dan doktor anda mungkin ingin mempertimbangkan langkah-langkah yang sesuai:
- Mercaptopurine (digunakan untuk merawat barah)
- Azathioprine (digunakan untuk mengurangkan tindak balas imun)
- Theophylline (digunakan untuk merawat asma)
Amaran Penting untuk mengetahui bahawa:
Kehamilan dan penyusuan
Tidak diketahui sama ada ADENURIC boleh membahayakan bayi yang belum lahir. ADENURIC tidak boleh digunakan semasa mengandung. Tidak diketahui sama ada ADENURIC masuk ke dalam susu ibu. Anda tidak boleh mengambil ADENURIC jika anda menyusu atau berhasrat untuk melakukannya.
Sekiranya anda hamil atau menyusu, fikir anda mungkin mengandung atau merancang untuk mempunyai bayi, minta nasihat doktor atau ahli farmasi anda sebelum mengambil ubat ini.
Memandu dan menggunakan mesin
Ketahuilah bahawa anda mungkin merasa pening, mengantuk, penglihatan kabur, mati rasa atau kesemutan semasa rawatan, dan jika gejala ini berlaku, anda tidak boleh memandu atau mengendalikan mesin.
ADENURIC mengandungi laktosa
Tablet ADENURIC mengandungi laktosa (sejenis gula). Sekiranya anda tahu bahawa anda tidak bertoleransi dengan gula, berbincanglah dengan doktor anda sebelum mengambil ubat ini.
Dos, Kaedah dan Masa Pentadbiran Cara menggunakan Adenurik: Posologi
Sentiasa ambil ubat ini tepat seperti yang diberitahu oleh doktor anda. Sekiranya anda tidak pasti, anda harus berjumpa doktor atau ahli farmasi anda.
- Dos biasa adalah satu tablet sehari. Bahagian belakang jalur menunjukkan hari-hari dalam seminggu untuk membantu anda memastikan bahawa anda telah mengambil dos anda setiap hari.
- Tablet mesti diminum. Anda boleh membawa mereka dekat atau menjauhkan diri dari makanan.
Hiperurisemia kronik dengan pemendapan urat ADENURIC boleh didapati dalam bentuk tablet 80 mg atau 120 mg. Doktor anda akan menetapkan dos yang paling sesuai untuk anda.
Terus minum ADENURIC setiap hari, walaupun anda tidak mengalami serangan suar atau gout.
Pencegahan dan rawatan peningkatan kadar asid urik pada pesakit yang menjalani kemoterapi ADENURIC boleh didapati dalam bentuk 120 mg tablet.
Mulailah mengambil ADENURIC dua hari sebelum kemoterapi dan terus mengambilnya mengikut nasihat doktor anda. Penggunaan biasanya tidak lama.
Overdosis Apa yang perlu dilakukan jika anda mengambil terlalu banyak Adenuric
Sekiranya anda mengambil lebih banyak ADENURIC daripada yang sepatutnya
Sekiranya berlaku overdosis yang tidak disengajakan, tanyakan kepada doktor anda apa yang harus dilakukan atau hubungi bilik kecemasan terdekat.
Sekiranya anda terlupa mengambil ADENURIC
Sekiranya anda lupa mengambil dos ADENURIC, ambil segera setelah anda menyedarinya, kecuali sudah hampir masanya untuk dos seterusnya. Dalam kes ini, langkau dos yang tidak dijawab dan ambil dos seterusnya pada waktu yang dijadualkan. Jangan mengambil dos berganda untuk menebus dos yang dilupakan.
Sekiranya anda berhenti mengambil ADENURIC
Jangan berhenti mengambil ADENURIC tanpa kebenaran doktor anda, walaupun anda berasa lebih baik. Sekiranya anda berhenti mengambil ADENURIC, tahap asid urik anda mungkin mulai meningkat dan gejala anda mungkin bertambah buruk kerana pembentukan kristal urat baru di dalam dan sekitar sendi dan buah pinggang anda.
Sekiranya anda mempunyai pertanyaan lebih lanjut mengenai penggunaan ubat ini, tanyakan kepada doktor atau ahli farmasi anda.
Kesan Sampingan Apakah kesan sampingan Adenuric
Seperti semua ubat, ubat ini boleh menyebabkan kesan sampingan, walaupun tidak semua orang mendapatnya.
Berhenti mengambil ubat dan segera hubungi doktor anda atau pergi ke bilik kecemasan terdekat jika anda mengalami kesan sampingan yang jarang berlaku (mungkin mempengaruhi sehingga 1 dari 1,000 orang), kerana tindak balas alergi yang teruk boleh berlaku:
- reaksi anafilaksis, hipersensitiviti ubat (lihat juga bahagian "Amaran dan Langkah berjaga-jaga")
- Ruam kulit yang mengancam nyawa dicirikan oleh melepuh dan mengelupas kulit dan permukaan dalaman rongga badan, mis. mulut dan alat kelamin, bisul yang menyakitkan di mulut dan / atau kawasan kemaluan, disertai oleh demam, sakit tekak dan keletihan (sindrom Stevens-Johnson / nekrolisis epidermis toksik), atau kelenjar getah bening yang membesar, hati yang membesar, hepatitis (hingga kegagalan hati), peningkatan jumlah sel darah putih (reaksi ubat dengan eosinofilia dan gejala sistemik - DRESS).
- ruam umum
Kesan sampingan yang biasa (boleh mempengaruhi sehingga 1 dari 10 orang) adalah:
- keabnormalan dalam keputusan ujian fungsi hati
- cirit-birit
- sakit kepala
- ruam (termasuk pelbagai jenis ruam kulit, lihat di bawah "tidak biasa" dan "jarang")
- loya
- peningkatan gejala gout
- bengkak setempat kerana pengekalan cecair di tisu (edema)
Kesan sampingan lain yang tidak disebutkan di atas disenaraikan di bawah.
Kesan sampingan yang tidak biasa (boleh mempengaruhi sehingga 1 dari 100 orang) adalah:
- penurunan selera makan, perubahan kadar gula darah (diabetes) yang gejala mungkin dahaga berlebihan, peningkatan kadar lemak darah, kenaikan berat badan
- kehilangan libido (keinginan seksual)
- sukar tidur, mengantuk
- pening, mati rasa, kesemutan, sensasi taktil yang dikurangkan atau diubah (hypoesthesia, hemiparesis atau paraesthesia), perubahan rasa (dysgeusia), penurunan deria bau (hyposmia)
- kelainan pada jejak ECG, degupan jantung tidak teratur atau cepat, persepsi degupan jantung (berdebar-debar)
- kemerahan atau kemerahan (mis. kemerahan pada muka atau leher), peningkatan tekanan darah, pendarahan (pendarahan, hanya dilihat pada pesakit yang menjalani kemoterapi kerana gangguan darah)
- batuk, sesak nafas, sakit dada, radang saluran hidung dan / atau kerongkong (jangkitan saluran pernafasan), bronkitis
- mulut kering, sakit perut atau ketidakselesaan, gas berlebihan, pedih ulu hati / senak, sembelit, pergerakan usus yang lebih kerap, muntah, ketidakselesaan perut
- gatal-gatal, gatal-gatal, radang kulit, perubahan warna kulit, bintik-bintik merah atau ungu kecil pada kulit, bintik-bintik merah rata pada kulit, kawasan merah pada kulit ditutup dengan benjolan kecil, ruam, kawasan kemerahan dan bintik-bintik pada kulit, gangguan kulit yang lain
- kekejangan otot, kelemahan otot, sakit otot atau sendi, bursitis atau artritis (keradangan sendi biasanya disertai dengan sakit, bengkak dan / atau kekakuan), sakit di bahagian kaki, sakit belakang, kekejangan otot
- darah dalam air kencing, peningkatan kekerapan membuang air kecil, hasil ujian air kencing yang tidak normal (peningkatan kadar protein dalam air kencing) penurunan keupayaan ginjal untuk berfungsi dengan baik
- keletihan, sakit dada, ketidakselesaan dada
- batu di pundi hempedu atau saluran empedu (cholelithiasis)
- peningkatan tahap hormon perangsang tiroid (TSH)
- perubahan dalam ujian biokimia darah atau jumlah sel darah merah atau platelet (perubahan dalam keputusan ujian darah)
- Batu karang
- kesukaran mendapat ereksi
Kesan sampingan yang jarang berlaku (boleh mempengaruhi sehingga 1 dari 1000 orang) adalah:
- kerosakan otot, keadaan yang jarang berlaku boleh menjadi serius. Masalah otot boleh berkembang dan khususnya, jika anda merasa tidak sihat atau demam tinggi pada masa yang sama, ini mungkin disebabkan oleh kerosakan sel otot yang tidak normal. Segera hubungi doktor anda sekiranya anda mengalami sakit otot, kelembutan atau kelemahan
- pembengkakan ketara pada lapisan kulit yang lebih dalam, terutamanya di sekitar bibir, mata, alat kelamin, tangan, kaki atau lidah, dengan kemungkinan sukar bernafas
- demam tinggi yang berkaitan dengan ruam kulit seperti campak, kelenjar getah bening yang membesar, hati yang membesar, hepatitis (hingga kegagalan hati), peningkatan jumlah sel darah putih (leukositosis, sama ada berkaitan atau tidak dengan eosinofilia)
- kemerahan kulit (eritema), ruam dalam pelbagai jenis (misalnya gatal, tompok putih, lepuh, lepuh yang mengandung nanah, mengelupas kulit, ruam seperti campak), eritema meresap, nekrosis dan lecet epidermis dan membran mukus , mengakibatkan pengelupasan dan kemungkinan sepsis (sindrom Stevens-Johnson / nekrolisis epidermis toksik)
- rasa gementar
- dahaga
- berdering di telinga
- penglihatan kabur, perubahan penglihatan
- keguguran rambut
- ulserasi bukal
- keradangan pankreas: gejala biasa adalah sakit perut, mual dan muntah
- peningkatan berpeluh
- penurunan berat badan, peningkatan selera makan, kehilangan selera makan yang tidak terkawal (anoreksia)
- kekejangan otot dan / atau sendi
- tahap sel darah rendah yang tidak normal (sel darah putih atau sel darah merah atau platelet)
- keinginan untuk membuang air kecil
- perubahan atau penurunan jumlah dalam air kencing kerana keradangan pada buah pinggang (nefritis tubulointerstitial)
- keradangan hati (hepatitis)
- menguning kulit (penyakit kuning)
- kerosakan hati
Sekiranya anda mendapat kesan sampingan, berbincanglah dengan doktor atau ahli farmasi anda. Ini termasuk kemungkinan kesan sampingan yang tidak disenaraikan dalam risalah ini.
Melaporkan kesan sampingan
Sekiranya anda mendapat kesan sampingan, berbincanglah dengan doktor atau ahli farmasi anda. Ini termasuk kemungkinan kesan sampingan yang tidak disenaraikan dalam risalah ini. Anda juga boleh melaporkan kesan sampingan secara langsung melalui sistem pelaporan nasional yang disenaraikan dalam Lampiran V. Dengan melaporkan kesan sampingan, anda dapat membantu memberikan lebih banyak maklumat mengenai keselamatan ubat ini.
Tamat Tempoh dan Pengekalan
Jauhkan ubat ini dari pandangan dan jangkauan kanak-kanak.
- Jangan gunakan ubat tersebut selepas tarikh luput yang tertera pada kadbod dan pada kertas lepuh tablet selepas "EXP". Tarikh luput merujuk pada hari terakhir dalam sebulan.
- Produk ubat ini tidak memerlukan syarat penyimpanan khas.
Jangan buang ubat melalui air buangan atau sampah rumah. Tanya ahli farmasi anda bagaimana membuang ubat yang tidak lagi anda gunakan. Ini akan membantu melindungi alam sekitar.
Apa yang dikandung oleh ADENURIC
Bahan aktifnya adalah febuxostat.
Setiap tablet mengandungi 80 mg atau 120 mg febuxostat.
Eksipien adalah:
Inti tablet: laktosa monohidrat, selulosa mikrokristal, magnesium stearat, hidroksipropilselulosa, natrium croscarmellose, siloid hidrat koloid.
Lapisan tablet: Opadry II kuning, 85F42129 mengandung: polivinil alkohol, titanium dioksida (E171), makrogol jenis 3350, talc, besi oksida kuning (E172).
Seperti apa ADENURIC dan kandungan peknya
Tablet bersalut filem ADENURIC berwarna kuning pucat / kuning dan berbentuk kapsul. Tablet bersalut filem 80 mg dilekatkan dengan "80" di satu sisi. Tablet bersalut filem 120 mg dilekatkan dengan "120" di satu sisi.
ADENURIC 80 mg dan 120 mg dibungkus dalam lepuh lutsinar (Aclar / PVC / Aluminium) yang mengandungi 14 tablet.
ADENURIC 80 mg dan 120 mg boleh didapati dalam pek tablet bersalut filem 14, 28, 42, 56, 84 dan 98.
Tidak semua saiz pek boleh dipasarkan.
Risalah Pakej Sumber: AIFA (Badan Perubatan Itali). Kandungan yang diterbitkan pada Januari 2016. Maklumat yang ada mungkin tidak terkini.
Untuk mempunyai akses ke versi paling terkini, disarankan untuk mengakses laman web AIFA (Badan Perubatan Itali). Penafian dan maklumat berguna.
01.0 NAMA PRODUK PERUBATAN
TABEL ADENURIC 80 MG DILAPAT DENGAN FILM
02.0 KOMPOSISI KUALITATIF DAN KUANTITATIF
Setiap tablet mengandungi 80 mg febuxostat.
Eksipien dengan kesan yang diketahui:
Setiap tablet mengandungi 76.50 mg laktosa (sebagai monohidrat)
Untuk senarai lengkap eksipien, lihat bahagian 6.1.
03.0 BORANG FARMASI
Tablet bersalut filem (tablet).
Tablet muda berwarna kuning / kuning, bersalut filem, berbentuk kapsul dengan "80" tertera pada satu sisi.
04.0 MAKLUMAT KLINIKAL
04.1 Petunjuk terapeutik
Rawatan hiperuricaemia kronik dengan pemendapan urat (termasuk sejarah, atau adanya, tophi dan / atau gouty arthritis).
ADENURIC ditunjukkan pada orang dewasa.
04.2 Posologi dan kaedah pentadbiran
Dos
Dos oral ADENURIC yang disyorkan adalah 80 mg sekali sehari dan boleh diambil sama ada dekat atau jauh dari makanan. Dengan nilai asid urik serum> 6 mg / dL (357 μmol / L) selepas 2-4 minggu, ADENURIC 120 mg sekali sehari mungkin dipertimbangkan.
ADENURIC berfungsi cukup cepat untuk membolehkan penentuan baru asid urik serum selepas 2 minggu. Matlamat terapi adalah untuk mengurangkan dan mengekalkan tahap asid urik serum di bawah 6 mg / dL (357 μmol / L).
Tempoh rawatan sekurang-kurangnya 6 bulan disyorkan untuk profilaksis eksaserbasi gout (lihat bahagian 4.4).
Mata pelajaran warga tua
Tidak perlu penyesuaian dos pada orang tua (lihat bahagian 5.2).
Kerosakan buah pinggang
Keberkesanan dan keselamatan produk ubat belum sepenuhnya terbukti pada pesakit dengan gangguan ginjal yang teruk (pelepasan kreatinin
Tidak perlu penyesuaian dos pada pesakit dengan gangguan ginjal ringan atau sederhana.
Kerosakan hepatik
Keberkesanan dan keselamatan febuxostat belum dikaji pada pesakit dengan gangguan hati yang teruk (Child Pugh kelas C).
Dos yang disyorkan untuk pesakit dengan gangguan hepatik ringan adalah 80 mg. Terdapat maklumat terhad mengenai penggunaan produk ubat pada pesakit dengan gangguan hati yang sederhana.
Populasi kanak-kanak
Keselamatan dan keberkesanan ADENURIC pada kanak-kanak berumur di bawah 18 tahun belum dapat dipastikan. Data tidak tersedia.
Kaedah pentadbiran
Penggunaan secara lisan
ADENURIC mesti diberikan secara oral dan boleh diambil dengan atau tanpa makanan.
04.3 Kontraindikasi
Hipersensitiviti terhadap bahan aktif atau salah satu daripada eksipien yang disenaraikan dalam bahagian 6.1 (lihat juga bahagian 4.8).
04.4 Amaran khas dan langkah berjaga-jaga yang sesuai untuk digunakan
Gangguan kardio-vaskular
Rawatan dengan febuxostat tidak digalakkan pada pesakit dengan penyakit jantung iskemia atau kegagalan jantung kongestif.
Terdapat kejadian kejadian kardiovaskular APTC yang dilaporkan oleh penyiasat (titik akhir yang ditentukan oleh "Kolaborasi Trialis Anti-Platelet) (termasuk kematian kardiovaskular, infark miokard bukan fatal, strok tidak fatal) pada kumpulan febuxostat berbanding dengan yang dirawat dengan allopurinol dalam kajian APEX dan FACT (1.3 berbanding 0.3 kejadian setiap 100 tahun pesakit), tetapi tidak dalam kajian CONFIRMS (lihat bahagian 5.1 untuk ciri kajian terperinci). Kejadian kejadian kardiovaskular APTC yang dilaporkan oleh penyiasat dalam kajian fasa 3 yang dikumpulkan (APEX, FACT, dan CONFIRMS) adalah 0.7 berbanding 0.6 kejadian setiap 100 tahun pesakit.
Dalam kajian lanjutan jangka panjang, kejadian kejadian APTC yang dilaporkan oleh penyiasat adalah 1.2 dan 0.6 kejadian setiap 100 tahun pesakit untuk febuxostat dan allopurinol. Tidak ada perbezaan yang signifikan secara statistik dan tidak ada hubungan kausal dengan febuxostat. Faktor risiko yang dikenal pasti untuk pesakit ini adalah sejarah klinikal penyakit aterosklerotik dan / atau infark miokard, atau kegagalan jantung kongestif.
Alergi / hipersensitiviti terhadap ubat
Laporan jarang mengenai reaksi alergi / hipersensitiviti yang teruk termasuk sindrom Stevens-Johnson yang mengancam nyawa, nekrolisis epidermis toksik dan reaksi / kejutan anafilaksis akut telah dikumpulkan dalam tempoh selepas pemasaran. Dalam kebanyakan kes, reaksi ini berlaku pada bulan pertama terapi febuxostat. Sebilangan, tetapi tidak semua, pesakit ini telah melaporkan gangguan ginjal dan / atau hipersensitiviti terdahulu terhadap allopurinol. Dalam beberapa kes, reaksi hipersensitiviti yang teruk, termasuk reaksi ubat dengan eosinofilia dan gejala sistemik (DRESS) telah dikaitkan dengan demam, penglibatan hematologi, renal atau hepatik. Pesakit harus diberitahu mengenai tanda-tanda dan gejala dan dipantau dengan teliti untuk gejala reaksi alergi / hipersensitiviti (lihat bahagian 4.8). Rawatan dengan febuxostat harus dihentikan segera jika berlaku reaksi alergi / hipersensitiviti yang teruk, termasuk sindrom Stevens-Johnson, pencegahan rawatan pencegahan dikaitkan dengan prognosis yang lebih baik. Sekiranya pesakit mengalami reaksi alergi / hipersensitiviti, termasuk sindrom Stevens-Johnson dan reaksi / kejutan anafilaksis akut, febuxostat tidak boleh diberikan lagi.
Serangan gout akut (suar)
Rawatan dengan febuxostat tidak boleh dimulakan sehingga serangan gout akut telah sembuh sepenuhnya. Pada permulaan terapi, flare-up gout mungkin berlaku disebabkan oleh perubahan tahap asid urik serum, yang terjadi. Menentukan setelah mobilisasi urat dari deposit tisu (lihat bahagian 4.8 dan 5.1). Pada permulaan rawatan dengan febuxostat, disyorkan profilaksis terhadap kemunculan gout sekurang-kurangnya 6 bulan menggunakan NSAID atau colchicine (lihat bahagian 4.2).
Sekiranya kemunculan gout berlaku semasa rawatan dengan febuxostat, ia tidak boleh dihentikan. Eksaserbasi harus dirawat secara serentak, sesuai dengan keperluan setiap pesakit. Rawatan berterusan dengan febuxostat mengurangkan kekerapan dan intensiti suar gout.
Pemendapan xanthine
Pada pesakit di mana kadar urat terbentuk meningkat (contohnya pada neoplasma malignan dan semasa rawatan mereka atau dalam sindrom Lesch-Nyhan), kepekatan mutlak xanthine dalam air kencing boleh, dalam kes yang jarang berlaku, meningkat dalam ukuran yang memungkinkan depositnya di saluran kencing. Oleh kerana tidak ada pengalaman dengan febuxostat, penggunaannya dalam kategori pesakit ini tidak digalakkan.
Mercaptopurine / azathioprine
Penggunaan febuxostat tidak dianjurkan pada pasien yang dirawat bersamaan dengan mercaptopurine / azathioprine. Pengurangan dos mercaptopurine atau azathioprine disyorkan untuk mengelakkan kemungkinan kesan hematologi (lihat bahagian 4.5).
Subjek yang telah menjalani pemindahan organ
Oleh kerana tidak ada pengalaman dengan penggunaan ADENURIC pada penerima transplantasi organ, penggunaan febuxostat tidak dianjurkan pada pasien ini (lihat bahagian 5.1).
Theophylline
Pentadbiran bersama febuxostat 80 mg dan theophylline 400 mg sebagai dos tunggal pada subjek sihat menunjukkan ketiadaan interaksi farmakokinetik (lihat bahagian 4.5). Febuxostat 80 mg boleh digunakan pada pesakit yang dirawat bersamaan dengan theophylline tanpa risiko peningkatan tahap plasma theophylline Tidak ada data yang tersedia untuk febuxostat 120 mg.
Penyakit hati
Semasa ujian klinikal fasa 3 gabungan, kelainan ujian fungsi hati ringan (5.0%) diperhatikan pada pesakit yang dirawat dengan febuxostat. Ujian fungsi hati dianjurkan sebelum memulai terapi febuxostat dan pada selang waktu berkala setelah itu dinilai oleh doktor (lihat bahagian 5.1).
Penyakit kelenjar tiroid
Dalam kajian peluasan label terbuka jangka panjang, peningkatan nilai TSH (> 5.5 mcIU / mL) diperhatikan pada pesakit jangka panjang yang dirawat dengan febuxostat (5.5%). Perhatian harus digunakan dengan febuxostat pada pesakit dengan fungsi tiroid yang terganggu (lihat bahagian 5.1).
Laktosa
Tablet Febuxostat mengandungi laktosa. Pesakit dengan intoleransi galaktosa keturunan yang jarang berlaku, kekurangan laktase Lapp atau sindrom penyerapan glukosa-galaktosa tidak boleh mengambil ubat ini.
04.5 Interaksi dengan produk ubat lain dan bentuk interaksi lain
Mercaptopurine / azathioprine
Berdasarkan mekanisme tindakan febuxostat terhadap penghambatan xanthine oxidase (XO), penggunaan ADENURIC bersamaan dengan mercaptopurine / azathioprine tidak digalakkan. Pencegahan XO oleh febuxostat boleh menyebabkan peningkatan kepekatan plasma ubat ini, yang membawa kepada toksisitas (lihat bahagian 4.4 ). Tidak ada kajian interaksi febuxostat dengan ubat metabolisme XO yang dilakukan.
Tidak ada kajian interaksi yang dilakukan antara kemoterapi febuxostat dan sitotoksik. Tidak ada data mengenai keselamatan febuxostat yang digunakan bersamaan dengan terapi sitotoksik.
Substrat Rosiglitazone / CYP2C8
Febuxostat telah terbukti sebagai perencat lemah CYP2C8 in vitro. Dalam kajian pada subjek yang sihat, pemberian bersama febuxostat 120 mg sekali sehari dengan dos rosiglitazone 4 mg oral tidak memberi kesan terhadap farmakokinetik rosiglitazone dan metabolitnya N-desmethyl rosiglitazone, menunjukkan bahawa febuxostat bukan penghambat enzim CYP2C8 in vivo. Oleh itu, penggunaan febuxostat dan rosiglitazone atau substrat CYP2C8 yang lain tidak dijangka memerlukan penyesuaian dos untuk sebatian ini.
Theophylline
Kajian interaksi dengan febuxostat dilakukan pada subjek yang sihat untuk menilai sama ada penghambatan XO dapat menyebabkan peningkatan tahap teofilin beredar, seperti yang dilaporkan untuk perencat XO lain. Hasil kajian menunjukkan bahawa pemberian bersama febuxostat, 80 mg sekali sehari, dan theophylline, 400 mg dos tunggal, tidak mempengaruhi farmakokinetik dan keselamatan teofilin. Oleh itu, tidak perlu berhati-hati apabila febuxostat 80 mg dan theophylline diberikan bersamaan. Tidak ada data yang tersedia untuk febuxostat 120 mg.
Naproxen dan perencat glukuronidasi lain
Metabolisme febuxostat bergantung pada enzim uridine glucuronosyl transferase (UGT). Dadah yang menghalang glukuronidasi, seperti NSAID dan probenecid, secara teorinya dapat mempengaruhi penghapusan febuxostat. Pada subjek yang sihat, penggunaan bersama febuxostat dan naproxen 250 mg dua kali sehari dikaitkan dengan peningkatan pendedahan kepada febuxostat (Cmax 28%, AUC) 41% dan t1 / 2 26%). Dalam kajian klinikal, penggunaan naproxen atau perencat NSAID / Cox-2 lain tidak berkaitan dengan peningkatan kesan sampingan yang signifikan secara klinikal. Febuxostat dapat diberikan bersamaan dengan naproxen, tanpa memerlukan penyesuaian dos febuxostat atau naproxen.
Pengaruh glukuronidasi
Pengaruh enzim UGT yang kuat boleh mengakibatkan peningkatan metabolisme dan penurunan keberkesanan febuxostat. Oleh itu, pemeriksaan asid urik serum disarankan 1-2 minggu setelah permulaan terapi dengan pemicu glukuronidasi yang kuat. Sebaliknya, penghentian rawatan dengan induktor glukuronidasi boleh mengakibatkan dalam peningkatan tahap febuxostat plasma.
Colchicine / indomethacin / hydrochlorothiazide / warfarin
Febuxostat boleh diberikan bersamaan dengan colchicine atau indomethacin tanpa perlu menyesuaikan dos febuxostat atau bahan aktif lain yang diberikan secara bersamaan.
Tidak diperlukan penyesuaian dos febuxostat apabila diberikan bersamaan dengan hidroklorotiazid.
Tidak diperlukan penyesuaian dos warfarin apabila diberikan bersamaan dengan febuxostat. Pentadbiran febuxostat (80 mg atau 120 mg sekali sehari) dengan warfarin tidak mempengaruhi farmakokinetik warfarin pada pesakit yang sihat. Selanjutnya, INR dan Faktor VII yang diaktifkan tidak dipengaruhi oleh pentadbiran febuxostat.
Substrat Desipramine / CYP2D6
Febuxostat telah terbukti sebagai perencat lemah CYP2D6 secara in vitro. Dalam kajian pada subjek yang sihat, 120 mg ADENURIC sekali sehari menghasilkan peningkatan min sebanyak 22% dalam AUC desipramine, substrat CYP2D6, menunjukkan kemungkinan tindakan perencatan lemah febuxostat pada enzim CYP2D6. dalam vivo. Sekiranya berlaku bersamaan febuxostat dan substrat CYP2D6 yang lain, oleh itu, keperluan penyesuaian dos untuk sebatian ini tidak dapat dibayangkan.
Antasid
Telah ditunjukkan bahawa pengambilan antasid serentak yang mengandungi magnesium hidroksida dan aluminium hidroksida menunda penyerapan febuxostat (sekitar 1 jam) dan menyebabkan penurunan Cmax sebanyak 32%, sementara tidak ada perubahan yang signifikan yang diperhatikan berkaitan dengan "AUC" . Oleh itu, adalah mungkin untuk mengambil febuxostat tanpa mengambil kira penggunaan ubat antasid.
04.6 Kehamilan dan penyusuan
Kehamilan
Data mengenai jumlah kehamilan terdedah yang sangat terhad menunjukkan tiada kesan febuxostat yang tidak diingini terhadap kehamilan atau kesihatan janin / bayi baru lahir. Kajian pada haiwan tidak menunjukkan kesan berbahaya secara langsung atau tidak langsung terhadap kehamilan, perkembangan embrio / janin atau kelahiran (lihat bahagian 5.3). Potensi risiko untuk manusia tidak diketahui. Febuxostat tidak boleh digunakan semasa kehamilan.
Masa makan
Tidak diketahui sama ada febuxostat diekskresikan dalam susu manusia. Kajian pada haiwan telah menunjukkan perkumuhan bahan aktif ini dalam susu ibu disertai dengan defisit perkembangan pada bayi yang baru lahir semasa menyusui. Risiko untuk bayi yang disusui tidak dapat dikecualikan. Febuxostat tidak boleh digunakan semasa menyusui. "Menyusui.
Kesuburan
Dalam kajian pembiakan haiwan, dos hingga 48 mg / kg / hari tidak menunjukkan kesan buruk yang bergantung pada dos pada kesuburan (lihat bahagian 5.3). Kesan ADENURIC terhadap kesuburan manusia tidak diketahui.
04.7 Kesan terhadap kemampuan memandu dan menggunakan mesin
Kesabaran, pening, paraestesia dan penglihatan kabur telah dilaporkan dengan penggunaan febuxostat. Pesakit harus berhati-hati sebelum memandu, mengoperasikan mesin atau melakukan aktiviti berbahaya sehingga mereka cukup yakin bahawa penggunaan ADENURIC tidak menjejaskan prestasi mereka.
04.8 Kesan yang tidak diingini
Ringkasan profil keselamatan
Reaksi buruk yang paling kerap dilaporkan dalam ujian klinikal (4.072 subjek yang dirawat dengan sekurang-kurangnya dos 10 mg hingga 300 mg) dan pengalaman selepas pemasaran adalah serangan gout akut, kelainan fungsi hati, cirit-birit, mual, sakit kepala, ruam dan edema. tindak balas buruk kebanyakannya ringan atau sederhana. Reaksi hipersensitiviti serius terhadap febuxostat, beberapa di antaranya dikaitkan dengan gejala sistemik, berlaku dalam pengalaman selepas pemasaran.
Jadual senarai tindak balas buruk
Reaksi buruk yang biasa (≥1 / 100 -
Jadual 1: Reaksi buruk yang dilaporkan dalam kajian fasa III gabungan jangka panjang dan pengalaman selepas pemasaran
* Reaksi buruk yang dikumpulkan dalam pengalaman selepas pemasaran
** Rawatan diare yang tidak berjangkit dan ujian fungsi hati yang tidak normal dalam kajian fasa 3 gabungan lebih kerap berlaku pada pesakit yang dirawat bersamaan dengan kolkisin.
*** Lihat bahagian 5.1 untuk kejadian serangan gout dalam percubaan terkawal rawak fasa 3 individu.
Penerangan mengenai tindak balas buruk yang dipilih
Kes-kes reaksi hipersensitiviti yang teruk terhadap febuxostat, termasuk sindrom Stevens-Johnson, nekrolisis epidermal toksik dan reaksi anafilaksis / kejutan, telah berlaku dalam pengalaman selepas pemasaran. Sindrom Stevens-Johnson dan nekrolisis epidermis toksik dicirikan oleh letusan kulit progresif yang berkaitan dengan lepuh atau luka mukosa. dan kerengsaan mata.
Reaksi hipersensitiviti terhadap febuxostat mungkin dikaitkan dengan gejala berikut: reaksi kulit yang dicirikan oleh ruam makulopapular yang menyusup, ruam umum atau pengelupasan, tetapi juga luka kulit, edema muka, demam, perubahan hematologi seperti trombositopenia dan eosinofilia, dan penglibatan organ tunggal atau berbilang ( hati dan ginjal, termasuk nefritis tubulointerstitial) (lihat bahagian 4.4).
Serangan gout akut biasanya diperhatikan sejurus permulaan rawatan dan selama beberapa bulan pertama. Selepas itu, kekerapan serangan gout berkurang bergantung pada masa. Profilaksis serangan gout akut disyorkan (lihat bahagian 4.2 dan 4.4).
Melaporkan tindak balas buruk yang disyaki
Melaporkan tindak balas buruk yang disyaki berlaku setelah kebenaran produk ubat adalah penting kerana ia memungkinkan pemantauan berterusan terhadap keseimbangan manfaat / risiko produk ubat tersebut. Profesional penjagaan kesihatan diminta untuk melaporkan sebarang reaksi buruk yang disyaki melalui sistem pelaporan nasional. "Alamat https: //www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 Overdosis
Sekiranya berlaku overdosis, pesakit harus diberi rawatan simptomatik dan sokongan.
05.0 HARTA FARMAKOLOGI
05.1 Sifat farmakodinamik
Kumpulan farmakoterapi: Persediaan antigout, sediaan yang menghalang pengeluaran asid urik.
Kod ATC: M04AA03
Mekanisme tindakan
Asid urik adalah produk akhir metabolisme purin dan pada manusia ia dihasilkan mengikut urutan hypoxanthine → xanthine → asid urik. Kedua-dua langkah tindak balas di atas dikatalisis oleh xanthine oxidase (XO). Febuxostat adalah turunan 2 -arylthiazole yang mempunyai kesan terapeutik untuk mengurangkan asid urik serum melalui perencatan selektif XO. Febuxostat adalah perencat selektif kuat, bukan purin, XO (NP-SIXO) dengan nilai Ki (perencatan d "berterusan) secara in vitro kurang daripada 1 nanomolar. Febuxostat telah terbukti dapat menghambat XO dengan keberkesanan yang hebat, baik dalam bentuk teroksidasi dan dalam bentuk berkurang. Pada kepekatan terapeutik, febuxostat tidak menghalang enzim lain yang terlibat dalam metabolisme purin atau pyrimidines, iaitu guanine deaminase, hypoxanthine-guanine phosphoribosyltransferase, orotate phosphoribosyltransferase, orotidine monophosphate decarboxylase atau purine nucleosylase.
Keberkesanan dan keselamatan klinikal
Keberkesanan ADENURIC ditunjukkan dalam tiga kajian fasa 3 penting (dua kajian utama APEX dan FACT, dan kajian CONFIRMS tambahan yang dijelaskan di bawah) yang dilakukan pada 4,101 pesakit dengan hiperuricaemia dan gout. Dalam setiap kajian fasa 3 penting, ADENURIC menunjukkan kemampuan yang lebih besar daripada allopurinol untuk mengurangkan dan mengekalkan kadar asid urik serum. Titik akhir keberkesanan utama dalam kajian APEX dan FAKTA adalah peratusan pesakit di mana kadar asid urik serum dalam 3 bulan terakhir menghasilkan
Kajian APEX: APEX (Allopurinol and Placebo-Controlled Efficacy of Febuxostat-Study of the efficacy of febuxostat dikendalikan terhadap allopurinol dan plasebo) adalah Tahap 3, kajian rawak, double-blind, multicenter, selama 28 minggu. 1.072 pesakit secara rawak. yang menerima: plasebo (n = 134), ADENURIC 80 mg sekali sehari (n = 267), ADENURIC 120 mg sekali sehari (n = 269), ADENURIC 240 mg sekali sehari (n = 134) o allopurinol (pada dos 300 mg sekali sehari [n = 258] untuk pesakit dengan kreatinin serum awal ≤1,5 mg / dL atau pada dos 100 mg sekali sehari [n = 10] untuk pesakit dengan kreatinin serum awal> 1,5 mg / dL dan ≤2,0 mg / dL ) Dosis 240 mg febuxostat (sama dengan dua kali dos maksimum yang disyorkan) digunakan untuk penilaian keselamatan.
Kajian APEX menunjukkan keunggulan yang signifikan secara statistik bagi kumpulan yang dirawat dengan ADENURIC 80 mg sekali sehari dan ADENURIC 120 mg sekali sehari dalam menurunkan asid urik serum ke paras di bawah 6 mg / dL (357 μmol / L) berbanding dengan kumpulan yang diberi dos allopurinol konvensional 300 mg (n = 258) / 100 mg (n = 10) (lihat Jadual 2 dan Rajah 1). Kajian FAKTA: FAKTA (Percubaan terkawal Febuxostat Allopurinol) adalah kajian 52 minggu, rawak, double-blind, multicentre, phase 3. 760 pesakit secara rawak menerima: ADENURIC 80 mg sekali sehari (n = 256), ADENURIC 120 mg sekali sehari (n = 251), atau allopurinol 300 mg sekali sehari (n = 253).
Kajian FACT menunjukkan kelebihan yang signifikan secara statistik dari kumpulan ADENURIC 80 mg dan ADENURIC 120 mg sekali sehari dalam menurunkan dan mengekalkan asid urik serum di bawah 6 mg / dL (357 μmol / L) berbanding dengan kumpulan yang dirawat dengan dos allopurinol konvensional 300 mg.
Jadual 2 merangkum hasil titik akhir keberkesanan utama:
Jadual 2
Peratusan pesakit dengan kadar asid urik serum
Tiga lawatan bulanan terakhir
Keupayaan ADENURIC untuk menurunkan kadar asid urik serum adalah cepat dan berterusan. Pengurangan kadar asid urik serum kepada nilai
Kajian CONFIRMS: Kajian CONFIRMS adalah kajian fasa 3 selama 26 minggu, secara rawak, terkawal, untuk menilai keselamatan dan keberkesanan febuxostat 40 mg dan 80 mg, dibandingkan dengan allopurinol 300 mg atau 200 mg, pada pesakit dengan gout dan hiperuricaemia. pesakit secara rawak: ADENURIC 40 mg sekali sehari (n = 757), ADENURIC 80 mg sekali sehari (n = 756) atau allopurinol 300/200 mg sekali sehari (n = 756). 65% pesakit mengalami gangguan buah pinggang ringan hingga sederhana ( dengan pelepasan kreatinin 30-89 mL / min) Profilaksis gout adalah wajib melebihi tempoh 26 minggu.
Bahagian pesakit dengan kadar urat serum μmol / L pada lawatan terakhir adalah 45% untuk 40 mg febuxostat, 67% untuk 80 mg febuxostat dan 42% untuk allopurinol 300/200 mg, masing-masing.
Titik akhir utama dalam subkumpulan pesakit dengan gangguan buah pinggang
Kajian APEX menilai keberkesanan ubat pada 40 pesakit dengan gangguan ginjal (serum awal kreatinin> 1,5 mg / dL dan ≤ 2,0 mg / dL). Bagi pesakit dengan gangguan ginjal yang secara rawak menerima allopurinol, dos terakhir terhad kepada 100 mg sehari sekali. ADENURIC mencapai titik akhir keberkesanan primer masing-masing pada 44% (80 mg sekali sehari), 45% (120 mg sekali sehari), dan 60% (240 mg sekali sehari) berbanding dengan 0% yang terdapat dalam 100 mg allopurinol sekali sehari dan kumpulan plasebo.
Tidak ada perbezaan yang signifikan secara klinikal dalam kadar penurunan kepekatan asid urik serum pada subjek yang sihat tanpa mengira status fungsi buah pinggang mereka (58% pada kumpulan fungsi ginjal normal dan 55% pada kumpulan gangguan buah pinggang yang teruk).
Analisis "pada pesakit dengan gout dan gangguan ginjal didefinisikan secara prospektif dalam kajian CONFIRMS, dan menunjukkan bahawa febuxostat jauh lebih berkesan dalam mengurangkan kadar urat serum daripada
Titik akhir utama dalam subkumpulan pesakit dengan kadar asid urik serum ≥ 10 mg / dL
Kira-kira 40% pesakit (APEX dan FACT diambil bersama) mempunyai nilai asid urik serum awal ≥ 10 mg / dL. Dalam subkumpulan ini ADENURIC mencapai titik akhir keberkesanan utama (tahap asid urik
Dalam kajian CONFIRMS, bahagian pesakit yang memenuhi titik akhir keberkesanan utama (tahap asid urik
Hasil klinikal: Peratusan pesakit yang memerlukan rawatan untuk serangan gout
Kajian APEX: Dalam tempoh profilaksis 8 minggu, sebahagian besar pesakit (36%) yang dirawat dengan febuxostat 120 mg memerlukan rawatan untuk serangan gout daripada febuxostat 80 mg (28%), allopurinol 300 mg (23%) dan plasebo ( 20%). Serangan meningkat selepas tempoh profilaksis dan secara beransur-ansur menurun dari masa ke masa. Antara 46% dan 55% subjek menerima rawatan untuk serangan gout akut dari minggu 8 hingga minggu ke 28. Serangan gout selama 4 minggu terakhir kajian (minggu 24 -28) diperhatikan pada 15% (febuxostat 80, 120 mg), 14% (allopurinol 300 mg) dan 20% (plasebo) pesakit. FAKTA: Dalam tempoh profilaksis 8 minggu, bahagian yang lebih besar (36%) pesakit yang dirawat dengan febuxostat 120 mg memerlukan rawatan untuk mengatasi masalah gout daripada kedua-dua rawatan dengan febuxostat 80 mg (22%) dan allopurinol 300 mg (21%).
Selepas tempoh profilaksis 8 minggu, kejadian serangan akut secara beransur-ansur meningkat dan menurun dari masa ke masa (64% dan 70% subjek mendapat rawatan untuk serangan gout akut dari minggu ke 8 hingga minggu ke 52). Serangan gout selama 4 minggu terakhir kajian (minggu 49-52) diperhatikan pada 6-8% (febuxostat 80 mg, 120 mg) dan 11% (allopurinol 300 mg) pesakit.
Peratusan pesakit yang memerlukan rawatan untuk flare-up gout (APEX dan FACT Studies) secara numerik lebih rendah pada kumpulan yang mencapai tahap urat serum post-baseline.
Semasa kajian CONFIRMS, peratusan pesakit yang memerlukan rawatan untuk serangan gout (Hari 1 hingga Bulan 6) masing-masing adalah 31% dan 25% untuk kumpulan febuxostat 80 mg dan allopurinol. Tidak ada perbezaan dalam bahagian pesakit yang memerlukan rawatan untuk serangan gout antara kumpulan 80 mg dan 40 mg febuxostat.
Kajian peluasan label terbuka jangka panjang
Kajian EXCEL (C02-021): EXCEL adalah kajian lanjutan keselamatan Tahap 3, terbuka, multisentra, rawak, terkawal allopurinol, untuk pesakit yang telah menyelesaikan kajian Fasa 3 yang penting (APEX atau FAKTA). Sebanyak 1.086 pesakit telah mendaftar: ADENURIC 80 mg sekali sehari (n = 649), ADENURIC 120 mg sekali sehari (n = 292) dan allopurinol 300/100 mg sekali sehari (n = 145). Kira-kira 69% pesakit tidak memerlukan perubahan rawatan untuk mencapai tindak balas akhir yang stabil. Pesakit yang mempunyai tiga tahap urica berturut-turut> 6.0 mg / dL ditarik.
Tahap urat serum dipertahankan dari masa ke masa (mis. 91% dan 93% pesakit pada rawatan awal dengan febuxostat 80 mg dan 120 mg, masing-masing, mengalami uricaemia
Data tiga tahun menunjukkan pengurangan kejadian kemunculan gout dengan kurang dari 4% pesakit yang memerlukan rawatan untuk eksaserbasi (iaitu lebih daripada 96% pesakit yang tidak memerlukan rawatan untuk eksaserbasi) setelah 16-24 bulan dan 30- 36 bulan 46% dan 38% pesakit pada rawatan stabil akhir dengan febuxostat 80 mg atau 120 mg sekali sehari, masing-masing, mempunyai penyelesaian lengkap tophus primer yang dapat diraba dari awal hingga lawatan terakhir.
Kajian FOCUS (TMX-01-005): FOCUS adalah kajian pelanjutan keselamatan Tahap 2, label terbuka, multisenter, 5 tahun untuk pesakit yang telah menyelesaikan 4 minggu dos febuxostat dalam kajian TMX double-blind -00-004. 116 pesakit didaftarkan dan pada mulanya menerima febuxostat 80 mg sekali sehari. 62% pesakit tidak memerlukan penyesuaian dos untuk mengekalkan uricaemia
Bahagian pesakit dengan kadar urat serum
Semasa ujian klinikal fasa 3, perubahan ringan pada nilai ujian fungsi hati (5.0%) diperhatikan pada pesakit yang dirawat dengan febuxostat. Nilai-nilai ini serupa dengan yang dilaporkan untuk allopurinol (4.2%) (lihat bahagian 4.4). Peningkatan nilai TSH (> 5.5 mcIU / mL) diperhatikan dalam kajian peluasan label terbuka jangka panjang pada pesakit. dirawat dengan febuxostat (5.5%) dan pada pesakit yang dirawat dengan allopurinol (5.8%) (lihat bahagian 4.4).
05.2 Sifat farmakokinetik
Pada subjek yang sihat, Cmax (kepekatan plasma maksimum) dan AUC (kawasan di bawah kurva) febuxostat meningkat dos secara berkadar selepas pemberian dos tunggal dan berulang dari 10 mg hingga 120 mg. Untuk dos febuxostat antara 120 mg dan 300 mg, lebih besar daripada peningkatan proporsional dos AUC diperhatikan. Tidak ada pengumpulan yang nyata selepas pemberian dos 10 mg hingga 240 mg setiap 24 jam. Febuxostat mempunyai jangka hayat penghapusan terminal yang jelas (t1 / 2) sekitar 5-8 jam.
Analisis farmakokinetik / farmakodinamik populasi dilakukan pada 211 pesakit dengan hiperuricaemia dan gout yang telah dirawat dengan ADENURIC pada dosis 40-240 mg sekali sehari.
Secara umum, parameter farmakokinetik febuxostat, yang dianggarkan oleh analisis ini, konsisten dengan parameter yang diamati pada subjek yang sihat, yang menunjukkan bahawa subjek sihat mewakili untuk tujuan penilaian farmakokinetik / farmakodinamik pada populasi pesakit gout.
Penyerapan
Febuxostat diserap dengan cepat (Tmax 1,0-1,5 jam) dan hampir sepenuhnya (sekurang-kurangnya 84%). Berikutan pemberian satu dos oral atau beberapa dos oral 80 dan 120 mg sekali sehari, Cmax masing-masing kira-kira 2,8-3,2 mcg / mL, dan 5,0-5,3 mcg / mL. Ketersediaan bio mutlak formulasi tablet febuxostat belum dikaji.
Berikutan pemberian beberapa dos oral 80 mg sekali sehari atau dos 120 mg tunggal bersama dengan makanan tinggi lemak, penurunan Cmax masing-masing 49% dan 38%, dan penurunan Cmax diperhatikan. "AUC dari 18 % dan 16% masing-masing.
Walau bagaimanapun, tidak ada perubahan yang signifikan secara klinikal dalam penurunan peratusan kepekatan asid urik serum ketika dinilai (dos berulang 80 mg). Oleh itu, ADENURIC boleh diambil sama ada berdekatan atau jauh dari makan.
Pembahagian
Jumlah pengagihan jelas di keadaan mantap (Vss / F) febuxostat berkisar antara 29 hingga 75 l selepas dos oral 10-300 mg. Pengikatan protein plasma febuxostat adalah sekitar 99.2%, (terutamanya albumin), dan tetap berterusan berbanding kepekatan yang dicapai dengan dos 80 hingga 120 mg. Pengikatan protein metabolit aset metabolit antara 82% dan 91% lebih kurang.
Biotransformasi
Febuxostat dimetabolisme secara meluas melalui konjugasi melalui sistem enzim uridine difosfat glukuronosiltransferase (UDPGT) dan melalui pengoksidaan melalui sistem sitokrom P450 (CYP). Empat metabolit hidroksil aktif secara farmakologi telah dikenal pasti, tiga di antaranya dapat diperhatikan dalam plasma manusia.n vitro dengan mikrosom hati manusia menunjukkan bahawa metabolit oksidatif ini terdiri terutamanya dari CYP1A1, CYP1A2, CYP2C8 atau CYP2C9 dan febuxostat glucuronide terutamanya dari UGT 1A1, 1A8, dan 1A9.
Penghapusan
Febuxostat dihilangkan oleh kedua-dua laluan hepatik dan buah pinggang. Selepas pemberian oral febuxostat berlabel 14C dengan dos 80 mg, kira-kira 49% daripada dos itu pulih dalam air kencing sebagai febuxostat tidak berubah (3%), zat aktif acylglucoronide (30%), metabolit oksidatifnya bersama-sama dengan konjugat mereka (13 %), dan metabolit lain yang tidak diketahui (3%). Sebagai tambahan kepada penghapusan melalui air kencing, kira-kira 45% dos pulih dalam tinja dalam bentuk febuxostat yang tidak berubah (12%), acylglucuronide dari bahan aktif (1%), metabolit oksidatif yang diketahui bersama-sama dengan konjugat mereka (25% , dan metabolit lain yang tidak diketahui (7%).
Kerosakan buah pinggang
Selepas pemberian dos berulang 80 mg ADENURIC pada pesakit dengan gangguan ginjal ringan, sederhana atau teruk, Cmax febuxostat tidak berbeza dengan subjek dengan fungsi ginjal normal. Purata AUC febuxostat meningkat kira-kira 1.8 kali ganda daripada 7.5 mcg.h / mL pada kumpulan fungsi ginjal normal kepada 13.2 mcg.h / mL pada kumpulan gangguan buah pinggang yang teruk. "AUC metabolit aktif meningkat hingga 2 dan 4 lipat, masing-masing. Walau bagaimanapun, tidak perlu penyesuaian dos pada subjek dengan gangguan buah pinggang ringan atau sederhana.
Kerosakan hepatik
Selepas pemberian berulang sebanyak 80 mg ADENURIC pada pesakit dengan gangguan hepatik ringan (Child-Pugh Class A) atau sederhana (Child-Pugh Class B), Cmax dan AUC febuxostat dan metabolitnya tidak berubah dengan ketara. Berbanding dengan subjek yang normal fungsi hepatik Tidak ada kajian yang dilakukan pada pesakit dengan gangguan hati yang teruk (Child-Pugh Class C).
Umur
Tidak ada perubahan ketara dalam AUC febuxostat atau metabolitnya yang diperhatikan setelah pemberian dos oral ADENURIC berulang pada subjek tua berbanding subjek sihat yang lebih muda.
Jenis
Berikutan dos oral ADENURIC berulang, Cmax dan AUC masing-masing 24% dan 12% lebih tinggi daripada wanita pada lelaki. Walau bagaimanapun, Cmax dan AUC yang disesuaikan dengan berat badan serupa untuk kedua-dua jantina. Tidak diperlukan penyesuaian dos berdasarkan jantina.
05.3 Data keselamatan praklinikal
Kesan yang berlaku dalam kajian bukan klinikal umumnya diperhatikan dengan pendedahan ubat melebihi pendedahan maksimum manusia.
Karsinogenesis, mutagenesis, penurunan kesuburan
Pada tikus jantan, peningkatan yang signifikan secara statistik pada tumor pundi kencing (papilloma sel peralihan dan karsinoma) hanya diperhatikan apabila terdapat batu xanthine pada kumpulan yang diberi dos tertinggi, sepadan dengan dos sekitar 11 kali lebih tinggi daripada pendedahan. pada mana-mana jenis tumor lain diperhatikan, baik pada tikus atau tikus jantan, dan juga pada tikus atau tikus betina.Perhatian ini dianggap sebagai akibat metabolisme spesies spesies purin dan komposisi urin dan tidak ada kaitan dengan penggunaan klinikal produk ubat.
Ujian genotoksisiti standard tidak menunjukkan kesan genotoksik febuxostat yang relevan.
Febuxostat pada dos oral hingga 48 mg / kg / hari tidak memberi kesan terhadap kesuburan dan prestasi pembiakan pada tikus jantan dan betina.
Tidak ada bukti penurunan kesuburan, kesan teratogenik atau akibat berbahaya bagi janin akibat tindakan febuxostat. Pada tikus, pada dos yang tinggi dan dengan pendedahan kira-kira 4.3 kali ganda pada manusia, diperhatikan keracunan bagi ibu disertai pengurangan indeks penyapihan dan kelewatan dalam perkembangan keturunan.Kajian teratologi yang dilakukan pada tikus dan arnab hamil dengan pendedahan sekitar 4.3 dan 13 kali ganda bagi manusia, masing-masing tidak mendedahkan kesan teratogenik febuxostat.
06.0 MAKLUMAT FARMASI
06.1 Eksipien
Inti tablet
Laktosa monohidrat
Selulosa mikrokristalin
Magnesium stearat
Hydroxypropylcellulose
Natrium Croscarmellose
Silika, koloid terhidrat
Lapisan tablet
Opadry II, kuning, 85F42129 yang mengandungi:
Polivinil alkohol
Titanium dioksida (E171)
Macrogol jenis 3350
Perbincangan
Oksida besi kuning (E172)
06.2 Ketidaksesuaian
Tidak relevan.
06.3 Tempoh sah
3 tahun.
06.4 Langkah berjaga-jaga khas untuk penyimpanan
Ubat ini tidak memerlukan syarat penyimpanan khas.
06.5 Sifat pembungkusan segera dan kandungan bungkusan
Lepuh lutsinar (Aclar / PVC / Aluminium) mengandungi 14 tablet.
ADENURIC 80 mg boleh didapati dalam pek tablet bersalut filem 14, 28, 42, 56, 84 dan 98.
Tidak semua saiz pek boleh dipasarkan.
06.6 Arahan penggunaan dan pengendalian
Tiada arahan khas.
07.0 PEMEGANG KEBENARAN PEMASARAN
Menarini International Operations Luxembourg S.A.
1, Avenue de la Gare, L-1611 Luxembourg
Luxembourg
08.0 NOMBOR KEBENARAN PEMASARAN
EU / 1/08/447/001
EU / 1/08/447/002
EU / 1/08/447/005
EU / 1/08/447/006
EU / 1/08/447/007
EU / 1/08/447/008
039538018
039538020
09.0 TARIKH KEBENARAN ATAU PEMBAHARUAN KEBENARAN
Tarikh kebenaran pertama: 21 April 2008
Tarikh pembaharuan terkini: 20 Disember 2012
10.0 TARIKH SEMAKAN TEKS
April 2015