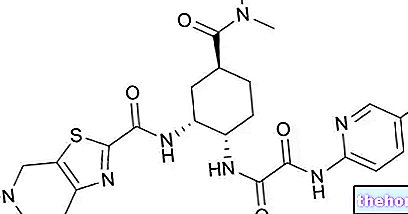
kalsium dan asid anorganik, seperti, asid nitrik, asid hidroklorik atau asid sulfurik. Berikut adalah tindak balas kimia yang melibatkan penggunaan asid terakhir ini:
Ca3 (PO4) 2 + 3 H2SO4 → 3 CaSO4 + 2 H3PO4
Proses termal, sebaliknya, melibatkan mendapatkan anhidrida fosforik bermula dari unsur fosforus. Setelah terbentuk, anhidrida mesti dihidrat sehingga asid ortofosfat diperoleh, seperti yang digambarkan dalam tindak balas berikut:
P2O5 + 3 H2O → 2 H3PO4
Proses terakhir ini secara amnya menghasilkan asid ortofosforik yang lebih murni daripada proses basah.
persekitaran, ia kelihatan sebagai pepejal putih yang mencair pada suhu sekitar 42 ° C.
Walau bagaimanapun, asid fosforik umumnya dipasarkan dalam bentuk larutan berair 85% pekat. Ia adalah penyelesaian yang tidak berwarna, tidak berbau dan tidak mudah menguap, tetapi menghakis dan dengan konsistensi yang agak padat, hampir "sirap".
Selain larut dalam air, asid ortofosfat juga larut dalam etanol. Ia tidak mudah meletup atau mudah terbakar, tetapi kerana hakisannya pada kulit dan membran mukus, ia harus ditangani dengan hati-hati.
untuk menyokong lekatan bahan simenasi untuk kapsul, jambatan, venir, tambalan, dan lain-lain. Dalam konteks ini, asid ortofosforik umumnya digunakan dalam larutan 37%.







.jpg)