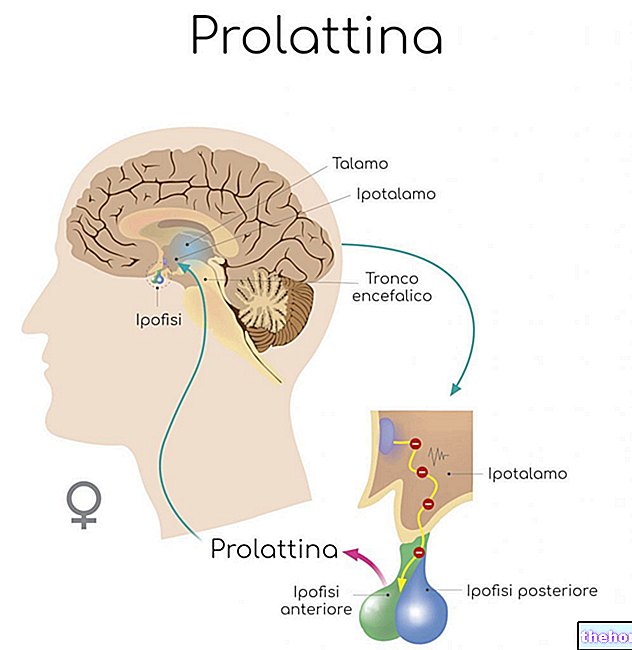
Bahan aktif: Anidulafungin
ECALTA 100 mg serbuk untuk pekat untuk larutan untuk infusi
Petunjuk Mengapa Ecalta digunakan? Untuk apa itu?
ECALTA mengandungi bahan aktif anidulafungin dan digunakan pada orang dewasa untuk merawat sejenis jangkitan kulat darah atau organ dalaman lain yang disebut kandidiasis invasif. Jangkitan disebabkan oleh sel sejenis jamur (ragi) yang disebut Candida.
ECALTA tergolong dalam kumpulan ubat yang dipanggil echinocandins. Ubat ini digunakan untuk merawat jangkitan kulat yang teruk.
ECALTA menghalang perkembangan normal dinding sel kulat. Dengan adanya ECALTA, sel-sel kulat mempunyai dinding sel yang tidak lengkap atau rosak dan ini menjadikannya rapuh atau tidak dapat tumbuh.
Kontraindikasi Apabila Ecalta tidak boleh digunakan
Jangan gunakan ECALTA:
- jika anda alah kepada anidulafungin, echinocandins lain (contohnya CANCIDAS) atau mana-mana ramuan lain dari ubat ini.
Langkah berjaga-jaga untuk penggunaan Apa yang perlu anda ketahui sebelum mengambil Ecalta
Bercakap dengan doktor, ahli farmasi atau jururawat anda sebelum menggunakan ECALTA. Doktor anda mungkin memutuskan untuk memantau
- fungsi hati lebih berhati-hati jika anda mengalami masalah hati semasa rawatan.
- sekiranya anda diberi ubat bius semasa menjalani rawatan dengan ECALTA.
Anak-anak
ECALTA tidak boleh diberikan kepada pesakit yang berumur di bawah 18 tahun.
Interaksi Dadah atau makanan mana yang boleh mengubah kesan Ecalta
Beritahu doktor atau ahli farmasi anda jika anda mengambil, baru-baru ini mengambil atau mungkin mengambil ubat lain.
Jangan mula mengambil ubat lain atau berhenti menggunakannya tanpa kebenaran doktor atau ahli farmasi anda.
Amaran Penting untuk mengetahui bahawa:
Kehamilan dan penyusuan
Kesan ECALTA pada wanita hamil tidak diketahui.Oleh itu, penggunaan ECALTA tidak digalakkan semasa kehamilan. Wanita berpotensi melahirkan anak mesti menggunakan kaedah kontrasepsi yang mencukupi. Segera hubungi doktor anda sekiranya anda hamil semasa dirawat dengan ECALTA.
Kesan ECALTA pada wanita menyusui tidak diketahui. Minta nasihat doktor atau ahli farmasi anda sebelum menggunakannya.
ECALTA semasa menyusu. Minta nasihat doktor atau ahli farmasi anda sebelum mengambil sebarang ubat.
ECALTA mengandungi fruktosa
Ubat ini mengandungi fruktosa (sejenis gula). Sekiranya anda diberitahu oleh doktor bahawa anda mempunyai "intoleransi terhadap beberapa gula, hubungi doktor anda sebelum menggunakan ubat ini.
Dos, Kaedah dan Masa Pentadbiran Cara menggunakan Ecalta: Posologi
ECALTA akan sentiasa disiapkan dan ditadbir oleh doktor atau profesional kesihatan (anda akan mendapat lebih banyak maklumat mengenai kaedah penyediaan ubat ini di akhir risalah pakej di bahagian yang dikhaskan untuk doktor dan profesional penjagaan kesihatan).
Rawatan bermula dengan 200 mg pada hari pertama (dos pemuatan). Ini akan diikuti dengan dos harian 100 mg (dos penyelenggaraan).
ECALTA diberikan kepada anda sekali sehari dengan infus perlahan (titisan) ke dalam urat. Ini memerlukan masa sekurang-kurangnya 1.5 jam untuk dos pemeliharaan dan 3 jam untuk dos pemuatan.
Doktor anda akan menentukan tempoh rawatan dan jumlah ECALTA yang akan anda terima setiap hari dan akan memeriksa tindak balas anda terhadap rawatan dan keadaan anda.
Secara amnya, rawatan harus diteruskan sekurang-kurangnya 14 hari dari hari terakhir Candida dikesan dalam darah.
Sekiranya anda terlupa menggunakan ECALTA
Oleh kerana ubat ini akan diberikan kepada anda di bawah pengawasan perubatan yang ketat, tidak mungkin dos akan terlewat. Walau bagaimanapun, beritahu doktor atau ahli farmasi anda sekiranya anda merasakan dos yang telah dilewatkan.
Anda tidak boleh diberi dos berganda oleh doktor anda.
Sekiranya anda berhenti mengambil ECALTA
Sekiranya doktor anda berhenti mengambil ECALTA semestinya tidak ada kesan.
Doktor anda mungkin menetapkan ubat lain setelah menjalani rawatan dengan ECALTA untuk meneruskan rawatan jangkitan kulat atau untuk mengelakkannya kembali.
Sekiranya simptom asal jangkitan berulang, beritahu doktor atau profesional penjagaan kesihatan yang lain dengan segera.
Sekiranya anda mempunyai pertanyaan lebih lanjut mengenai penggunaan ubat ini, tanyakan kepada doktor, ahli farmasi atau jururawat anda.
Pengumpulan semula
Setiap botol mesti disusun semula dalam keadaan aseptik dengan 30 ml air untuk suntikan untuk mendapatkan kepekatan 3.33 mg / ml. Masa penggantian boleh bertahan sehingga 5 minit. Selepas pencairan seterusnya, larutan mesti dibuang sekiranya kehadiran zarah atau perubahan warna dikenal pasti.
Larutan yang disusun semula dapat disimpan hingga 25 ° C hingga 24 jam sebelum pencairan berikutnya.
Pencairan dan infusi
Kandungan botol yang disusun semula mesti dipindahkan dalam keadaan aseptik ke dalam beg intravena (atau botol) yang mengandungi natrium klorida untuk infus 9 mg / ml (0,9%) atau glukosa untuk infus 50 mg / ml (5%) untuk mendapatkan kepekatan anidulafungin sama dengan 0.77 mg / ml. Jadual di bawah menunjukkan jumlah yang diperlukan untuk setiap dos.
Keperluan pencairan untuk pentadbiran ECALTA
A: Natrium klorida untuk infusi 9 mg / ml (0,9%) atau glukosa untuk infus 50 mg / ml (5%)
B: Kepekatan larutan untuk infusi adalah 0.77 mg / mL. Kadar infusi tidak boleh melebihi 1.1 mg / min (bersamaan dengan 1.4 mL / min apabila disusun semula dan dicairkan seperti yang diperintahkan).
Setiap kali larutan dan bekas dibenarkan, produk perubatan parenteral harus diperiksa secara visual sebelum pemberian untuk mengetahui adanya zarah atau perubahan warna.Jika kehadiran zarah atau perubahan warna dikenal pasti, larutan mesti dibuang.
Untuk kegunaan tunggal sahaja. Ubat yang tidak digunakan dan sisa yang berasal dari ubat ini mesti dibuang sesuai dengan peraturan tempatan.
Overdosis Apa yang perlu dilakukan jika anda mengambil terlalu banyak Ecalta
Sekiranya anda bimbang anda mungkin diberi ECALTA lebih banyak daripada yang sepatutnya, beritahu doktor atau profesional penjagaan kesihatan yang lain dengan segera.
Kesan Sampingan Apakah kesan sampingan Ecalta
Seperti semua ubat, ubat ini boleh menyebabkan kesan sampingan, walaupun tidak semua orang mendapatnya. Sebilangan kesan sampingan ini akan diperhatikan oleh doktor anda semasa dia memantau tindak balas dan keadaan anda.
Reaksi alahan yang mengancam nyawa, termasuk kesukaran bernafas dengan mengi atau memburuknya ruam yang ada sebelumnya, jarang dilaporkan semasa pentadbiran ECALTA.
Kesan sampingan yang serius - beritahu doktor atau profesional penjagaan kesihatan anda yang lain sekiranya anda mengalami salah satu perkara berikut:
- Kejang (sesuai)
- Kemerahan
- Ruam kulit, gatal-gatal
- Kilatan panas
- Urtikaria
- Penguncupan otot saluran udara secara tiba-tiba yang boleh menyebabkan mengi atau batuk
- Kesukaran bernafas
Kesan sampingan yang lain
Kesan sampingan yang sangat biasa (boleh mempengaruhi lebih daripada 1 dari 10 orang) adalah:
- Tahap kalium rendah dalam darah (hipokalaemia)
- Cirit-birit
- Loya
Kesan sampingan yang biasa (boleh mempengaruhi sehingga 1 dari 10 orang) adalah:
- Kejang (sesuai)
- Sakit kepala
- Dia mencuba semula
- Perubahan dalam ujian fungsi hati
- Ruam kulit, gatal-gatal
- Perubahan dalam ujian fungsi buah pinggang
- Perubahan aliran hempedu dari pundi hempedu ke usus (kolestasis)
- Tahap gula darah tinggi
- Tekanan darah tinggi
- Tekanan darah rendah
- Penguncupan otot saluran udara secara tiba-tiba yang boleh menyebabkan mengi atau batuk
- Kesukaran bernafas
Kesan sampingan yang tidak biasa (boleh mempengaruhi sehingga 1 dari 100 orang) adalah:
- Gangguan pembekuan
- Kemerahan
- Kilatan panas
- Sakit perut
- Urtikaria
- Sakit di tempat suntikan
Kesan yang tidak diingini dari frekuensi yang tidak diketahui (frekuensi tidak dapat dianggarkan dari data yang ada) adalah:
- Reaksi alergi yang mengancam nyawa
Melaporkan kesan sampingan
Sekiranya anda mendapat kesan sampingan, berbincanglah dengan doktor, ahli farmasi atau jururawat anda. Ini termasuk kemungkinan kesan sampingan yang tidak disenaraikan dalam risalah ini. Anda juga boleh melaporkan kesan sampingan secara langsung melalui sistem pelaporan nasional V. Dengan melaporkan kesan sampingan, anda boleh membantu. untuk memberikan lebih banyak maklumat mengenai keselamatan ubat ini.
Tamat Tempoh dan Pengekalan
Jauhkan ubat ini dari pandangan dan jangkauan kanak-kanak. Jangan gunakan ubat ini selepas tarikh luput yang tertera pada label. Tarikh luput merujuk pada hari terakhir bulan tersebut.
Simpan di dalam peti sejuk (2 ° C - 8 ° C).
Penyelesaian yang disusun semula dapat disimpan hingga 25 ° C hingga 24 jam. Penyelesaian infus boleh disimpan pada suhu 25 ° C (suhu bilik) hingga 48 jam atau disimpan dalam keadaan beku sekurang-kurangnya 72 jam dan harus diberikan pada suhu 25 ° C (suhu bilik) dalam 48 jam.
Jangan buang ubat-ubatan melalui air buangan atau sampah isi rumah.
Maklumat lain
Apa yang mengandungi ECALTA
Bahan aktifnya adalah anidulafungin. Setiap botol serbuk mengandungi 100 mg anidulafungin
Bahan-bahan lain adalah: fruktosa, manitol, polysorbate 80, asam tartaric, sodium hidroksida (untuk penyesuaian pH), asid hidroklorik (untuk penyesuaian pH).
Seperti apa ECALTA dan kandungan peknya
ECALTA boleh didapati sebagai pek yang mengandungi 1 botol 100 mg serbuk untuk pekat untuk larutan infus.
Serbuk berwarna putih hingga putih.
Risalah Pakej Sumber: AIFA (Badan Perubatan Itali). Kandungan yang diterbitkan pada Januari 2016. Maklumat yang ada mungkin tidak terkini.
Untuk mempunyai akses ke versi paling terkini, disarankan untuk mengakses laman web AIFA (Badan Perubatan Itali). Penafian dan maklumat berguna.
01.0 NAMA PRODUK PERUBATAN
ECALTA 100 MG POWDER FOR CONCENTRATE FOR SOLUTION FOR INFUSION
02.0 KOMPOSISI KUALITATIF DAN KUANTITATIF
Setiap botol mengandungi 100 mg anidulafungin.
Larutan yang disusun semula mengandungi 3.33 mg / ml anidulafungin dan larutan yang dicairkan mengandungi 0.77 mg / ml anidulafungin.
Eksipien dengan kesan yang diketahui: fruktosa 102.5 mg setiap botol.
Untuk senarai lengkap eksipien, lihat bahagian 6.1.
03.0 BORANG FARMASI
Serbuk untuk pekat untuk larutan untuk infusi.
Lyophilisate pepejal putih hingga putih.
Larutan yang disusun semula mempunyai pH 3.5 hingga 5.5.
04.0 MAKLUMAT KLINIKAL
04.1 Petunjuk terapeutik
Rawatan kandidiasis invasif pada pesakit dewasa (lihat bahagian 4.4 dan 5.1).
04.2 Posologi dan kaedah pentadbiran
Rawatan ECALTA harus dimulakan oleh doktor yang berpengalaman dalam rawatan jangkitan kulat invasif. Sampel kultur jamur harus dikumpulkan sebelum permulaan terapi.Terapi dapat dimulakan sebelum hasil ujian kultur diketahui dan dapat disesuaikan dengan sewajarnya apabila hasil ini tersedia.
Dos
Dosis pemuatan 200 mg tunggal harus diberikan pada hari pertama rawatan, diikuti dengan 100 mg sehari selepas itu. Tempoh rawatan harus berdasarkan tindak balas klinikal pesakit. Secara amnya, terapi antijamur harus diteruskan sekurang-kurangnya 14 hari setelah budaya positif terakhir.
Tempoh rawatan
Data tidak mencukupi untuk menyokong penggunaan dos 100 mg untuk tempoh rawatan melebihi 35 hari.
Pesakit dengan gangguan buah pinggang dan hati
Tidak diperlukan penyesuaian dos pada pesakit dengan gangguan hati yang ringan, sederhana atau teruk. Tidak diperlukan penyesuaian dos pada pesakit dengan tahap gangguan buah pinggang, termasuk pesakit yang menjalani dialisis. ECALTA dapat diberikan tanpa mengira bila dialisis dilakukan (lihat bahagian 5.2).
Populasi pesakit khas lain
Tidak diperlukan penyesuaian dos pada pesakit dewasa berdasarkan jantina, berat badan, etnik, positif HIV atau pada pesakit tua (lihat bahagian 5.2).
Populasi kanak-kanak
Keselamatan dan keberkesanan ECALTA pada anak-anak di bawah 18 tahun belum terbukti. Data yang ada saat ini dijelaskan di bahagian 5.2 tetapi tidak mungkin untuk menyimpulkan rejimen yang disyorkan.
Kaedah pentadbiran
Untuk pentadbiran intravena sahaja.
ECALTA mesti disusun semula dengan air untuk suntikan pada kepekatan 3,33 mg / ml dan kemudian diencerkan hingga kepekatan 0,77 mg / ml. Untuk arahan mengenai penggabungan semula produk ubat sebelum pentadbiran, lihat bahagian 6.6.
Dianjurkan agar ECALTA diberikan pada kadar infus yang tidak melebihi 1.1 mg / min (bersamaan dengan 1.4 ml / min apabila serbuk disusun semula dan dicairkan seperti yang diperintahkan). Reaksi berkaitan infusi jarang berlaku apabila kadar infus anidulafungin tidak melebihi 1.1 mg / min (lihat bahagian 4.4).
ECALTA tidak boleh diberikan sebagai bolus.
04.3 Kontraindikasi
Hipersensitiviti terhadap bahan aktif atau salah satu daripada eksipien yang disenaraikan dalam bahagian 6.1.
Hipersensitiviti terhadap ubat lain dari kelas echinocandin.
04.4 Amaran khas dan langkah berjaga-jaga yang sesuai untuk digunakan
ECALTA belum dikaji pada pesakit dengan endokarditis, osteomielitis atau meningitis dari Candida.
Keberkesanan ECALTA hanya dinilai pada sebilangan kecil pesakit neutropenik (lihat bahagian 5.1).
Kesan hepatik
Peningkatan tahap enzim hati telah diperhatikan pada subjek yang sihat dan pada pesakit yang dirawat dengan anidulafungin. Perubahan hati yang signifikan secara klinikal telah berlaku pada beberapa pesakit dengan keadaan perubatan yang serius yang dirawat dengan beberapa produk ubat bersamaan dengan anidulafungin. Episod disfungsi hepatik yang signifikan, hepatitis dan kegagalan hati tidak biasa dalam kajian klinikal. Pesakit dengan peningkatan enzim hati semasa rawatan dengan anidulafungin harus dipantau untuk kemungkinan memburuknya fungsi hati dan menilai keseimbangan risiko-manfaat terapi anidulafungin yang berterusan.
Reaksi anafilaksis
Reaksi anafilaksis, termasuk kejutan, telah dilaporkan semasa penggunaan anidulafungin. Sekiranya reaksi tersebut berlaku, pemberian anidulafungin harus dihentikan dan terapi yang sesuai digunakan.
Reaksi berkaitan infusi
Reaksi buruk yang berkaitan dengan infusi, termasuk ruam, urtikaria, pembilasan, pruritus, dispnea, bronkospasme dan hipotensi, telah dilaporkan semasa rawatan dengan anidulafungin.
Kemerosotan reaksi yang berkaitan dengan infus berikutan pemberian anestetik yang bersamaan diperhatikan dalam kajian bukan klinikal (pada tikus) (lihat bahagian 5.3). Perkaitan klinikal kesan ini tidak diketahui. Walau bagaimanapun, berhati-hati diperlukan apabila anidulafungin diberikan bersama dengan agen anestetik.
Kandungan fruktosa
Pesakit dengan masalah keturunan yang jarang berlaku mengenai intoleransi fruktosa tidak boleh mengambil ubat ini.
04.5 Interaksi dengan produk ubat lain dan bentuk interaksi lain
Anidulafungin bukan substrat, penginduksi atau perencat isoenzim sitokrom P450 yang berkaitan secara klinikal (1A2, 2B6, 2C8, 2C9, 2C19, 2D6, 3A). Penting untuk menunjukkan bahawa kajian dalam vitro mereka tidak menolak kemungkinan adanya interaksi dalam vivo.
Kajian interaksi telah dilakukan dengan anidulafungin dan produk ubat lain yang kemungkinan dapat dilakukan bersama. Tidak disyorkan penyesuaian dos produk ubat ini atau anidulafungin apabila yang terakhir diberikan dengan siklosporin, vorikonazol, dan tacrolimus dan tidak diselaraskan penyesuaian dos anidulafungin apabila diberikan bersama dengan amfoterisin B atau rifampisin.
Populasi kanak-kanak
Kajian interaksi hanya dilakukan pada orang dewasa.
04.6 Kehamilan dan penyusuan
Kehamilan
Tidak ada data yang mencukupi dari penggunaan anidulafungin pada wanita hamil.
Kesan perkembangan ringan diperhatikan pada arnab yang dirawat dengan andidulafungin semasa kehamilan dengan adanya ketoksikan ibu (lihat bahagian 5.3). Potensi risiko untuk manusia tidak diketahui. Oleh itu, penggunaan anidulafungin pada kehamilan tidak digalakkan.
Masa makan
Kajian haiwan menunjukkan bahawa anidulafungin diekskresikan dalam susu ibu. Tidak diketahui sama ada anidulafungin diekskresikan dalam susu ibu. Keputusan mengenai sama ada untuk meneruskan / menghentikan penyusuan atau terapi anidulafungin mesti diambil dengan mengambil kira manfaat penyusuan susu ibu untuk anak dan manfaat rawatan anidulafungin untuk ibu.
Kesuburan
Untuk anidulafungin, tiada kesan terhadap kesuburan dilihat dalam kajian yang dilakukan pada tikus jantan dan betina (lihat bahagian 5.3).
04.7 Kesan keupayaan memandu dan menggunakan mesin
Belum ada kajian mengenai kemampuan memandu dan menggunakan mesin.
04.8 Kesan yang tidak diingini
Ringkasan profil keselamatan
Lima belas ratus enam puluh lima subjek dirawat dengan satu atau beberapa dos anidulafungin intravena dalam ujian klinikal: 1308 pesakit dalam ujian klinikal Tahap 2/3 (923 pesakit dengan kandidiasis invasif / kandidiasis, 355 pesakit dengan kandidiasis oral / esofagus, 30 pesakit dengan invasif aspergillosis) dan 257 pesakit dalam kajian Fasa 1.
Profil keselamatan anidulafungin berdasarkan pada 840 pesakit dengan kandidiasis invasif / kandidiasis yang dirawat dengan dos harian yang disyorkan 100 mg dalam 9 kajian. Pada mulanya, dalam 3 kajian (satu perbandingan lawan fluconazole, dua bukan perbandingan) 204 pesakit diperiksa; jangka masa purata rawatan intravena pada pesakit ini adalah 13.5 hari (antara 1 hingga 38 hari) dan 119 pesakit dirawat dengan anidulafungin selama ≥ 14 hari. Dalam 6 kajian lain (dua perbandingan lawan caspofungin dan empat bukan perbandingan), 636 pesakit diperiksa, termasuk 53 neutropenik dan 131 dengan jangkitan tisu dalam; jangka masa purata rawatan intravena pada pesakit neutropenik dan pesakit dengan jangkitan tisu dalam dalam kajian ini masing-masing 10.0 (jarak 1 hingga 42) dan 14.0 (julat 1 hingga 42) hari. Reaksi buruk umumnya ringan hingga sederhana dan jarang menyebabkan penghentian rawatan.
Reaksi buruk berkaitan infus telah dilaporkan semasa rawatan dengan anidulafungin dalam ujian klinikal, seperti yang diringkaskan dalam Jadual 1, seperti: pembilasan, pembilasan, pruritus, ruam dan urtikaria.
Reaksi buruk berjadual
Jadual di bawah merangkumi tindak balas buruk semua sebab (istilah MedDRA) yang dilihat pada 840 subjek yang dirawat dengan 100 mg anidulafungin dengan kekerapan sepadan sangat biasa (≥ 1/10), biasa (≥ 1/100 hingga
Jadual 1. Jadual Reaksi buruk
* Lihat bahagian 4.4.
Melaporkan tindak balas buruk yang disyaki
Pelaporan tindak balas buruk yang disyaki berlaku setelah kebenaran produk ubat adalah penting kerana memungkinkan pemantauan berterusan terhadap keseimbangan manfaat / risiko produk ubat tersebut. Profesional penjagaan kesihatan diminta untuk melaporkan sebarang reaksi buruk yang disyaki melalui sistem pelaporan nasional. Dalam "Lampiran V .
04.9 Overdosis
Seperti mana-mana overdosis, langkah-langkah sokongan umum yang diperlukan harus digunakan.
Sekiranya berlaku overdosis, reaksi buruk yang disenaraikan dalam bahagian 4.8 mungkin berlaku.
Dalam ujian klinikal, satu dos 400 mg anidulafungin secara tidak sengaja diberikan sebagai dos pemuatan. Tidak ada reaksi buruk yang dilaporkan. Tidak ada ketoksikan yang membatasi dos dalam kajian yang melibatkan 10 sukarelawan yang sihat. Diberikan dos pemuatan 260 mg, diikuti dengan 130 mg setiap hari; 3 daripada 10 subjek melaporkan peningkatan transaminase sementara dan tanpa gejala (≤ 3 x Had Normal Atas (ULN)).
ECALTA tidak dapat dihubungi.
05.0 HARTA FARMAKOLOGI
05.1 Sifat farmakodinamik
Kumpulan farmakoterapeutik: antijamur untuk kegunaan sistemik, antikulat lain untuk penggunaan sistemik.
Kod ATC: JO2AX06.
Mekanisme tindakan
Anidulafungin adalah "echinocandin semi-sintetik, lipopeptida yang disintesis dari produk penapaian"Aspergillus nidulans.
Anidulafungin secara selektif menghalang beta-D-glucan-synthase, enzim yang terdapat pada sel-sel kulat tetapi bukan mamalia. Ini melibatkan "penghambatan pembentukan beta-D-glukan, komponen penting dari dinding sel jamur. Anidulafungin telah menunjukkan" aktiviti fungisida terhadap Candida spp. dan aktiviti "terhadap kawasan pertumbuhan sel aktif hyphae Aspergillus fumigatus.
Aktiviti secara in vitro
Anidulafungin menunjukkan aktiviti " secara in vitro ke arah C. albicans, C. glabrata, C. parapsilosis, C. krusei Dan C. tropis. Untuk kesesuaian klinikal data ini, lihat "Keberkesanan dan keselamatan klinikal" Aspergillus fumigatus.
Isolasi dengan mutasi di kawasan titik panas gen sasaran telah dikaitkan dengan kegagalan klinikal atau jangkitan kulat permulaan baru (penembusan). Rawatan dengan caspofungin terlibat dalam kebanyakan kes klinikal. Walau bagaimanapun, dalam eksperimen haiwan mutasi ini memberikan ketahanan silang terhadap ketiga-tiga echinocandin, sehingga sehingga pengalaman klinikal lebih lanjut diperoleh pada anidulafungin isolat ini diklasifikasikan sebagai tahan terhadap echinocandins.
Aktiviti itu secara in vitro anidulafungin terhadap spesies Candida ia tidak seragam. Khususnya, untuk C. parapsilosis MIC (Kepekatan Inhibitori Minimum) anidulafungin lebih tinggi daripada spesies lain dari Candida. "Jawatankuasa Eropah untuk Uji Kerentanan Antimikroba (EUCAST) telah menentukan teknik piawai untuk ujian kepekaan anidulafungin spesies Candida serta titik penafsiran masing-masing.
Jadual 2. Titik Pecahan EUCAST
1 C. parapsilosis mempunyai "perubahan intrinsik dalam gen sasaran, yang mungkin merupakan mekanisme yang bertanggungjawab untuk MIC yang lebih tinggi daripada spesies lain Candida. Dalam kajian klinikal hasil untuk anidulafungin dengan C. parapsilosis namun, penggunaan echinocandins dalam kandidiemia tidak berbeza secara statistik daripada spesies lain C. parapsilosis ia mungkin tidak dianggap sebagai terapi pilihan pertama
2 EUCAST tidak menentukan titik putus yang tidak berkaitan dengan spesies untuk Anidulafungin
Aktiviti dalam vivo
Anidulafungin yang diberikan secara ibu bapa berkesan terhadap spesies Candida dalam model tetikus dan arnab yang tidak kompeten dan imunokompromis. Rawatan dengan anidulafungin memanjangkan kadar kelangsungan hidup dan juga mengurangkan beban Candida spp. dalam organ yang berkenaan, apabila ditentukan pada selang waktu antara 24 dan 96 jam dari rawatan terakhir.
Jangkitan yang dikaji pada haiwan makmal termasuk jangkitan yang disebarkan C. albicans pada arnab neutropenik, jangkitan oesophageal / oropharyngeal pada arnab neutropenik dengan C. albicans tahan terhadap flukonazol dan tikus neutropenik jangkitan yang disebarkan dengan jangkitan C. glabrata tahan terhadap flukonazol.
Keberkesanan dan keselamatan klinikal
Candidemia dan bentuk Candidiasis Invasif lain
Keselamatan dan keberkesanan anidulafungin dinilai dalam percubaan klinikal yang penting, rawak, double-blind, multicenter, Fasa 3 yang dijalankan di beberapa negara terutamanya pada pesakit non-neutropenik, dengan kandidiemia dan dalam sejumlah kecil pesakit dengan jangkitan mendalam. Candida dilokalisasikan ke tisu atau berkaitan dengan pembentukan abses. Pesakit dengan endokarditis, osteomielitis atau meningitis dari Candida, atau mereka yang mempunyai jangkitan dari C. krusei, dikecualikan secara khusus dari kajian ini. Pesakit secara rawak menerima anidulafungin (200 mg dos pemberian intravena diikuti oleh 100 mg sehari secara intravena) atau flukonazol (800 mg dos pemuatan intravena diikuti oleh 400 mg sehari) dan dikelompokkan dengan skala APACHE II (≤ 20 dan> 20) dan berdasarkan kehadiran atau ketiadaan neutropenia. Rawatan diberikan sekurang-kurangnya 14 hari dan tidak lebih dari 42 hari. Pesakit di kedua lengan rawatan dibenarkan beralih ke flukonazol oral setelah sekurang-kurangnya 10 hari terapi intravena, dengan syarat mereka dapat bertoleransi dengan rawatan oral dan berada dalam usia sekurang-kurangnya 24 jam dan kultur darah yang lebih baru negatif untuk Candida spp.
Pesakit yang telah menerima sekurang-kurangnya satu dos ubat kajian dan yang mempunyai budaya positif untuk Candida spp. dari laman web yang biasanya steril sebelum pendaftaran dimasukkan ke dalam populasi Modified Intent-To-Treat (MITT). Dalam analisis keberkesanan primer (tindak balas keseluruhan pada akhir terapi intravena pada populasi MITT) anidulafungin dibandingkan dengan flukonazol pada pra- perbandingan statistik dua peringkat yang ditentukan (non-inferiority diikuti oleh keunggulan). Tindak balas keseluruhan yang berjaya memerlukan peningkatan klinikal dan pembasmian mikrobiologi. Pesakit ditindaklanjuti selama enam minggu setelah semua terapi selesai.
Dua ratus lima puluh enam pesakit, berusia 16 hingga 91 tahun, secara rawak menjalani rawatan dan menerima sekurang-kurangnya satu dos ubat kajian. Spesies yang paling kerap diasingkan semasa lawatan awal adalah C. albicans (63.8% anidulafungin, 59.3% fluconazole), diikuti oleh C. glabrata (15,7 %, 25,4 %), C. parapsilosis (10.2%, 13.6%) e C. tropis (11.8%, 9.3%) - dengan masing-masing 20, 13 dan 15 strain dari 3 spesies terakhir dalam kumpulan anidulafungin. Sebilangan besar pesakit mempunyai skor APACHE II ≤ 20 dan sebilangan kecil pesakit neutropenik.
Data keberkesanan, baik global dan berkaitan dengan pelbagai subkumpulan, ditunjukkan di bawah dalam Jadual 3.
a Dikira sebagai anidulafungin tolak flukonazol
b Dengan atau tanpa kandidiemia bersamaan
c Intra-perut
d Data disajikan untuk pesakit dengan patogen tunggal pada awal
dan 98.3% selang keyakinan, untuk pelbagai perbandingan yang dibuat pada masa-masa berikutnya melalui analisis post-hoc.
Kadar kematian pada kedua-dua lengan rawatan anidulafungin dan flukonazol ditunjukkan di bawah dalam Jadual 4:
Data tambahan pada pesakit neutropenik
Keberkesanan anidulafungin (200 mg dos intravena diikuti oleh 100 mg sehari secara intravena) pada pesakit neutropenik dewasa (ditentukan dengan jumlah neutrofil mutlak ≤ 500 sel / mm3, WBC ≤ 500 sel / mm3 atau penyiasat yang diklasifikasikan sebagai neutropenik pada awal) dengan kandidiasis invasif yang disahkan secara mikrobiologi dinilai dalam analisis gabungan 5 kajian prospektif (1 perbandingan lawan caspofungin dan 4 terbuka, tidak boleh dibandingkan). Pesakit dirawat sekurang-kurangnya 14 hari. Pada pesakit yang stabil secara klinikal, beralih ke terapi azole oral dibenarkan setelah sekurang-kurangnya 5-10 hari rawatan anidulafungin. Sebanyak 46 pesakit dimasukkan dalam analisis. Sebilangan besar pesakit hanya kandidiemia (84.8%; 39/46). Patogen yang paling kerap diasingkan pada peringkat awal adalah C. tropis (34,8%; 16/46), C. krusei (19,6%; 9/46), C. parapsilosis (17,4%; 8/46), C. albicans (15.2%; 7/46), dan C. glabrata (15.2%; 7/46). Tahap tindak balas kejayaan keseluruhan pada akhir rawatan intravena (titik akhir primer) adalah 26/46 (56.5%) dan pada akhir semua rawatan adalah 24/46 (52.2%). Semua penyebab kematian sehingga akhir kajian (lawatan susulan 6 minggu) adalah 21/46 (45.7%).
Keberkesanan anidulafungin pada pesakit neutropenik dewasa (ditentukan dengan jumlah neutrofil mutlak ≤ 500 sel / mm3 pada awal) dengan kandidiasis invasif dinilai dalam kajian prospektif, terkawal, double-blind, rawak.Pesakit yang layak dirawat dengan anidulafungin (200 mg dos pemuatan intravena diikuti oleh 100 mg sehari secara intravena) atau caspofungin (70 mg dos pemuatan intravena diikuti dengan 50 mg sehari secara intravena.) (2: 1 pengacakan). Pesakit dirawat sekurang-kurangnya 14 hari.
Pada pesakit yang stabil secara klinikal, peralihan terapi azole oral dibenarkan setelah sekurang-kurangnya 10 hari rawatan kajian. Sebanyak 14 pesakit neutropenik dengan kandidiasis invasif mikrobiologi yang disahkan (populasi MITT) (11 anidulafungin, caspofungin) telah mendaftar dalam kajian ini. Sebilangan besar pesakit mempunyai kandidiemia sahaja. Patogen yang paling kerap diasingkan pada peringkat awal adalah C. tropis (4 anidulafungin, 0 caspofungin), C.. parapsilosis (2 anidulafungin, 1 caspofungin), C. krusei (2 anidulafungin, 1 caspofungin) C. ciferrii (2 anidulafungin, 0 caspofungin). Tahap tindak balas yang berjaya secara keseluruhan pada akhir rawatan intravena (titik akhir utama) adalah 8/11 (72.7%) untuk anidulafungin dan 3/3 (100%) untuk caspofungin (perbezaan -27.3, 95% CI: -80.9, 40.3); kadar tindak balas kejayaan keseluruhan pada akhir semua rawatan adalah 8/11 (72.7%) untuk anidulafungin dan 3/100%) untuk caspofungin (perbezaan -27.3, 95% CI: -80, 9, 40.3). Semua penyebab kematian sehingga lawatan susulan 6 minggu untuk anidulafungin (populasi MITT) adalah 4/11 (36.4%), dan 2/3 (66.7%) untuk caspofungin.
Pesakit dengan kandidiasis invasif yang dikonfirmasi secara mikrobiologi (populasi MITT) dan neutropenia dikenal pasti dalam "analisis gabungan dari 4 kajian prospektif yang tidak serupa, terbuka dan berlainan. Keberkesanan anidulafungin (200 mg dos pemuatan per intravena diikuti oleh 100 mg per hari secara intravena) dinilai pada 35 pesakit dewasa neutropenik yang ditentukan dengan jumlah neutrofil mutlak ≤ 500 sel / mm3 atau pada 22 pesakit dengan WBC ≤ 500 sel / mm3 atau pada 13 pesakit yang diklasifikasikan sebagai penyelidik sebagai neutropenik pada peringkat awal. Pesakit dirawat sekurang-kurangnya 14 hari. Pada pesakit yang stabil secara klinikal, beralih ke terapi azole oral dibenarkan setelah sekurang-kurangnya 5-10 hari rawatan anidulafungin. Sebilangan besar pesakit mempunyai kandidiemia sahaja (85.7%). Patogen yang paling kerap diasingkan pada peringkat awal adalah C. tropis (12 pesakit), C. albicans (7 pesakit), C. glabrata (7 pesakit), C. krusei (7 pesakit) e C. parapsilosis (6 pesakit). Tahap tindak balas yang berjaya secara keseluruhan pada akhir rawatan intravena (titik akhir primer) adalah 18/35 (51.4%), dan 16/35 (45.7%) pada akhir semua rawatan. Semua penyebab kematian pada hari ke-28 adalah 10/35 (28.6%). Tahap tindak balas kejayaan keseluruhan pada akhir rawatan intravena dan pada akhir semua rawatan adalah 7/13 (53.8%) untuk kedua-dua daripada 13 pesakit yang diklasifikasikan oleh penyiasat sebagai neutropenik pada awal.
Data tambahan pada pesakit dengan jangkitan tisu dalam
Keberkesanan anidulafungin (200 mg dos pemuatan intravena diikuti oleh 100 mg sehari secara intravena) pada pesakit dewasa dengan kandidiasis tisu dalam yang disahkan secara mikrobiologi dinilai dalam analisis gabungan 5 kajian prospektif dari reka bentuk yang serupa (1 perbandingan dan 4 secara terbuka). Pesakit dirawat sekurang-kurangnya 14 hari. Dalam 4 kajian label terbuka, beralih kepada terapi azole oral dibenarkan setelah sekurang-kurangnya 5-10 hari rawatan anidulafungin. Sebanyak 129 pesakit dimasukkan dalam analisis. Dua puluh satu pesakit (16.3%) mengalami kandidiemia bersamaan. Skor rata-rata APACHE II adalah 14.9 (jarak 2-44). Tempat jangkitan yang paling kerap adalah rongga peritoneal 54.3%, 70/129), saluran hepatobiliari (7.0%, 9/129), rongga pleura (5.4%, 7/129) dan buah pinggang (3.1%, 4/129) Patogen yang paling kerap diasingkan dari tisu dalam pada awal C. albicans (64,3%; 83/129), C. glabrata (31,0%; 40/129), C. tropis (11.6%; 15/129) e C. krusei (5.4%; 7/129). Jadual 5 melaporkan keseluruhan tahap kejayaan pada akhir rawatan intravena (titik akhir primer) dan pada akhir semua rawatan, serta kematian semua penyebab sehingga lawatan susulan selama 6 minggu.
tindak balas kejayaan keseluruhan ditakrifkan sebagai kejayaan klinikal dan mikrobiologi
b EOIVT, Akhir Rawatan Intravena; EOT, Tamat Semua Rawatan
05.2 Sifat farmakokinetik
Ciri umum farmakokinetik
Farmakokinetik anidulafungin dicirikan pada sukarelawan yang sihat, pada populasi khas dan pada pesakit. Kebolehubahan antara subjek rendah diperhatikan dalam pendedahan sistemik (pekali variasi? 25%) keadaan mantap dicapai pada hari pertama setelah dos pemuatan (dua kali dos penyelenggaraan).
Pembahagian
Farmakokinetik anidulafungin dicirikan oleh jangka hayat pengedaran yang cepat (0.5-1 jam) dan isipadu pengedaran 30-50 L, yang serupa dengan jumlah cecair badan.
Anidulafungin terikat secara meluas (> 99%) kepada protein plasma. Tidak ada kajian khusus mengenai penyebaran tisu anidulafungin pada manusia. Oleh itu, tidak ada maklumat mengenai penembusan anidulafungin ke dalam cecair serebrospinal (CSF) dan / atau melalui penghalang darah-otak.
Biotransformasi
Metabolisme hepatik anidulafungin tidak diperhatikan. Anidulafungin bukan substrat yang berkaitan secara klinikal, pemicu atau perencat isoenzim sitokrom P450. Anidulafungin tidak mungkin mempunyai kesan yang relevan secara klinikal terhadap metabolisme ubat yang dimetabolisme oleh isoenzim sitokrom P450.
Anidulafungin diubah melalui degradasi kimia yang perlahan pada suhu fisiologi dan pH menjadi peptida gelung terbuka tanpa aktiviti antijamur. Separuh hayat penurunan secara in vitro anidulafungin dalam keadaan fisiologi adalah sekitar 24 jam. Produk gelung terbuka dalam vivoia kemudiannya ditukar menjadi agen penghancur peptida dan dihilangkan terutamanya oleh perkumuhan hempedu.
Penghapusan
Pelepasan anidulafungin kira-kira 1 l / jam. Anidulafungin mempunyai jangka hayat penghapusan utama sekitar 24 jam yang mencirikan sebahagian besar profil masa kepekatan plasma dan separuh hayat terminal 40-50 jam yang mencirikan fasa penghapusan terminal profil.
Dalam kajian klinikal dos tunggal, radiolabelled (14C) anidulafungin (≥ 88 mg) diberikan kepada sukarelawan yang sihat. Kira-kira 30% daripada dos radioaktif yang diberikan dihilangkan pada najis selama 9 hari dan kurang daripada 10% daripada dos tersebut dipulihkan sebagai ubat yang tidak berubah. . Kepekatan anidulafungin jatuh di bawah had kuantifikasi yang lebih rendah 6 hari selepas pentadbiran. Jumlah radioaktiviti yang diturunkan dari ubat dinyatakan dalam darah, air kencing dan najis 8 minggu selepas pemberian.
Lineariti
Anidulafungin menunjukkan farmakokinetik linier dalam pelbagai dos harian tunggal (15-130 mg).
Populasi pesakit khas
Pesakit dengan jangkitan kulat
Farmakokinetik anidulafungin pada pesakit dengan jangkitan kulat adalah serupa dengan yang diamati pada subjek yang sihat berdasarkan analisis farmakokinetik populasi. Dengan rejimen dos 200/100 mg setiap hari pada kadar infusi 1.1 mg / min, Cmax pada keadaan mantap dan kepekatan palung (Cmin) masing-masing mencapai 7 dan 3 mg / l, dengan min AUC pada keadaan mantap kira-kira 110 mg • j / l.
Berat
Walaupun berat badan dikenal pasti sebagai sumber perubahan dalam analisis farmakokinetik populasi, berat badan mempunyai kepentingan klinikal minimum pada farmakokinetik anidulafungin.
Jantina kekitaan
Kepekatan plasma anidulafungin pada sukarelawan lelaki dan wanita adalah serupa. Dalam kajian yang dilakukan pada pesakit pelbagai dos, pelepasan ubat sedikit lebih cepat (kira-kira 22%) pada lelaki.
Warga emas
Analisis farmakokinetik populasi menunjukkan bahawa pelepasan median sedikit berbeza antara kumpulan orang tua (umur ≥ 65 tahun, median CL = 1,07 l / j) dan kumpulan bukan tua (umur
Perlumbaan
Farmakokinetik anidulafungin serupa pada subjek Kaukasia, Hitam, Asia dan Hispanik.
Positif HIV
Penyesuaian dos tidak diperlukan pada pesakit HIV-positif, tanpa mengira terapi antiretroviral.
Kekurangan hepatik
Anidulafungin tidak dimetabolisme oleh hati. Farmakokinetik anidulafungin diperiksa pada subjek dengan gangguan hati Child-Pugh kelas A, B atau C. Kepekatan anidulafungin tidak meningkat pada subjek dengan tahap gangguan hati.
Walaupun sedikit penurunan AUC diperhatikan pada pesakit dengan gangguan hepatik Gred C Child-Pugh, pengurangan itu berada dalam lingkungan anggaran populasi yang diperhatikan untuk subjek yang sihat.
Kegagalan buah pinggang
Anidulafungin mempunyai pelepasan ginjal yang tidak dapat diabaikan (fungsi ginjal normal. Anidulafungin tidak dapat dialisis dan boleh diberikan tanpa mengira bila dialisis dilakukan.
Pesakit kanak-kanak
Farmakokinetik anidulafungin setelah sekurang-kurangnya 5 dos harian diperiksa pada 24 subjek pediatrik imunokompromi (umur 2-11 tahun) dan remaja (12-17 tahun) dengan neutropenia. The penstabil dicapai pada hari pertama setelah dos pemuatan (dua kali dos penyelenggaraan) dan Cmax dan AUCs di keadaan mantap meningkat secara berkadar dosis. Pendedahan sistemik selepas pemberian dos penyelenggaraan 0,75 mg dan 1,5 mg / kg / hari pada populasi ini setanding dengan yang diperhatikan pada orang dewasa selepas pemberian 50 dan 100 mg / hari masing-masing. Kedua-dua rejimen dos tersebut dapat diterima dengan baik oleh pesakit ini.
05.3 Data keselamatan praklinikal
Dalam kajian selama 3 bulan, bukti ketoksikan hati, termasuk peningkatan enzim dan perubahan morfologi, diperhatikan pada tikus dan monyet yang diberi dos 4-6 kali pendedahan terapi klinikal yang dijangkakan. secara in vitro Dan dalam vivo dengan anidulafungin tidak memberikan bukti potensi genotoksik. Kajian haiwan jangka panjang belum dilakukan untuk menilai potensi karsinogenik anidulafungin.
Pentadbiran anidulafungin pada tikus tidak menunjukkan kesan pada pembiakan, termasuk kesuburan pada lelaki dan wanita.
Anidulafungin melintasi penghalang plasenta pada tikus dan dikesan pada plasma janin.
Kajian mengenai perkembangan embrio-janin dilakukan dengan dosis antara 0,2 dan 2 kali (tikus) dan antara 1 dan 4 kali (arnab) yang dicadangkan dos pemeliharaan terapi 100 mg / hari. Anidulafungin tidak menghasilkan jenis ketoksikan perkembangan berkaitan ubat pada tikus yang diuji pada dos maksimum. Kesan perkembangan yang diperhatikan pada arnab (berat badan yang sedikit berkurang) hanya berlaku pada dos tertinggi yang diuji, dos yang juga menghasilkan ketoksikan ibu.
Kepekatan anidulafungin otak rendah (nisbah otak / plasma kira-kira 0.2) pada tikus dewasa dan neonatal yang tidak dijangkiti setelah satu dos. Walau bagaimanapun, kepekatan otak meningkat pada tikus neonatal yang tidak dijangkiti selepas 5 dos harian (nisbah otak / plasma kira-kira 0.7). Dalam beberapa kajian dos pada arnab dengan kandidiasis yang disebarkan dan pada tikus dengan jangkitan CNS yang disebabkan oleh Candida, anidulafungin mengurangkan beban kulat di otak.
Tikus dirawat dengan tiga dos anidulafungin dan dibius dalam satu jam menggunakan kombinasi ketamin dan xylazine. Tikus dalam kumpulan dos yang lebih tinggi melaporkan reaksi berkaitan infus yang diperburuk oleh anestesia. Beberapa Tikus dalam kumpulan dos perantara melaporkan reaksi yang serupa, tetapi hanya selepas pentadbiran anestesia.
Tidak ada reaksi buruk yang dilaporkan pada haiwan yang dirawat dengan dosis yang lebih rendah dengan adanya atau tidak adanya anestesia dan pada kumpulan dos perantaraan sekiranya tidak ada anestesia, tidak ada reaksi yang berkaitan dengan infus.
06.0 MAKLUMAT FARMASI
06.1 Eksipien
Fruktosa
Mannitol
Polysorbate 80
Asid tartarik
Natrium hidroksida (untuk penyesuaian pH)
Asid hidroklorik (untuk penyesuaian pH)
06.2 Ketidaksesuaian
Produk ubat ini tidak boleh dicampurkan dengan produk lain kecuali yang disebutkan dalam bahagian 6.6.
06.3 Tempoh sah
3 tahun.
Lawatan suhu selama 96 jam hingga 25 ° C dibenarkan, dan serbuk dapat dikembalikan ke keadaan penyimpanan yang disejukkan.
Penyelesaian semula:
Penyelesaian yang disusun semula dapat disimpan hingga 25 ° C hingga 24 jam.
Kestabilan kimia-fizikal larutan yang dibentuk semula telah ditunjukkan selama 24 jam pada suhu 25 ° C.
Dari sudut pandang mikrobiologi, memerhatikan keadaan aseptik yang optimum, larutan yang disusun semula dapat digunakan hingga 24 jam kemudian jika disimpan pada suhu 25 ° C.
Penyelesaian untuk infusi:
Penyelesaian untuk infusi boleh disimpan pada suhu 25 ° C selama 48 jam atau disimpan dalam keadaan beku sekurang-kurangnya 72 jam.
Kestabilan kimia-fizikal larutan infusi yang digunakan telah ditunjukkan selama 48 jam pada 25 ° C.
Dari sudut pandang mikrobiologi, memerhatikan keadaan aseptik yang optimum, larutan infus dapat digunakan selama 48 jam setelah penyediaan jika disimpan pada suhu 25 ° C.
06.4 Langkah berjaga-jaga khas untuk penyimpanan
Simpan di dalam peti sejuk (2 ° C - 8 ° C).
Untuk keadaan penyimpanan selepas penggabungan dan pencairan produk ubat, lihat bahagian 6.3.
06.5 Sifat pembungkusan segera dan kandungan bungkusan
Botol kaca Jenis I 30 ml dengan penyumbat elastomer (getah butil dengan lapisan polimer lengai di permukaan yang bersentuhan dengan produk dan dengan pelincir di permukaan atas untuk memudahkan pengeluaran) dan penutup aluminium dengan penutup flip-off.
Pek 1 botol.
06.6 Arahan penggunaan dan pengendalian
Tiada arahan khas untuk pelupusan.
ECALTA mesti disusun semula dengan air untuk suntikan dan kemudian dicairkan dengan larutan natrium klorida 9 mg / ml (0,9%) untuk suntikan dengan glukosa 50 mg / ml (5%) untuk infus SAHAJA. Keserasian ECALTA yang dibentuk semula dengan bahan intravena, aditif atau produk ubat selain natrium klorida 9 mg / ml (0,9%) atau glukosa 50 mg / ml (5%) belum dapat dipastikan.
Pengumpulan semula
Setiap botol mesti disusun semula dalam keadaan aseptik dengan 30 ml air untuk suntikan untuk mendapatkan kepekatan 3.33 mg / ml. Masa penggantian boleh bertahan sehingga 5 minit. Selepas pencairan berikutnya, larutan tersebut harus dibuang sekiranya kehadiran zarah atau perubahan warna dikenal pasti.
Pencairan dan infusi
Kandungan botol yang disusun semula mesti dipindahkan dalam keadaan aseptik ke dalam beg intravena (atau botol) yang mengandungi natrium klorida untuk infus 9 mg / ml (0,9%) atau glukosa untuk infus 50 mg / ml 5%) sehingga untuk mendapatkan kepekatan anidulafungin sama dengan 0.77 mg / ml. Jadual di bawah menunjukkan jumlah yang diperlukan untuk setiap dos.
Keperluan pencairan untuk pentadbiran ECALTA
Natrium klorida untuk infusi 9 mg / ml (0,9%) atau glukosa untuk infus 50 mg / ml (5%)
B Kepekatan larutan untuk infusi ialah 0.77 mg / ml
Kadar infusi tidak boleh melebihi 1.1 mg / min (bersamaan dengan 1.4 ml / min apabila disusun semula dan dicairkan seperti yang diperintahkan) (lihat bahagian 4.2, 4.4 dan 4.8).
Setiap kali larutan dan bekas dibenarkan, produk perubatan parenteral harus diperiksa secara visual sebelum pemberian untuk mengetahui adanya zarah atau perubahan warna.Jika kehadiran zarah atau perubahan warna dikenal pasti, larutan mesti dibuang.
Ubat yang tidak digunakan dan sisa yang berasal dari ubat ini mesti dibuang sesuai dengan peraturan tempatan
07.0 PEMEGANG KEBENARAN PEMASARAN
Pfizer Terhad
Jalan Ramsgate, Sandwich
Kent, CT13 9NJ, United Kingdom.
08.0 NOMBOR KEBENARAN PEMASARAN
EU / 1/07/416/002
038382026
09.0 TARIKH KEBENARAN ATAU PEMBAHARUAN KEBENARAN
Tarikh kebenaran pertama: 20 September 2007
Tarikh pembaharuan terkini: 23 Ogos 2012
10.0 TARIKH SEMAKAN TEKS
26 Ogos 2014








.jpg)