Trypsin dan chymotrypsin adalah dua enzim utama dalam pencernaan protein makanan. Kedua-duanya dihasilkan dan dirembeskan sebagai zimogen, iaitu dalam bentuk tidak aktif, oleh pankreas; zymogen prekursor trypsin disebut trypsinogen, sementara chymotrypsin disebut chymotrypsinogen.
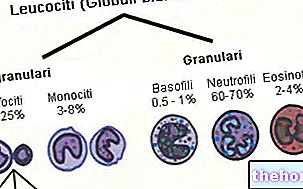
Trypsin dan chymotrypsin tergolong dalam keluarga besar enzim proteolitik (terlibat dalam pencernaan protein) dan subkumpulan endopeptidases. Bahan ini - termasuk pepsin gastrik dan elastase pankreas - menyerang ikatan peptida dalam rantai asid amino, sehingga menimbulkan serpihan molekul yang lebih kecil. Enzim yang tergolong dalam kumpulan kedua, iaitu exopeptidases, menyelesaikan kerja trypsin dan chymotrypsin, melepaskan asid amino tunggal dari hujung rantai peptida; karboksipeptidase pankreas (A1, A2 dan B, yang menyerang hujung karboksil), tetapi juga aminopeptidases (yang menyerang hujung aminoterminal) dan dipeptidase, kedua-duanya dihasilkan dan dirembeskan oleh mukosa usus kecil, tergolong dalam keluarga ini. serupa dengan apa yang telah dilihat untuk trypsin (trypsinogen) dan chymotrypsin (chymotrypsinogen), disekresikan oleh pankreas dalam bentuk tidak aktif. Dalam ketiga-tiga kes tersebut enzim yang terlibat dalam proses pengaktifan enzimatik adalah enteropeptidase, protein yang dihasilkan dan dirembeskan oleh sel mukosa duodenum; lebih khusus lagi, enteropeptidase khusus untuk trypsinogen, yang pernah diubah menjadi trypsin juga mengaktifkan enzim proteolitik lain, termasuk trypsinogen yang sama.
Mari kita ingat secara ringkas bahawa duodenum adalah bahagian pertama usus kecil dan bukan sahaja jus pankreas mengalir ke dalamnya, tetapi juga jus hepatik (hempedu), penting untuk pembetulan pH dan pencernaan lipid.

Perbezaan fungsional antara trypsin dan chymotrypsin hanya menyangkut kekhususannya, iaitu kemampuan untuk mengenali dan memisahkan hanya ikatan yang terbentuk oleh asid amino tertentu. Trypsin bertindak terutamanya pada ikatan peptida yang melibatkan asid amino asas (seperti arginin dan lisin), sementara chymotrypsin terutamanya menghidrolisis ikatan yang melibatkan tirosin, fenilalanin, triptofan, leusin dan metionin.
Terima kasih kepada pelbagai enzim proteolitik, dengan sumbangan keasidan gastrik, protein makanan - awalnya dibentuk oleh beberapa lusin asid amino - dipecah menjadi dipeptida, tripeptida dan asid amino bebas, semua bahan mudah diserap yang berasal dari kapilari mukosa usus diangkut ke hati.
Trypsin dan chymotrypsin di dalam najis
Penentuan chymotrypsin dan trypsin pada tinja digunakan, dan terutama sekali pada masa lalu, sebagai ujian tidak langsung mengenai keupayaan fungsional pankreas eksokrin. Sekiranya sesuatu pada tahap kelenjar ini tidak berfungsi dengan baik, adalah logik untuk mengharapkan penurunan sintesis trypsin dan chymotrypsin, yang juga kekurangan najis. Ujian ini mempunyai kepekaan yang baik, tetapi dibebani dengan risiko sebenar positif palsu dan negatif palsu. Penggunaan julap, misalnya, mengurangkan kepekatan enzim dalam bahan tinja, sementara pengambilan ekstrak pencernaan pankreas (seperti pankreatin) atau sayur-sayuran (seperti tangkai nanas, pepaya, papain dan bromelain) menyebabkan hasil negatif palsu. flora usus juga sedikit sebanyak mempengaruhi jumlah trypsin dan chymotrypsin yang tidak berubah di dalam najis; kerana alasan ini penggunaan antibiotik dapat menghasilkan negatif palsu; sebaliknya, dengan adanya divertikulosis dan keadaan lain yang memihak kepada pembiakan bakteria, hasil positif palsu dapat direkodkan.
Aplikasi klasik pengujian trypsin dan chymotrypsin dalam najis adalah pengesanan kekurangan pankreas pada pesakit dengan fibrosis sista. Salah satu akibat penyakit ini adalah penurunan pengangkutan normal trypsin dan enzim pencernaan lain dari pankreas. Ke duodenum atas sebab ini, semasa kelahiran, najis kanak-kanak dengan fibrosis kistik sangat padat, sehingga menyebabkan penyumbatan usus. Akibatnya, terdapat sejumlah kecil chymotrypsin dan trypsin dalam mekonium.