Struktur dan fungsi
Hemoglobin adalah metalloprotein yang terkandung dalam sel darah merah, yang bertanggungjawab untuk mengangkut oksigen dalam aliran darah. Sebenarnya, oksigen hanya larut dalam air secara sederhana; oleh itu, kuantiti yang larut dalam darah (kurang daripada 2% daripada jumlah keseluruhan) tidak mencukupi untuk memenuhi permintaan metabolik tisu. Oleh itu, keperluan untuk pembawa tertentu jelas.
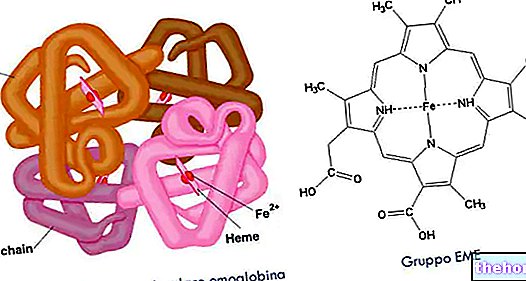
Dalam aliran darah, oksigen tidak dapat mengikat protein secara langsung dan terbalik, seperti yang berlaku untuk logam seperti tembaga dan besi. Tidak menghairankan, di tengah-tengah setiap subunit protein hemoglobin, dibungkus dalam cangkang protein, kita dapati apa yang disebut prostetik kumpulan EME, dengan hati yang logam diwakili oleh atom besi dalam Fe2 + keadaan pengoksidaan (negeri dikurangkan), yang mengikat oksigen dengan cara yang boleh balik.
Analisis darah
- Nilai hemoglobin normal dalam darah: 13-17 g / 100 ml
Pada wanita nilainya rata-rata 5-10% lebih rendah daripada pada lelaki.
Kemungkinan Penyebab Hemoglobin Tinggi
- Polycythemias
- Tempat tinggal yang panjang di tanah tinggi
- Penyakit paru-paru kronik
- Penyakit jantung
- Doping darah (penggunaan eritropoietin dan derivatif atau bahan yang meniru tindakannya)
Kemungkinan Penyebab Hemoglobin Rendah
- Anemia
- Kekurangan zat besi (kekurangan zat besi)
- Pendarahan yang banyak
- Karsinoma
- Kehamilan
- Thalassemias
- Melecur
Oleh itu, kandungan oksigen dalam darah diberikan oleh penjumlahan kuantiti kecil yang dilarutkan dalam plasma dengan pecahan terikat pada besi hemoglobin.
Lebih dari 98% oksigen yang ada dalam darah terikat ke hemoglobin, yang pada gilirannya beredar di aliran darah yang dialokasikan dalam sel darah merah. Oleh itu, tanpa hemoglobin, eritrosit tidak dapat menjalankan tugasnya sebagai pengangkut oksigen dalam darah.
Memandangkan peranan utama logam ini, sintesis hemoglobin memerlukan pengambilan zat besi yang mencukupi dalam diet. Kira-kira 70% zat besi yang terdapat di dalam badan sebenarnya terkandung dalam kumpulan hemoglobin heme.
Hemoglobin terdiri daripada 4 subunit yang secara strukturnya serupa dengan myoglobin *.
* Sementara, hemoglobin mengangkut oksigen dari paru-paru ke tisu, myoglobin membawa oksigen yang dikeluarkan oleh hemoglobin ke dalam pelbagai organel sel yang menggunakannya (misalnya mitokondria).

Hemoglobin adalah metalloprotein besar dan kompleks, yang dicirikan oleh empat rantai protein globular yang masing-masing melilit kumpulan heme yang mengandungi Fe2 +.
Oleh itu, untuk setiap molekul hemoglobin kita dapati empat kumpulan heme yang terbungkus dalam rantai protein globular relatif. Oleh kerana terdapat empat atom besi dalam setiap molekul hemoglobin, setiap molekul hemoglobin dapat mengikat empat atom oksigen pada dirinya sendiri, menurut reaksi yang dapat diterbalikkan:
Hb + 4O2 ← → Hb (O2) 4
Seperti diketahui oleh kebanyakan orang, tugas hemoglobin adalah mengambil oksigen di paru-paru, melepaskannya ke sel yang memerlukannya, mengambil karbon dioksida dari mereka dan melepaskannya ke paru-paru di mana chilo bermula lagi.
Semasa perjalanan darah di kapilari alveoli pulmonari, hemoglobin mengikat oksigen ke dirinya sendiri, yang kemudiannya melepaskan ke tisu dalam peredaran periferal. Pertukaran ini berlaku kerana ikatan oksigen dengan zat besi kumpulan EME mudah berubah dan sensitif terhadap banyak faktor, yang paling penting ialah ketegangan atau tekanan separa oksigen.
Pengikatan oksigen ke hemoglobin dan kesan Bohr
Di paru-paru, ketegangan oksigen plasma meningkat kerana penyebaran gas dari alveoli ke darah (↑ PO2); peningkatan ini menyebabkan hemoglobin mengikat oksigen dengan kuat; sebaliknya berlaku pada tisu periferal, di mana kepekatan oksigen terlarut dalam darah menurun (↓ PO2) dan tekanan separa karbon dioksida meningkat (↑ CO2); ini mendorong hemoglobin untuk melepaskan oksigen dan dikenakan CO2. Menyederhanakan konsep sebanyak mungkin, semakin banyak karbon dioksida yang terdapat dalam darah, semakin sedikit oksigen yang terikat pada hemoglobin.
Walaupun jumlah oksigen yang dilarutkan secara fizikal dalam darah sangat rendah, oleh itu ia memainkan peranan penting. Sebenarnya, kuantiti ini sangat mempengaruhi kekuatan ikatan antara oksigen dan hemoglobin (serta mewakili "nilai rujukan penting dalam mengatur pengudaraan paru).
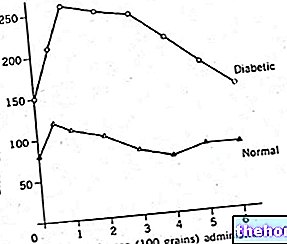
Meringkaskan segala-galanya dengan grafik, jumlah oksigen yang dihubungkan dengan hemoglobin tumbuh sehubungan dengan pO2 mengikuti lengkung sigmoid:

Fakta bahawa kawasan dataran tinggi begitu besar meletakkan margin keselamatan penting pada ketepuan maksimum hemoglobin semasa perjalanan ke paru-paru. Walaupun pO2 pada tahap alveolar biasanya sama dengan 100 mm Hg, memerhatikan angka yang kita perhatikan sebenarnya bagaimana walaupun tekanan separa oksigen sama dengan 70 mmHg (kejadian biasa pada beberapa penyakit atau tinggal di ketinggian tinggi), peratusan hemoglobin tepu tetap hampir dengan 100%.
Di kawasan cerun maksimum, apabila ketegangan separa oksigen turun di bawah 40 mmHg, kemampuan hemoglobin untuk mengikat oksigen turun secara tiba-tiba.
Dalam keadaan rehat, PO2 dalam cecair intraselular adalah kira-kira 40 mmHg; di lokasi ini, kerana undang-undang gas, oksigen yang larut dalam plasma meresap ke arah tisu O2 yang lebih lemah, melintasi membran kapilari. Akibatnya, ketegangan plasma O2 menurun lebih jauh dan ini mendorong pembebasan oksigen dari hemoglobin. . Semasa aktiviti fizikal yang sengit, sebaliknya, ketegangan oksigen dalam tisu turun menjadi 15 mmHg atau kurang, akibatnya darahnya kekurangan oksigen.
Untuk apa yang telah dikatakan, dalam keadaan rehat, sejumlah besar hemoglobin beroksigen meninggalkan tisu, tetap tersedia sekiranya diperlukan (misalnya untuk menangani peningkatan metabolisme secara tiba-tiba di beberapa sel).
Garis pepejal yang ditunjukkan dalam gambar di atas disebut keluk pemisahan hemoglobin; biasanya ditentukan secara in vitro pada pH 7.4 dan pada suhu 37 ° C.
Kesan Bohr mempunyai akibat baik pada pengambilan O2 pada tahap paru-paru dan pelepasannya pada tahap tisu.
Apabila terdapat lebih banyak karbon dioksida terlarut dalam bentuk bikarbonat, hemoglobin membebaskan oksigen dengan lebih mudah dan dibebankan dengan karbon dioksida (dalam bentuk bikarbonat).

Kesan yang sama diperoleh dengan mengasidkan darah: semakin banyak pH darah menurun dan semakin sedikit oksigen tetap terikat pada hemoglobin; tidak menghairankan, dalam darah karbon dioksida larut terutama dalam bentuk asid karbonik, yang terurai.



Sebagai penghormatan kepada penemu, kesan pH atau karbon dioksida pada pemisahan oksigen dikenali sebagai kesan Bohr.
Seperti yang dijangkakan, dalam lingkungan asam, hemoglobin melepaskan oksigen dengan lebih mudah, sementara dalam lingkungan asas ikatan dengan oksigen lebih kuat.

Faktor lain yang mampu mengubah pertalian hemoglobin untuk oksigen termasuk suhu. Khususnya, pertalian hemoglobin untuk oksigen berkurang dengan peningkatan suhu badan. Ini sangat menguntungkan pada musim sejuk dan bulan musim bunga, kerana suhu darah paru (bersentuhan dengan udara persekitaran luaran) lebih rendah daripada yang dicapai dalam tisu, oleh itu pelepasan oksigen difasilitasi.

2.3 diphosphoglycerate adalah perantara dalam glikolisis yang mempengaruhi pertalian hemoglobin dengan oksigen. Sekiranya kepekatannya dalam sel darah merah meningkat, pertalian hemoglobin untuk oksigen menurun, sehingga memudahkan pembebasan oksigen ke tisu. Tidak menghairankan, kepekatan eritrosit sebanyak 2,3 peningkatan diphosphoglycerate, misalnya, dalam anemia, kekurangan kardio-paru dan semasa tinggal di ketinggian tinggi.
Secara amnya, kesan 2,3 bifosfogliserat agak lambat, terutamanya jika dibandingkan dengan tindak balas yang cepat terhadap perubahan pH, suhu dan tekanan separa karbon dioksida.

Kesan Bohr sangat penting semasa kerja otot yang sengit; dalam keadaan seperti itu, pada tisu yang paling terdedah kepada tekanan terdapat peningkatan suhu dan tekanan karbon dioksida tempatan, oleh itu dalam keasidan darah. Seperti yang dijelaskan di atas, semua ini mendorong pelepasan oksigen ke tisu, menggeser kurva pemisahan hemoglobin ke kanan.