Bahan aktif: Bimatoprost
LUMIGAN 0.1 mg / ml titisan mata, larutan
Sisipan pakej Lumigan tersedia untuk saiz pek:- LUMIGAN 0.1 mg / ml titisan mata, larutan
- LUMIGAN 0.3 mg / ml titisan mata, larutan
Mengapa Lumigan digunakan? Untuk apa itu?
LUMIGAN adalah ubat antiglaucoma. Ia tergolong dalam kategori ubat yang disebut prostamides.
Titisan mata LUMIGAN digunakan untuk mengurangkan tekanan mata yang tinggi. Ubat ini boleh digunakan sendiri atau bersama dengan titisan mata lain yang disebut beta-blocker, yang juga berfungsi untuk mengurangkan tekanan pada mata.
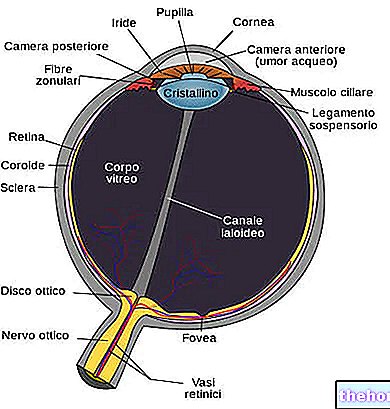
Mata mengandungi cecair berasaskan air yang jernih yang menyuburkan bahagian dalamnya. Cecair ini terus dikeluarkan dari mata dan cecair baru dihasilkan untuk menggantikan yang hilang. Sekiranya cecair tidak dibersihkan dengan cepat, tekanan di dalam mata akan meningkat. Ubat ini berfungsi untuk meningkatkan jumlah cecair yang dikeluarkan, sehingga mengurangkan tekanan pada mata. Tekanan mata yang meningkat, jika tidak dikurangi, dapat menyebabkan penyakit yang disebut glaukoma dan akhirnya dapat menyebabkan kerusakan penglihatan.
Kontraindikasi Apabila Lumigan tidak boleh digunakan
Jangan gunakan LUMIGAN 0.1 mg / ml
- jika anda alah (hipersensitif) terhadap bimatoprost atau bahan LUMIGAN lain.
- jika anda terpaksa berhenti menggunakan titisan mata pada masa lalu kerana kesan yang tidak diingini dari pengawet benzalkonium klorida.
Langkah berjaga-jaga untuk penggunaan Apa yang perlu anda ketahui sebelum anda mengambil Lumigan
Bercakap dengan doktor atau ahli farmasi anda sebelum menggunakan LUMIGAN 0.1 mg / ml.
Rujuk doktor anda sekiranya:
- mengalami masalah pernafasan
- mempunyai masalah hati atau buah pinggang
- telah dikendalikan untuk katarak pada masa lalu
- menderita mata kering
- mempunyai atau mempunyai masalah dengan kornea (bahagian depan mata yang jelas)
- pakai kanta lekap (lihat "Maklumat penting mengenai beberapa ramuan LUMIGAN 0.1 mg / ml")
- pernah atau pernah menderita hipotensi atau bradikardia
- mengalami "jangkitan virus atau" radang mata.
LUMIGAN boleh menyebabkan kegelapan dan memanjangkan bulu mata, juga dapat menggelapkan kelopak mata. Lama kelamaan, warna iris juga menjadi gelap. Perubahan ini dapat kekal dan lebih ketara jika hanya satu mata yang dirawat.
Kanak-kanak dan remaja
LUMIGAN belum diuji pada pesakit di bawah usia 18 tahun oleh itu ia tidak boleh digunakan pada pesakit di bawah usia 18 tahun.
Interaksi Dadah atau makanan mana yang boleh mengubah kesan Lumigan
Beritahu doktor atau ahli farmasi anda jika anda mengambil, baru-baru ini mengambil atau mungkin mengambil ubat lain.
Amaran Penting untuk mengetahui bahawa:
Kehamilan dan penyusuan
Sekiranya anda hamil atau menyusu, fikir anda mungkin mengandung atau merancang untuk mempunyai bayi, minta nasihat doktor atau ahli farmasi anda sebelum mengambil ubat ini.
LUMIGAN boleh masuk ke dalam susu ibu, oleh itu disarankan untuk tidak menyusu semasa menjalani rawatan dengan LUMIGAN.
Memandu dan menggunakan mesin
Selepas pentadbiran LUMIGAN, mungkin terdapat sedikit pengaburan visual sementara.
Dalam kes ini, jangan memandu atau mengendalikan mesin sehingga penglihatan anda kembali jelas.
Maklumat penting mengenai sebilangan ramuan LUMIGAN 0.1 mg / ml
Jangan gunakan titisan semasa memakai kanta lekap. Setelah memberikan titisan mata, tunggu 15 minit sebelum memasukkan kembali kanta lekap anda. Bahan pengawet dalam LUMIGAN, yang disebut benzalkonium klorida, boleh menyebabkan kerengsaan mata dan boleh menghilangkan lensa kontak lembut.
Dos dan kaedah penggunaan Cara menggunakan Lumigan: Dos
Sentiasa gunakan ubat ini sama seperti yang diberitahu oleh doktor atau ahli farmasi anda. Sekiranya ragu-ragu, berjumpa dengan doktor atau ahli farmasi anda.
LUMIGAN hanya boleh digunakan pada mata. Dos yang disyorkan adalah satu tetes LUMIGAN sekali sehari, pada waktu petang, di setiap mata yang akan dirawat.
Sekiranya anda menggunakan LUMIGAN dengan ubat mata yang lain, sapukan titisan mata LUMIGAN terlebih dahulu dan tunggu 5 minit sebelum menggunakan ubat mata kedua.
Jangan menggunakannya lebih dari sekali sehari, kerana keberkesanan rawatan dapat dikurangkan.
Arahan Penggunaan:
Jangan gunakan botol jika cap jaminan pada penutup tidak utuh sebelum digunakan.
- Cuci tangan anda. Anda meletakkan kepala anda ke belakang dan melihat ke atas.
- Tarik perlahan penutup bawah anda ke bawah untuk membentuk poket kecil.
- Putar botol terbalik dan berikan tekanan lembut untuk melepaskan satu tetes tetes mata untuk setiap mata yang dirawat.
- Lepaskan penutup bawah dan tutup mata selama 30 saat.
Hapuskan apa-apa lebihan yang mengalir di pipi anda.
Sekiranya titisan tidak memasuki mata, ulangi operasi.
Untuk mengelakkan jangkitan dan kecederaan pada mata, hujung botol tidak boleh menyentuh mata atau bersentuhan dengan permukaan lain. Setelah menggunakan botol, tutup rapat dengan mengetatkan penutupnya kembali.
Sekiranya anda terlupa menggunakan LUMIGAN 0.1 mg / ml
Sekiranya anda lupa menggunakan LUMIGAN, secepat yang anda ingat, masukkan satu tetes dan kemudian kembali ke masa dos biasa anda. Jangan mengambil dos berganda untuk menebus dos yang dilupakan.
Sekiranya anda berhenti mengambil LUMIGAN 0.1 mg / ml
Agar ia berfungsi dengan betul, LUMIGAN mesti digunakan setiap hari. Sekiranya anda berhenti menggunakan LUMIGAN, tekanan mata anda mungkin meningkat, jadi anda harus berbincang dengan doktor anda sebelum menghentikan rawatan ini.
Sekiranya anda mempunyai pertanyaan lebih lanjut mengenai penggunaan ubat ini, tanyakan kepada doktor atau ahli farmasi anda.
Overdosis Apa yang perlu dilakukan jika anda mengambil Lumigan terlalu banyak
Sekiranya anda menggunakan lebih banyak LUMIGAN daripada yang sepatutnya, ini tidak mungkin menyebabkan akibat yang serius. Berikan dos seterusnya pada waktu biasa. Sekiranya ini membimbangkan anda, berjumpa dengan doktor atau ahli farmasi anda.
Kesan Sampingan Apakah kesan sampingan Lumigan
Seperti semua ubat, ubat ini boleh menyebabkan kesan sampingan, walaupun tidak semua orang mendapatnya.
Sekiranya anda mendapat kesan sampingan, berbincanglah dengan doktor atau ahli farmasi anda. Ini termasuk kemungkinan kesan sampingan yang tidak disenaraikan dalam risalah ini.
Kesan sampingan yang sangat biasa
Kesan ini boleh berlaku pada 1 atau lebih pada 10 pesakit.
Kesan pada mata
- Kemerahan sedikit (sehingga 29% orang)
Kesan sampingan yang biasa
Kesan ini boleh berlaku pada 1 hingga 9 daripada 100 pesakit.
Kesan pada mata
- Ulser kecil di permukaan mata, dengan atau tanpa keradangan
- Kerengsaan
- Mata gatal
- Sambungan bulu mata
- Kerengsaan semasa memberikan titisan pada mata
- Sakit mata
Kesan yang tidak diingini pada kulit
- Kelopak mata gatal merah
- Mencerah kulit di sekitar mata
- Pertumbuhan rambut di sekitar mata
Kesan sampingan yang tidak biasa
Kesan ini boleh berlaku pada 1 hingga 9 daripada 1,000 pesakit.
Dengan perbelanjaan mata
- Menggelapkan warna iris
- Mata letih
- Bengkak pada permukaan mata
- Penglihatan kabur
- Kehilangan bulu mata
Dengan mengorbankan kulit
- Kekeringan
- Kerak di tepi kelopak mata
- Bengkak kelopak mata
- Gatal Menjejaskan badan
- Sakit kepala
- Merasa tidak sihat
Kesan sampingan yang kekerapannya tidak diketahui
Dengan perbelanjaan mata
- Edema makula (pembengkakan retina di bahagian belakang mata yang boleh menyebabkan penglihatan memburuk)
- Mengelap kelopak mata
- Mata terbenam
- Mata kering Terjejas oleh badan
- Asma
- Memburukkan lagi asma
- Memburukkan lagi penyakit paru-paru yang disebut penyakit paru obstruktif kronik (COPD)
- Sesak nafas
- Gejala tindak balas alahan (bengkak, mata merah dan ruam)
Sebagai tambahan kepada kesan sampingan LUMIGAN 0.1 mg / ml, kesan sampingan berikut telah diperhatikan dengan ubat lain yang mengandungi kepekatan bimatoprost yang lebih tinggi (0.3 mg / ml):
- Pening
- Pembakaran okular
- Reaksi alahan pada mata
- Kelopak mata yang meradang
- Kesukaran melihat gambar yang tajam
- Melemahkan penglihatan
- Bengkak pada lapisan lutsinar yang menutupi permukaan mata
- Sensasi badan asing di mata
- Kepekaan terhadap cahaya
- Merobek
- Mata melekit
- Bulu mata yang lebih gelap
- Pendarahan retina
- Keradangan di dalam mata
- Edema makular sista (pembengkakan retina di dalam mata yang menyebabkan penglihatan bertambah buruk)
- Kekejangan kelopak mata
- Mengecilkan kelopak mata, menjauh dari permukaan mata
- Kemerahan kulit di sekitar mata
- Nilai tekanan darah meningkat
- Kelemahan
- Peningkatan nilai fungsi hati dalam ujian darah
Kesan sampingan lain dilaporkan dengan titisan mata yang mengandungi fosfat.
Dalam kes-kes yang sangat jarang berlaku, sebilangan pesakit dengan kerosakan teruk pada lapisan depan mata yang jelas (kornea) telah mengembangkan kawasan legap di kornea kerana penambahan kalsium semasa rawatan.
Melaporkan kesan sampingan
Sekiranya anda mendapat kesan sampingan, berbincanglah dengan doktor atau ahli farmasi anda. Ini termasuk kemungkinan kesan sampingan yang tidak disenaraikan dalam risalah ini. Anda juga boleh melaporkan kesan sampingan secara langsung melalui sistem pelaporan nasional yang disenaraikan dalam Lampiran V. Dengan melaporkan kesan sampingan, anda dapat membantu memberikan lebih banyak maklumat mengenai keselamatan ubat ini.
Tamat Tempoh dan Pengekalan
Jauhkan ubat ini dari pandangan dan jangkauan kanak-kanak.
Jangan gunakan ubat ini selepas tarikh luput yang tertera pada label botol dan kadbod selepas TAMAT. Tarikh luput merujuk pada hari terakhir bulan tersebut.
Buang botol selewat-lewatnya 4 minggu setelah pembukaan pertama, walaupun ia masih mengandungi beberapa tetes. Ini akan mengelakkan jangkitan. Untuk membantu anda mengingati, tulis tarikh pertama kali dibuka di ruang yang terdapat di kotak.
Jangan buang ubat melalui air buangan atau sampah rumah. Tanya ahli farmasi anda bagaimana membuang ubat yang tidak lagi anda gunakan. Ini akan membantu melindungi alam sekitar.
Tarikh Akhir "> Maklumat lain
Apa yang mengandungi LUMIGAN 0.1 mg / ml
- Bahan aktif adalah bimatoprost. Satu ml larutan mengandungi 0.1 mg bimatoprost.
- Bahan-bahan lain adalah benzalkonium klorida (pengawet), natrium klorida, natrium fosfat asas heptahidrat, asid sitrik monohidrat dan air yang disucikan. Sebilangan kecil asid hidroklorik atau natrium hidroksida dapat ditambahkan untuk mengekalkan tahap keasidan (pH) normal.
Keterangan tentang rupa LUMIGAN 0.1 mg / ml dan kandungan peknya
LUMIGAN adalah titisan mata yang jernih dan tidak berwarna, dibekalkan dalam pek yang mengandungi 1 botol plastik atau 3 botol plastik, masing-masing dengan penutup skru.
Setiap botol kira-kira separuh penuh dan mengandungi 3 mililiter larutan, cukup untuk penggunaan selama 4 minggu.
Tidak semua saiz pek boleh dipasarkan.
Risalah Pakej Sumber: AIFA (Badan Perubatan Itali). Kandungan yang diterbitkan pada Januari 2016. Maklumat yang ada mungkin tidak terkini.
Untuk mempunyai akses ke versi paling terkini, disarankan untuk mengakses laman web AIFA (Badan Perubatan Itali). Penafian dan maklumat berguna.
01.0 NAMA PRODUK PERUBATAN -
LUMIGAN 0.1 MG / ML MATA DROPS, PENYELESAIAN
02.0 KOMPOSISI KUALITATIF DAN KUANTITATIF -
1 ml larutan mengandungi 0.1 mg bimatoprost.
Eksipien dengan kesan yang diketahui:
Satu ml larutan mengandungi 0.2 mg benzalkonium klorida.
Untuk senarai lengkap eksipien, lihat bahagian 6.1.
03.0 BORANG FARMASI -
Titisan mata, penyelesaian.
Penyelesaian tidak berwarna.
04.0 MAKLUMAT KLINIKAL -
04.1 Petunjuk terapeutik -
Pengurangan tekanan intraokular yang meningkat pada glaukoma sudut terbuka kronik dan hipertensi okular pada orang dewasa (sebagai monoterapi atau sebagai terapi tambahan kepada beta-blocker).
04.2 Posologi dan kaedah pentadbiran -
Dos
Dos yang disyorkan adalah satu tetes pada mata yang terkena, sekali sehari, diberikan pada waktu petang. Dos tidak boleh melebihi satu kali penggunaan harian, kerana penggunaan yang lebih kerap dapat mengurangkan kesan hipotensi pada tekanan darah.
Populasi kanak-kanak
Keselamatan dan keberkesanan LUMIGAN pada kanak-kanak berumur 0 hingga 18 tahun belum dapat dipastikan.
Pesakit dengan disfungsi hepatik dan buah pinggang:
LUMIGAN belum dikaji pada pesakit dengan disfungsi ginjal, atau disfungsi hati hingga sederhana hingga teruk, oleh itu ia harus digunakan dengan berhati-hati pada pesakit ini. Pada pesakit dengan riwayat gangguan hepatik ringan atau alanine aminotransferase (ALT), aspartate aminotransferase (AST) dan / atau bilirubin tidak normal pada awal terapi, tetes mata bimatoprost 0.3 mg / ml, penyelesaian tidak mempunyai kesan buruk pada fungsi hati pada 24 bulan rawatan.
Kaedah pentadbiran
Sekiranya banyak ubat oftalmik topikal digunakan, setiap ubat harus diberikan sekurang-kurangnya 5 minit.
04.3 Kontraindikasi -
Hipersensitiviti terhadap bahan aktif atau salah satu daripada eksipien yang disenaraikan dalam bahagian 6.1.
LUMIGAN 0.1 mg / ml dikontraindikasikan pada pesakit yang sebelumnya mempunyai reaksi buruk yang disyaki terhadap benzalkonium klorida yang mengakibatkan penghentian terapi.
04.4 Amaran khas dan langkah berjaga-jaga yang sesuai untuk digunakan -
Cermin mata
Sebelum memulakan rawatan, pesakit harus diberitahu tentang kemungkinan memanjangkan bulu mata, kelopak mata menjadi gelap dan peningkatan pigmentasi iris, kerana reaksi ini telah dikesan semasa rawatan dengan LUMIGAN. Sebilangan perubahan ini dapat kekal dan dapat menyebabkan perbezaan penampilan antara kedua mata ketika hanya satu mata yang dirawat. Peningkatan pigmentasi iris cenderung kekal. Perubahan pigmentasi disebabkan oleh peningkatan kandungan melanin dalam melanosit daripada peningkatan jumlah melanosit. Kesan jangka panjang peningkatan pigmentasi iris tidak diketahui. Perubahan warna iris yang dilihat berikutan penggunaan bimatoprost oftalmik mungkin tidak dapat dilihat selama beberapa bulan atau tahun. Pigmentasi coklat di sekitar murid biasanya mengembang secara sepusat ke pinggiran iris dan seluruh atau bahagian mata. Iris memperoleh warna coklat. Nampaknya rawatan tidak memberi kesan pada nevi atau areolae iris. Pada 12 bulan, kejadian hiperpigmentasi iris dengan bimatoprost 0.1 mg / ml tetes mata, larutan adalah 0.5%. Pada 12 bulan, kejadian tetes mata bimatoprost 0.3 mg / ml, larutan adalah 1, 5% (lihat bahagian 4.8, Jadual 2) dan tidak meningkat dalam 3 tahun ke depan rawatan Sifat semula jadi pigmentasi tisu periorbital telah dilaporkan pada beberapa pesakit.
Edema makular sistoid dilaporkan tidak jarang (≥1 / 1.000, edema makula (misalnya pesakit aphakic, pseudophakic dengan kapsul lensa posterior).
Terdapat laporan spontan berulang mengenai pengaktifan semula penyusupan kornea sebelumnya atau jangkitan okular dengan larutan mata bimatoprost 0.3 mg / ml, penyelesaian. LUMIGAN harus digunakan dengan berhati-hati pada pesakit dengan jangkitan mata virus sebelumnya yang ketara (mis. Herpes simplex) atau uveitis / iritis.
LUMIGAN belum dikaji pada pesakit dengan penyakit mata radang, neovaskular, radang, glaukoma sudut sempit, glaukoma kongenital atau glaukoma sudut akut.
Kutaneus
Terdapat potensi pertumbuhan rambut berlaku di kawasan di mana larutan LUMIGAN berulang kali bersentuhan dengan permukaan kulit. Oleh itu, penting untuk menggunakan LUMIGAN mengikut arahan dan untuk mengelakkannya berlumuran di pipi atau kawasan kulit yang lain.
Pernafasan
LUMIGAN belum dikaji pada pesakit dengan gangguan fungsi pernafasan. Walaupun maklumat terhad tersedia pada pesakit dengan riwayat asma atau COPD, eksaserbasi asma, dyspnoea dan COPD, serta kes asma, telah dilaporkan dalam tempoh selepas pemasaran. Kekerapan gejala ini tidak diketahui. Pesakit dengan COPD, asma, atau gangguan fungsi pernafasan kerana keadaan lain harus dirawat dengan berhati-hati.
Kardiovaskular
LUMIGAN belum dikaji pada pesakit dengan blok jantung gred 1 yang lebih besar atau kegagalan jantung kongestif yang tidak terkawal. Sejumlah laporan spontan bradikardia atau hipotensi telah direkodkan dengan larutan tetes mata 0,3 mg / ml bimatoprost. LUMIGAN harus digunakan dengan berhati-hati pada pesakit yang terdedah kepada bradikardia atau hipotensi.
Maklumat lain
Dalam kajian bimatoprost 0.3 mg / ml pada pesakit dengan glaukoma atau hipertensi okular ditunjukkan bahawa pendedahan mata yang lebih kerap kepada lebih daripada satu dos bimatoprost sehari dapat menurunkan kesan penurunan IOP (lihat bahagian 4.5) Pesakit menggunakan LUMIGAN bersama dengan analog prostaglandin lain harus dipantau untuk perubahan tekanan intraokular.
LUMIGAN 0.1 mg / ml mengandungi benzalkonium klorida (200 ppm) sebagai pengawet, yang dapat diserap oleh kanta lekap lembut. Kerana adanya benzalkonium klorida, kerengsaan mata dan perubahan warna kanta lekap lembut juga boleh berlaku. Kanta lekap mesti dikeluarkan sebelum disemai dan digunakan semula 15 minit selepas pentadbiran.
Benzalkonium klorida, biasanya digunakan sebagai pengawet dalam produk perubatan oftalmik, telah dilaporkan menyebabkan keratopati punat dan / atau keratopati ulseratif toksik. Oleh kerana LUMIGAN 0.1 mg / ml mengandungi 200 ppm benzalkonium klorida (empat kali kepekatan yang terdapat dalam bimatoprost 0.3 mg / ml tetes mata), ia harus digunakan dengan berhati-hati pada pasien dengan mata kering atau yang korneanya mungkin terganggu dan pada pesakit yang menggunakan pelbagai mata titisan yang mengandungi benzalkonium klorida. Sebagai tambahan, bagi pesakit ini, pemantauan klinikal diperlukan sekiranya penggunaan ubat berpanjangan.
Kes keratitis bakteria telah dilaporkan berkaitan dengan penggunaan wadah multidosis produk oftalmik topikal. Bekas ini secara tidak sengaja telah dicemari oleh pesakit yang, dalam kebanyakan kes, mempunyai penyakit okular yang bersamaan. Pesakit yang mengalami degradasi permukaan epitel okular berisiko lebih besar mengidap keratitis bakteria.
Arahkan pesakit untuk mengelakkan hujung bekas penghantaran tidak menyentuh mata atau struktur sekitarnya untuk mengelakkan kecederaan mata dan pencemaran larutan.
04.5 Interaksi dengan produk ubat lain dan bentuk interaksi lain -
Tidak ada kajian interaksi yang dilakukan.
Tidak ada interaksi yang diharapkan pada manusia kerana, setelah pemberian tetesan mata bimatoprost 0,3 mg / ml, larutan, kepekatan sistemik bimatoprost sangat rendah (kurang dari 0,2 ng / ml). Bimatoprost ditransformasikan melalui sistem enzim yang berlainan Dalam kajian praklinikal, tiada kesan pada enzim hepatik yang bertanggungjawab untuk metabolisme ubat.
Dalam kajian klinikal, bimatoprost 0,3 mg / ml, tetes mata, larutan digunakan bersamaan dengan beberapa produk perubatan oftalmik penyekat beta tanpa bukti interaksi.
LUMIGAN belum dinilai dalam terapi antiglaucoma tambahan dengan agen selain beta-blocker topikal.
Kesan penurunan IOP analog prostaglandin (contohnya LUMIGAN) mungkin kurang pada pesakit dengan glaukoma atau hipertensi okular apabila digunakan bersamaan dengan analog prostaglandin yang lain (lihat bahagian 4.4).
04.6 Kehamilan dan penyusuan susu ibu -
Kehamilan
Tidak ada data yang mencukupi mengenai penggunaan bimatoprost pada wanita hamil. Kajian haiwan menunjukkan ketoksikan pembiakan pada dos toksik ibu yang tinggi (lihat bahagian 5.3).
LUMIGAN tidak boleh digunakan semasa mengandung kecuali dalam kes keperluan mutlak.
Masa makan
Tidak diketahui sama ada bimatoprost dikeluarkan dalam susu manusia. Kajian haiwan menunjukkan bahawa bimatoprost dikeluarkan dalam susu ibu.Keputusan mesti dibuat sama ada untuk menghentikan penyusuan susu ibu atau menghentikan terapi LUMIGAN dengan mengambil kira faedah menyusui anak dan manfaat terapi untuk wanita.
Kesuburan
Tidak ada data mengenai kesan bimatoprost pada kesuburan manusia.
04.7 Kesan keupayaan memandu dan menggunakan mesin -
LUMIGAN mempunyai pengaruh yang tidak dapat diabaikan pada kemampuan memandu dan menggunakan mesin. Seperti rawatan oftalmik lain, jika penglihatan kabur sementara berlaku semasa penggunaan titisan, pesakit harus menunggu sehingga sebelum memandu atau mengoperasikan mesin. Penglihatan menjadi jelas kembali.
04.8 Kesan yang tidak diingini -
Dalam kajian klinikal fasa III selama 12 bulan, kira-kira 38% pesakit yang dirawat dengan titisan mata LUMIGAN 0,1 mg / ml, larutan mengalami reaksi buruk. Reaksi buruk yang paling sering dilaporkan adalah hiperemia konjungtiva (terutama sangat ringan hingga ringan dan diyakini tidak bersifat radang), yang terjadi pada 29% pesakit. Semua "kira-kira 4% pesakit menghentikan rawatan disebabkan oleh kejadian buruk pada kajian selama 12 bulan.
Reaksi buruk berikut telah dilaporkan dalam kajian klinikal dengan titisan mata LUMIGAN 0.1 mg / ml, larutan atau dalam tempoh selepas pemasaran. Sebilangan besar kesan okular ringan, dan tidak ada yang teruk.
Sangat biasa (≥1 / 10); biasa (≥1 / 100,
Jadual 1.
Dalam ujian klinikal, lebih daripada 1.800 pesakit menerima rawatan dengan LUMIGAN 0.3 mg / ml. Menggabungkan monoterapi fasa III dan data tambahan dengan LUMIGAN 0.3 mg / ml, tindak balas buruk yang paling kerap berlaku termasuk:
• pertumbuhan bulu mata hingga 45% pada tahun pertama dengan kejadian kes baru menurun menjadi 7% pada 2 tahun dan 2% pada 3 tahun
• hiperemia konjungtiva (terutama sangat ringan hingga ringan dan diyakini tidak bersifat radang) hingga 44% pada tahun pertama dengan kejadian kes baru menurun menjadi 13% pada 2 tahun dan menjadi 12% pada 3 tahun
• gatal mata hingga 14% pesakit pada tahun pertama dengan kejadian yang menurun hingga 3% pada 2 tahun dan 0% pada 3 tahun. Kurang daripada 9% pesakit terpaksa menghentikan rawatan kerana reaksi buruk pada tahun pertama dengan kejadian pesakit baru menghentikan rawatan sebanyak 3% pada kedua dan 3 tahun.
Jadual 2 melaporkan tindak balas buruk tambahan yang dilihat dengan LUMIGAN 0.3 mg / ml. Jadual ini juga merangkumi reaksi buruk yang berlaku dengan kedua-dua formulasi tetapi dengan frekuensi yang berbeza. Sebilangan besar kesan okular ringan hingga sederhana, dan tidak ada yang teruk.
Dalam setiap kelas frekuensi, reaksi buruk dilaporkan mengikut urutan penurunan.
Jadual 2.
Reaksi buruk yang dilaporkan dengan titisan mata yang mengandungi fosfat:
Kes kalsifikasi kornea yang berkaitan dengan penggunaan titisan mata yang mengandung fosfat jarang sekali dilaporkan pada beberapa pesakit dengan kornea yang teruk.
Melaporkan tindak balas buruk yang disyaki
Melaporkan tindak balas buruk yang disyaki berlaku setelah kebenaran produk ubat adalah penting kerana ia memungkinkan pemantauan berterusan terhadap keseimbangan manfaat / risiko produk ubat tersebut.Para profesional kesihatan diminta melaporkan sebarang reaksi buruk yang disyaki melalui sistem pelaporan nasional.
04.9 Overdosis -
Tidak ada kes overdosis yang dilaporkan dan tidak mungkin berlaku dengan penggunaan oftalmik.
Sekiranya berlaku overdosis, rawatan harus simtomatik dan menyokong. Sekiranya LUMIGAN tertelan secara tidak sengaja, mungkin berguna untuk mengetahui bahawa: Dalam kajian dua minggu pada tikus dan tikus didapati bahawa pemberian oral sehingga 100 mg / kg / hari tidak menyebabkan ketoksikan. Dos ini dinyatakan dalam mg / m² sekurang-kurangnya 210 kali lebih tinggi daripada dos yang terdapat dalam sebotol LUMIGAN 0.1 mg / ml titisan mata, larutan secara tidak sengaja diberikan kepada anak 10 kg.
05.0 HARTA FARMAKOLOGI -
05.1 "Sifat farmakodinamik -
Kumpulan farmakoterapi: oftalmologi, analog prostaglandin, kod ATC: S01EE03
Mekanisme tindakan
Mekanisme tindakan yang mana bimatoprost mengurangkan tekanan intraokular pada manusia dinyatakan dalam meningkatkan aliran humor berair trabekular dan uveo-scleral. Pengurangan tekanan intraokular bermula kira-kira 4 jam selepas pemberian pertama, kesan maksimum dicapai sekitar 8-12 jam.Kesannya berlangsung sekurang-kurangnya 24 jam.
Bimatoprost adalah agen hipotensi okular yang kuat. Ia adalah prostamida sintetik, berkaitan secara struktural dengan prostaglandin F2α (PGF2α), tetapi tidak bertindak melalui mana-mana reseptor prostaglandin yang diketahui. Bimatoprost secara selektif meniru kesan bahan biosintetik yang baru ditemui yang disebut prostamides. Reseptor prostamidal, bagaimanapun, belum dikenal pasti secara struktural.
Semasa kajian penting selama 12 bulan pada orang dewasa yang dirawat dengan titisan mata LUMIGAN 0,1 mg / ml, nilai purata IOP diurnal yang diukur pada setiap lawatan sepanjang tempoh kajian 12 bulan berbeza tidak lebih daripada 1.1 mmHg selama tempoh tersebut. sehari dan tidak pernah melebihi 17.7 mmHg.
LUMIGAN 0.1 mg / ml titisan mata mengandungi benzalkonium klorida dalam kepekatan 200 ppm.
Pengalaman terhad wujud dengan penggunaan LUMIGAN pada pesakit dengan glaukoma sudut pseudoexfoliative dan pigmentary, dan glaukoma penutupan sudut kronik dengan iridotomi paten.
Tidak ada kesan yang berkaitan secara klinikal terhadap denyut jantung dan tekanan darah semasa ujian klinikal.
Populasi kanak-kanak
Keselamatan dan keberkesanan LUMIGAN pada kanak-kanak berumur 0 hingga 18 tahun belum terbukti.
05.2 "Sifat farmakokinetik -
Penyerapan
In vitro bimatoprost menembusi kornea dan sklera manusia dengan baik. Selepas pentadbiran okular pada orang dewasa, pendedahan sistemik terhadap bimatoprost sangat rendah tanpa fenomena pengumpulan dari masa ke masa. Selepas pemberian harian satu tetes bimatoprost 0.3 mg / ml di kedua mata, untuk jangka masa dua minggu, darah konsentrasi memuncak dalam masa 10 beberapa minit selepas penanaman dan jatuh di bawah had pengesanan yang lebih rendah (0,025 ng / mL) dalam masa 1.5 jam selepas pemberian dos. Nilai min Cmax dan AUC 0-24 jam serupa pada hari ke-7 dan 14, dan masing-masing kira-kira 0.08 ng / mL dan 0.09 ng • h / mL; nilai-nilai ini menunjukkan bahawa kepekatan bimatoprost berterusan dicapai pada minggu pertama pentadbiran okular.
Pembahagian
Bimatoprost diedarkan secara sederhana ke tisu badan dan jumlah pengedaran sistemik pada manusia pada keadaan stabil adalah 0,67 l / kg. Dalam darah manusia, bimatoprost terutama terdapat dalam plasma. Pengikatan protein plasma bimatoprost adalah sekitar 88%.
Biotransformasi
Selepas pentadbiran okular, bimatoprost adalah komponen peredaran utama dalam darah, setelah peredaran sistemik dicapai. Bimatoprost, kemudian mengalami oksidasi, N-deetilasi dan glukuronidasi, membentuk pelbagai metabolit.
Penghapusan
Bimatoprost dihilangkan terutamanya oleh perkumuhan buah pinggang, sehingga 67% dari dos intravena yang diberikan kepada sukarelawan yang sihat dikeluarkan melalui air kencing, 25% dari dos tersebut dikeluarkan melalui najis. Separuh hayat penghapusan, ditentukan selepas pemberian intravena, kira-kira 45 minit; jumlah pelepasan darah adalah 1.5 L / jam / kg.
Ciri khas pada pesakit tua
Selepas dua dos harian bimatoprost 0.3 mg / ml tetes mata, larutan, nilai AUC0-24hr purata 0.0634 ng • h / ml bimatoprost pada pesakit tua (subjek berumur 65 tahun ke atas) jauh lebih tinggi. Berbanding dengan nilai sebanyak 0.0218 ng • h / ml dijumpai pada pesakit muda yang sihat. Walau bagaimanapun, hasil ini tidak penting secara klinikal kerana pendedahan sistemik pada orang tua dan muda tetap sangat rendah dengan pentadbiran okular. Tidak ada pengumpulan bimatoprost dalam darah dengan berlalunya masa, sementara profil keselamatan adalah sama pada kedua orang tua dan pesakit muda.
05.3 Data keselamatan praklinikal -
Kesan dalam kajian bukan klinikal diperhatikan hanya pada pendedahan yang dianggap signifikan melebihi pendedahan maksimum manusia, menunjukkan sedikit kaitan klinikal.
Pada monyet, pemberian bimatoprost okular setiap hari pada kepekatan ≥ 0.3 mg / ml selama satu tahun menyebabkan peningkatan pigmentasi iris dan kesan periokular yang bergantung kepada dos, yang ditandai dengan pelebaran sulkus dan fisur atas dan / atau bawah yang menonjol. Mekanisme peningkatan pigmentasi iris tampaknya disebabkan oleh peningkatan rangsangan dalam pengeluaran melanin dalam melanosit dan bukan pada peningkatan jumlah melanosit. Tidak ada perubahan fungsional atau mikroskopik yang berkaitan dengan kesan periokular, dan mekanisme tindakan tidak diketahui.berkaitan dengan perubahan periokular yang dijumpai.
Dalam satu siri kajian secara in vitro Dan dalam vivo bimatoprost tidak mutagenik atau karsinogenik.
Bimatoprost tidak menjejaskan kesuburan pada tikus pada dos hingga 0,6 mg / kg / hari (sekurang-kurangnya 103 kali dos manusia digunakan). Dalam kajian perkembangan embrio / janin, pengguguran diperhatikan, tetapi bukan kesan perkembangan, pada tikus dan tikus pada dos yang masing-masing sekurang-kurangnya 860 atau 1,700 kali lebih tinggi daripada dos manusia. Dos ini mengakibatkan pendedahan sistemik sekurang-kurangnya 33 atau 97 kali lebih tinggi, masing-masing, daripada yang ditunjukkan untuk manusia. Dalam kajian peri / postnatal pada tikus, ketoksikan ibu menyebabkan tempoh kehamilan yang pendek, kematian janin dan penurunan berat badan anak anjing, pada dos ≥ 0.3 mg / kg / hari (sekurang-kurangnya 41 kali yang ditunjukkan untuk manusia). Fungsi neuro-tingkah laku keturunan tidak terlibat.
06.0 MAKLUMAT FARMASI -
06.1 Eksipien -
Benzalkonium klorida
Natrium klorida
Dibasic sodium phosphate heptahydrate
Asid sitrat monohidrat
Asid hidroklorik atau natrium hidroksida (untuk menyesuaikan pH)
Air yang disucikan
06.2 Ketidaksesuaian "-
Tidak relevan.
06.3 Tempoh sah "-
2 tahun.
4 minggu selepas pembukaan pertama.
06.4 Langkah berjaga-jaga khas untuk penyimpanan -
Produk ubat ini tidak memerlukan syarat penyimpanan khas.
06.5 Sifat pembungkusan segera dan kandungan bungkusan -
Botol polietilena berketumpatan rendah putih susu dengan penutup skru polistirena.
Setiap botol mempunyai isi padu 3ml.
Saiz pek berikut boleh didapati: kadbod yang mengandungi 1 atau 3 botol larutan 3 ml.
Tidak semua saiz pek boleh dipasarkan.
06.6 Arahan penggunaan dan pengendalian -
Tiada arahan khas untuk pelupusan.
07.0 PEMEGANG "KEBENARAN PEMASARAN" -
Allergan Pharmaceuticals Ireland
Jalan Castlebar
Westport
Co.Mayo
Ireland
08.0 NOMBOR KEBENARAN PEMASARAN -
EU / 1/02/205 / 003-004
035447022
035447034
09.0 TARIKH KEBENARAN ATAU PEMBAHARUAN KEBENARAN -
7 Januari 2010
10.0 TARIKH ULASAN TEKS -
D.CCE Januari 2016















.jpg)