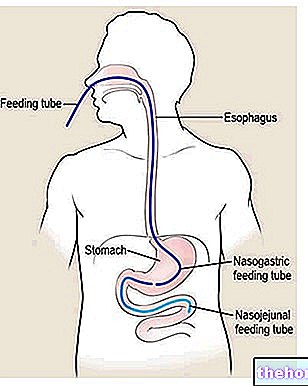
Bahan aktif: Vaksin influenza disiapkan dengan virus berpecah "berpecah", musim 2015/2016 yang tidak aktif
Vaxigrip, suspensi untuk suntikan dalam picagari yang diisi sebelumnya
Petunjuk Mengapa Vaxigrip digunakan? Untuk apa itu?
Vaxigrip adalah vaksin.
Vaksin ini membantu melindungi anda atau anak anda daripada selesema.
Penggunaan Vaxigrip harus berdasarkan kepada cadangan rasmi.
Apabila seseorang diberi Vaxigrip sistem kekebalan tubuh (sistem pertahanan semula jadi tubuh) akan menghasilkan perlindungannya sendiri (antibodi) terhadap penyakit tersebut. Tiada komponen yang terdapat dalam vaksin yang boleh menyebabkan selesema.
Influenza adalah penyakit yang dapat menyebar dengan cepat dan disebabkan oleh pelbagai jenis virus yang boleh berubah setiap tahun. Inilah sebabnya mengapa anda atau anak anda mungkin perlu diberi vaksin setiap tahun. "Selesema berlaku pada bulan-bulan dingin, antara bulan Oktober dan Maret. Sekiranya anda atau anak anda tidak diberi vaksin pada musim gugur, masih wajar untuk melakukan vaksinasi hingga musim semi, kerana anda atau anak anda menghadapi risiko terkena selesema hingga tahun ini. Doktor anda akan dapat memberi nasihat mengenai masa terbaik untuk vaksinasi.
Vaxigrip ditunjukkan untuk melindungi anda atau anak anda dari tiga jenis virus yang terkandung dalam vaksin bermula kira-kira 2-3 minggu setelah vaksinasi.
Tempoh inkubasi untuk selesema adalah beberapa hari, jadi jika anda atau anak anda terkena selesema segera sebelum atau setelah divaksinasi, anda atau anak anda masih boleh mendapat penyakit ini.
Vaksin tidak akan melindungi anda atau anak anda dari selesema, walaupun beberapa gejala serupa dengan selesema.
Kontraindikasi Apabila Vaxigrip tidak boleh digunakan
Untuk memastikan bahawa Vaxigrip adalah vaksin yang sesuai untuk anda atau anak anda, adalah penting untuk memberitahu doktor atau ahli farmasi anda jika anda atau anak anda mempunyai salah satu syarat yang disenaraikan di bawah. Sekiranya ada maklumat yang tidak jelas, tanyakan penjelasan doktor atau ahli farmasi anda.
Jangan gunakan Vaxigrip
- Sekiranya anda atau anak anda alah (hipersensitif):
- bahan aktif, atau
- ke mana-mana ramuan lain dari vaksin ini, (disenaraikan dalam bahagian 6), atau
- kepada komponen yang mungkin terdapat dalam jumlah yang sangat kecil seperti telur (ovalbumin atau, protein ayam), neomycin, formaldehid atau 9-octoxinol,
- Sekiranya anda atau anak anda mempunyai penyakit dengan demam tinggi atau sederhana atau penyakit akut, vaksinasi harus ditunda sehingga anda atau anak anda pulih.
Langkah berjaga-jaga untuk penggunaan Apa yang perlu anda ketahui sebelum mengambil Vaxigrip
Bercakap dengan doktor atau ahli farmasi anda sebelum anda diberi Vaxigrip
Beritahu doktor anda sebelum vaksinasi jika anda atau anak anda mempunyai:
- tindak balas imun yang berkurang (kekurangan imuniti atau mengambil ubat-ubatan yang mempengaruhi sistem imun).
- masalah lebam atau pendarahan
Doktor anda akan memutuskan sama ada anda atau anak anda harus menerima vaksin.
Sekiranya, atas sebab apa pun, anda atau anak anda menjalani ujian darah beberapa hari selepas vaksinasi selesema, sila beritahu doktor anda. Ini penting kerana hasil positif palsu telah diperhatikan pada beberapa pesakit yang baru-baru ini diberi vaksin.
Seperti semua vaksin, Vaxigrip mungkin tidak melindungi sepenuhnya semua orang yang telah divaksin.
Interaksi Ubat atau makanan mana yang boleh mengubah kesan Vaxigrip
Beritahu doktor atau ahli farmasi anda jika anda atau anak anda mengambil atau baru-baru ini mengambil vaksin atau ubat lain,
- Vaxigrip dapat diberikan secara serentak dengan vaksin lain dengan menyuntik ke anggota badan yang berlainan. Perlu dipertimbangkan bahawa, dalam kes ini, kejadian buruk mungkin lebih kuat.
- Tindak balas imunologi dapat dikurangkan ketika dirawat dengan ubat imunosupresif, seperti kortikosteroid, ubat sitotoksik atau radioterapi.
Amaran Penting untuk mengetahui bahawa:
Kehamilan dan penyusuan
Sekiranya anda hamil atau menyusu, fikir anda mungkin mengandung atau merancang untuk mempunyai bayi, minta nasihat doktor atau ahli farmasi anda sebelum menerima ubat ini.
Vaksin selesema boleh digunakan pada semua peringkat kehamilan. Berbanding dengan suku pertama, satu set data keselamatan yang lebih besar tersedia untuk suku kedua dan ketiga; namun, data dari penggunaan vaksin influenza di seluruh dunia tidak menunjukkan bahawa vaksin tersebut boleh memberi kesan berbahaya kepada ibu atau bayi.
Vaxigrip boleh diberikan jika anda menyusu. Doktor / ahli farmasi anda akan memutuskan sama ada anda harus diberi vaksin dengan Vaxigrip.
Memandu dan menggunakan mesin
Vaxigrip tidak mempunyai atau tidak dapat mempengaruhi kemampuan memandu atau menggunakan mesin.
Vaxigrip mengandungi kalium dan natrium
Ubat ini mengandungi kurang dari 1 mmol kalium (39 mg) dan natrium (23 mg) setiap dos, oleh itu ia pada dasarnya "bebas kalium" dan "bebas natrium".
Dos, Kaedah dan Masa Pentadbiran Cara menggunakan Vaxigrip: Posologi
Dos
Dewasa harus menerima dos 0.5 ml.
Gunakan pada kanak-kanak
Kanak-kanak berumur 36 bulan dan lebih tua harus menerima dos 0.5 ml.
Bayi berumur 6 hingga 35 bulan diberi dos 0.25 ml.
Sekiranya diperlukan oleh cadangan nasional, dos 0.5 ml dapat diberikan.
Sekiranya anak anda berusia kurang dari 9 tahun dan sebelumnya tidak pernah diberi vaksin terhadap influenza, dos kedua vaksin harus diberikan setelah selang waktu sekurang-kurangnya 4 minggu.
Kaedah dan kaedah pentadbiran
Doktor anda akan memberikan dos vaksin yang disyorkan melalui suntikan subkutan dalam atau intramuskular.
Tanya doktor atau ahli farmasi anda jika anda mempunyai pertanyaan lebih lanjut mengenai penggunaan ubat ini.
Overdosis Apa yang perlu dilakukan jika anda mengambil terlalu banyak Vaxigrip
Dalam beberapa kes, lebih banyak daripada dos yang disyorkan digunakan.
Dalam kes ini, ketika kesan sampingan dilaporkan, informasi tersebut sesuai dengan apa yang dijelaskan dalam Bahagian 4.
Kesan Sampingan Apakah kesan sampingan Vaxigrip
Seperti semua ubat, vaksin ini boleh menyebabkan kesan sampingan, walaupun tidak semua orang mendapatnya.
Reaksi alahan
Berjumpa doktor dengan SEGERA sekiranya anda atau anak anda melaporkan:
- Reaksi alahan yang teruk:
- Reaksi alergi yang teruk yang boleh menyebabkan kecemasan perubatan dengan tekanan darah rendah, pernafasan cepat dan cetek, degupan jantung yang cepat dan nadi lemah, kulit sejuk dan berkeringat, pening, yang boleh menyebabkan keruntuhan (kejutan).
- Pembengkakan kepala dan leher yang lebih ketara, termasuk muka, bibir, lidah, tekak atau bahagian badan yang lain, yang boleh menyebabkan kesukaran menelan atau bernafas (angioedema)
- Reaksi alahan seperti:
- reaksi kulit yang boleh merebak ke seluruh badan dengan gatal-gatal, gatal-gatal, ruam, kemerahan (eritema).
Kesan sampingan ini jarang berlaku (boleh mempengaruhi sehingga 1 dari 1.000 orang), kecuali gatal-gatal yang dilaporkan tidak biasa (boleh mempengaruhi hingga 1 dari 100 orang) pada kanak-kanak berumur 3 hingga 8 tahun.
Kesan sampingan lain yang dilaporkan
Sangat biasa (boleh mempengaruhi lebih dari 1 dari 10 orang) pada orang dewasa dan orang tua:
- Sakit kepala
- Sakit otot
- Perasaan umum yang tidak biasa menjadi tidak sihat, letih atau lemah
- Reaksi di tempat suntikan: sakit, kemerahan, bengkak, kekerasan, gatal-gatal
Sangat biasa (boleh mempengaruhi lebih daripada 1 dari 10 orang) pada populasi pediatrik *:
- Sakit kepala menangis yang tidak biasa, mudah marah, mengantuk
- Sakit otot
- Cirit-birit
- Mengurangkan atau kehilangan selera makan
- Perasaan umum tidak sihat, demam, gegaran
- Tindak balas di tempat suntikan: sakit, kemerahan, bengkak, kekerasan
Biasa (boleh mempengaruhi sehingga 1 dari 10 orang) pada orang dewasa dan orang tua:
- Sakit pada sendi
- Berpeluh bertambah
- Tindak balas tapak suntikan: lebam, gatal-gatal
- Menggigil, demam, perasaan tidak sihat, keletihan atau kelemahan yang tidak biasa
Biasa (boleh mempengaruhi sehingga 1 dari 10 orang) pada populasi pediatrik *:
- Pening
- Insomnia
- Dia mencuba semula
- Demam, menggigil, Reaksi di tempat suntikan: lebam, gatal, rasa tidak selesa, bengkak, kehangatan
Tidak biasa (boleh mempengaruhi sehingga 1 dari 100 orang) pada orang dewasa dan orang tua:
- Bengkak kelenjar di leher, ketiak atau pangkal paha
- Mengantuk, pening
- Rasa sakit (loya), cirit-birit
- Sindrom seperti selesema
- Reaksi di tempat suntikan: berasa sakit, kehangatan
Tidak biasa (boleh mempengaruhi sehingga 1 dari 100 orang) pada populasi pediatrik *:
- Bengkak kelenjar di leher, ketiak atau pangkal paha
- Cirit-birit
- Tindak balas tapak suntikan: pendarahan, panas * Kanak-kanak / remaja berumur 6 bulan hingga 17 tahun
Jarang (boleh mempengaruhi sehingga 1 dari 1000 orang) pada orang dewasa dan orang tua:
- Mati rasa atau pin dan jarum (paraesthesia), penurunan sensasi (hypoesthesia), mati rasa, sakit dan kelemahan pada lengan (radiculitis brachial), sakit saraf (neuralgia)
- Bengkak kelenjar di leher, ketiak atau pangkal paha
Frekuensi tidak diketahui (frekuensi tidak dapat dianggarkan dari data yang ada)
- Bengkak kelenjar di leher, ketiak atau pangkal paha
- Mati rasa atau pin dan jarum (paraesthesia)
- Kesakitan dilokalisasikan ke saluran saraf (neuralgia)
- Serangan (sawan)
- Gangguan neurologi yang boleh mengakibatkan kekakuan leher, kekeliruan, mati rasa, sakit dan kelemahan anggota badan, kehilangan keseimbangan, kehilangan refleks, kelumpuhan sebahagian atau seluruh badan (ensefalomielitis, neuritis, sindrom Guillain-Barré)
- Keradangan saluran darah (vaskulitis) yang boleh menyebabkan ruam kulit atau dalam kes yang jarang berlaku kepada masalah buah pinggang sementara
- Pengurangan sementara dalam jumlah jenis sel darah tertentu yang disebut platelet sebilangan kecil sel ini boleh menyebabkan lebam atau pendarahan yang berlebihan (trombositopenia sementara)
Kesan sampingan ini biasanya berlaku dalam 3 hari selepas vaksinasi dan hilang dalam 1 hingga 3 hari tanpa rawatan. Sebilangan besar kesan sampingan ini adalah intensiti ringan atau sederhana.
Pada orang dewasa
Pada orang tua
Dari umur 6 hingga 35 bulan
Dari umur 3 hingga 8 tahun
Umur 9 hingga 17 tahun
Dari usia 6 bulan hingga 17 tahun
Melaporkan kesan sampingan
Sekiranya anda atau anak anda mendapat kesan sampingan, berbincanglah dengan doktor atau ahli farmasi anda. Ini termasuk kemungkinan kesan sampingan yang tidak disenaraikan dalam risalah ini. Anda juga boleh melaporkan kesan sampingan secara langsung melalui sistem pelaporan nasional di https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse
Dengan melaporkan kesan sampingan, anda dapat membantu memberikan lebih banyak maklumat mengenai keselamatan ubat ini.
Tamat Tempoh dan Pengekalan
Jauhkan vaksin ini dari jarak dan pandangan kanak-kanak.
Jangan gunakan vaksin ini selepas tarikh luput yang dinyatakan pada bungkusan selepas singkatan EXP. Tarikh luput merujuk pada hari terakhir bulan itu.
Simpan di dalam peti sejuk (2 ° C - 8 ° C). Jangan beku. Simpan jarum suntik di casing luar untuk melindunginya dari cahaya.
Jangan membuang ubat-ubatan melalui air buangan atau sampah isi rumah. Tanya ahli farmasi anda bagaimana membuang ubat yang tidak anda gunakan lagi. Ini akan membantu melindungi alam sekitar.
Apa yang mengandungi Vaxigrip
Bahan aktifnya adalah: Virus influenza ("split" yang tidak aktif) dari strain berikut *:
A / California / 7/2009 (H1N1) pdm 09 - regangan setara (A / California / 7/2009, NYMC X-179A). …… 15 mikrogram HA **
A / Switzerland / 9715293/2013 (H3N2) - regangan setara (A / Australia Selatan / 55/2014, IVR-175) ……. 15 mikrogram HA **
B / Phuket / 3073/2013 ……… ... 15 mikrogram HA **
Untuk dos 0.5 ml.
* ditanam telur ayam yang disenyawakan dari ladang ayam yang sihat
** hemagglutinin
Komposisi vaksin ini mematuhi cadangan WHO (Pertubuhan Kesihatan Sedunia) (hemisfera Utara) dan keputusan E.U. diterima pakai untuk musim 2015/2016.
Bahan-bahan lain adalah: larutan penyangga yang mengandungi natrium klorida, natrium fosfat dihidrat, kalium dihidrogen fosfat, kalium klorida, air untuk suntikan.
Apa rupa dan kandungan bungkusan Vaxigrip
Vaxigrip adalah suspensi suntikan yang terdapat dalam jarum suntikan 0,5 ml dalam pek 1, 10, 20 atau 50 unit. Tidak semua saiz pek boleh dipasarkan.
Vaksin, setelah digoncang dengan lembut, muncul sebagai cairan yang sedikit keputihan dan pudar.
Risalah Pakej Sumber: AIFA (Badan Perubatan Itali). Kandungan yang diterbitkan pada Januari 2016. Maklumat yang ada mungkin tidak terkini.
Untuk mempunyai akses ke versi paling terkini, disarankan untuk mengakses laman web AIFA (Badan Perubatan Itali). Penafian dan maklumat berguna.
01.0 NAMA PRODUK PERUBATAN
SUSPENSI VAXIGRIP UNTUK INJEKSI DALAM SYRINGE YANG DIHASILKAN
02.0 KOMPOSISI KUALITATIF DAN KUANTITATIF
Virus influenza ("split" yang tidak aktif) dari strain berikut *:
• A / California / 7/2009 (H1N1) pdm 09 - regangan setara (A / California / 7/2009, NYMC X-179A) .................... …………………………………… 15 mcg HA **
• A / Switzerland / 9715293/2013 (H3N2) - regangan setara (A / Australia Selatan / 55/2014, IVR-175) …………………. …………………………………… 15 mcg HA **
• B / Phuket / 3073/2013 …………………………………… ........ 15 mcg HA **
untuk dos 0.5 ml
* ditanam telur ayam yang disenyawakan dari ladang ayam yang sihat
** hemagglutinin
Vaksin ini mematuhi cadangan Pertubuhan Kesihatan Sedunia (untuk hemisfera utara) dan keputusan Kesatuan Eropah untuk musim 2015/2016.
Untuk senarai lengkap eksipien, lihat Bahagian 6.1.
VAXIGRIP mungkin mengandung jejak telur, seperti ovalbumin, dan neomycin, formaldehid dan 9-octoxinol, yang merupakan komponen yang digunakan selama proses pembuatan (lihat Bahagian 4.3).
03.0 BORANG FARMASI
Suspensi untuk suntikan dalam picagari yang diisi sebelumnya.
Vaksin, setelah digoncang dengan lembut, muncul sebagai cairan yang sedikit keputihan dan pudar.
04.0 MAKLUMAT KLINIKAL
04.1 Petunjuk terapeutik
Profilaksis selesema.
VAXIGRIP ditunjukkan pada orang dewasa dan kanak-kanak dari usia 6 bulan.
VAXIGRIP mesti digunakan sesuai dengan cadangan rasmi.
04.2 Posologi dan kaedah pentadbiran
Dos
Dewasa: 0.5 ml.
Populasi kanak-kanak
Kanak-kanak berumur lebih dari 36 bulan: 0.5 ml.
Kanak-kanak berumur 6 hingga 35 bulan: 0.25 ml. Data klinikal terhad. Lihat Bahagian 6.6 untuk maklumat lebih lanjut mengenai pemberian dos 0.25 mL.
Sekiranya diperlukan oleh cadangan nasional, dos 0.5 ml dapat diberikan.
Kanak-kanak di bawah usia 9 tahun yang belum pernah diberi vaksin harus diberi dos kedua setelah selang waktu sekurang-kurangnya 4 minggu.
Kanak-kanak berumur kurang dari 6 bulan: keselamatan dan keberkesanan VAXIGRIP pada kanak-kanak berumur kurang dari 6 bulan belum terbukti. Tidak ada data yang tersedia.
Kaedah pentadbiran
Imunisasi harus dilakukan dengan suntikan intramuskular atau subkutan.
Untuk orang dewasa dan kanak-kanak berumur lebih dari 36 bulan: tempat yang disyorkan untuk suntikan intramuskular adalah otot deltoid.
Untuk bayi berumur 12 hingga 35 bulan: Tempat yang disyorkan untuk suntikan intramuskular adalah kawasan anterolateral paha (atau otot deltoid jika jisim otot mencukupi).
Untuk bayi berumur 6 hingga 11 bulan: Tempat yang disyorkan untuk suntikan intramuskular adalah kawasan anterolateral paha.
Langkah berjaga-jaga yang harus diambil sebelum mengendalikan atau mentadbir produk ubat.
Untuk arahan mengenai penyediaan produk ubat sebelum pentadbiran, lihat Bahagian 6.6.
04.3 Kontraindikasi
Hipersensitiviti terhadap bahan aktif, kepada mana-mana eksipien yang disenaraikan dalam Bahagian 6.1 atau komponen mana pun yang terdapat dalam jumlah seperti telur (ovalbumin, protein ayam), neomycin, formaldehid dan 9-octoxinol.
Vaksinasi harus ditangguhkan sekiranya penyakit demam sederhana, akut atau teruk.
04.4 Amaran khas dan langkah berjaga-jaga yang sesuai untuk digunakan
Seperti semua vaksin suntikan, rawatan dan pengawasan perubatan yang sesuai harus selalu tersedia sekiranya berlaku reaksi anafilaksis setelah pemberian vaksin.
VAXIGRIP tidak boleh diberikan secara intravaskular.
Seperti semua vaksin yang diberikan secara intramuskular, vaksin harus diberikan dengan berhati-hati kepada individu dengan trombositopenia atau gangguan pendarahan, kerana pendarahan mungkin terjadi pada individu-individu ini setelah pemberian intramuskular.
Seperti vaksin lain, vaksinasi dengan VAXIGRIP mungkin tidak melindungi 100% individu yang mudah terdedah.
Tindak balas antibodi mungkin tidak mencukupi pada pesakit dengan imunosupresi endogen atau iatrogenik.
Gangguan dengan ujian serologi
Lihat Bahagian 4.5.
04.5 Interaksi dengan produk ubat lain dan bentuk interaksi lain
VAXIGRIP boleh diberikan pada masa yang sama dengan vaksin lain. Imunisasi mesti dilakukan pada anggota badan yang berlainan, mesti dipertimbangkan bahawa pemberian bersamaan dapat meningkatkan reaksi buruk.
Tindak balas imunologi dapat dikurangkan jika pesakit dirawat dengan ubat imunosupresif.
Setelah vaksinasi influenza, hasil positif palsu telah diperhatikan dalam ujian serologi untuk mengenal pasti antibodi terhadap HIV1, Hepatitis C dan, di atas semua, HTLV1, ketika dilakukan dengan kaedah ELISA. Teknik Western Blot memungkinkan untuk menolak Keputusan ELISA Positif Palsu Ini palsu sementara reaksi positif mungkin disebabkan oleh tindak balas IgM terhadap vaksin.
04.6 Kehamilan dan penyusuan
Kehamilan
Vaksin influenza yang tidak aktif dapat digunakan pada semua peringkat kehamilan. Set data keselamatan yang lebih luas tersedia untuk suku kedua dan ketiga daripada suku pertama; namun, data dari penggunaan vaksin influenza yang tidak aktif di seluruh dunia tidak menunjukkan kejadian buruk janin dan ibu yang disebabkan oleh vaksin tersebut.
Masa makan
VAXIGRIP boleh digunakan semasa menyusu.
Kesuburan
Data kesuburan tidak tersedia.
04.7 Kesan keupayaan memandu dan menggunakan mesin
VAXIGRIP tidak mempunyai atau tidak dapat mempengaruhi kemampuan memandu dan menggunakan mesin.
04.8 Kesan yang tidak diingini
ke. Ringkasan profil keselamatan
Dalam kajian klinikal baru-baru ini, kira-kira 10,000 subjek dari usia 6 bulan telah menerima VAXIGRIP.
Berdasarkan sejarah imunisasi dan usia kanak-kanak, dos dan jumlah dos berbeza (lihat populasi Pediatrik dalam subseksyen b. Jadual reaksi buruk).
Reaksi yang diminta biasanya berlaku dalam 3 hari pertama pentadbiran VAXIGRIP, diselesaikan secara spontan dalam 1 hingga 3 hari sejak permulaan. Sebilangan besar reaksi buruk yang diminta adalah intensiti ringan hingga sederhana.
Reaksi buruk yang paling kerap dilaporkan dalam masa 7 hari selepas suntikan VAXIGRIP adalah sakit di tempat suntikan di seluruh populasi kecuali pada bayi 6 hingga 35 bulan, di mana kerengsaan lebih kerap dilaporkan.
Reaksi buruk sistemik yang diminta paling kerap dilaporkan dalam masa 7 hari selepas suntikan VAXIGRIP adalah sakit kepala pada orang dewasa, orang tua dan kanak-kanak berumur 9 hingga 17 tahun dan malaise pada kanak-kanak berumur 3 hingga 8 tahun.
Reaksi buruk yang diminta pada amnya kurang kerap berlaku pada orang tua daripada pada orang dewasa.
b. Jadual tindak balas buruk
Data di bawah merangkum frekuensi tindak balas buruk yang direkodkan berikutan vaksinasi dengan VAXIGRIP semasa ujian klinikal dan semasa pengalaman selepas pemasaran di seluruh dunia.
Kejadian buruk dinilai berdasarkan kekerapan menggunakan konvensyen berikut:
Sangat biasa (≥1 / 10);
Biasa (≥1 / 100,
Tidak biasa (≥1 / 1,000 y
Jarang (≥1 / 10,000 y
Sangat jarang (
Tidak diketahui (tidak dapat dianggarkan dari data yang ada).
Orang dewasa dan warga tua
Profil keselamatan di bawah didasarkan pada data daripada lebih daripada 4.300 orang dewasa dan 5,000 orang tua berusia lebih dari 60 tahun.
Jarang pada orang tua
Dilaporkan pada orang dewasa semasa ujian klinikal
Dilaporkan pada orang tua semasa ujian klinikal
Biasa pada orang tua
Tidak dikenali pada orang dewasa
Tidak dikenali di Warga emas
b. Populasi kanak-kanak
Bergantung pada sejarah imunisasi, kanak-kanak berumur 6 bulan hingga 8 tahun mendapat satu atau dua dos VAXIGRIP. Kanak-kanak dari usia 6 hingga 35 bulan menerima formulasi 0,25 ml, kanak-kanak dari usia 3 tahun menerima formulasi 0,5 ml.
• Kanak-kanak / remaja dari 3 hingga 17 tahun:
Profil keselamatan di bawah ini berdasarkan data yang diperoleh di lebih daripada 300 kanak-kanak berumur 3 hingga 8 tahun dan lebih kurang 70 kanak-kanak / remaja berusia 9 hingga 17 tahun.
Pada kanak-kanak berumur 3 hingga 8 tahun, reaksi buruk yang paling kerap dilaporkan dalam masa 7 hari selepas suntikan VAXIGRIP adalah rasa sakit / nyeri di tempat suntikan (56.3%), merasa sakit (27.3%), mialgia (25.5%) dan eritema / kemerahan di tempat suntikan (23.4%).
Pada kanak-kanak / remaja berusia 9 hingga 17 tahun, tindak balas buruk yang diminta yang paling sering dilaporkan dalam masa 7 hari selepas suntikan VAXIGRIP adalah rasa sakit / nyeri di tempat suntikan (54.5% hingga 70.6%), sakit kepala (22.4% hingga 23.6%), myalgia (12.7% hingga 17.6%) dan eritema / kemerahan di tempat suntikan (5.5% hingga 17.6%).
Data di bawah merangkum frekuensi tindak balas buruk yang dicatatkan pada kanak-kanak / remaja berusia 3 hingga 17 tahun selepas vaksinasi dengan VAXIGRIP semasa ujian klinikal dan semasa pengalaman selepas pemasaran di seluruh dunia.
Dilaporkan semasa ujian klinikal pada kanak-kanak berumur 3 hingga 8 tahun
Dilaporkan dalam ujian klinikal pada kanak-kanak / remaja berusia 9 hingga 17 tahun
Biasa pada kanak-kanak / remaja berumur 9 hingga 17 tahun
Sangat biasa pada kanak-kanak / remaja berumur 9 hingga 17 tahun
Tidak dikenali pada kanak-kanak / remaja berumur 9 hingga 17 tahun
• Kanak-kanak berumur 6 hingga 35 bulan:
Profil keselamatan yang dilaporkan di bawah adalah berdasarkan data yang diperoleh pada kira-kira 50 kanak-kanak berumur 6 hingga 35 bulan.
Dalam kajian klinikal, reaksi buruk yang paling kerap dilaporkan dalam tempoh 3 hari selepas suntikan VAXIGRIP adalah sakit di tempat suntikan (23.5%), mudah marah (23.5%), demam (20.6%) dan tangisan yang tidak biasa (20.6%).
Dalam kajian lain, reaksi buruk yang diminta yang paling sering dilaporkan dalam masa 7 hari selepas suntikan VAXIGRIP adalah kerengsaan (60%), demam (50%), selera makan menurun (35%) dan tangisan yang tidak biasa (30%).).
Data di bawah meringkaskan kekerapan tindak balas buruk yang direkodkan pada bayi berusia 6 hingga 35 bulan dalam masa 3 atau 7 hari selepas pemberian satu atau dua dos 0.25 ml VAXIGRIP, selama dua kajian klinikal ini dan semasa pengalaman selepas pemasaran di seluruh dunia:
Laporkan dalam masa 3 hari selepas suntikan VAXIGRIP
c. Populasi khas lain
Walaupun hanya sejumlah subjek dengan morbiditi bersama yang terdaftar, kajian dilakukan pada pesakit yang telah menjalani transplantasi ginjal, pesakit asma, atau kanak-kanak dari usia 6 bulan hingga 3 tahun dengan penyakit yang menyebabkan mereka berisiko tinggi untuk berkembang. komplikasi yang berkaitan dengan selesema yang teruk, tidak menunjukkan perbezaan yang besar dari segi profil keselamatan VAXIGRIP pada populasi ini.
Melaporkan tindak balas buruk yang disyaki
Pelaporan tindak balas buruk yang disyaki berlaku setelah kebenaran produk ubat adalah penting kerana ia memungkinkan pemantauan berterusan terhadap keseimbangan manfaat / risiko produk ubat tersebut. Profesional penjagaan kesihatan diminta untuk melaporkan sebarang reaksi buruk yang disyaki melalui sistem pelaporan nasional. "Alamat http: //www.agenziafarmaco.gov.it/it/responsabili.
04.9 Overdosis
Terdapat laporan pemberian ubat melebihi dos yang disyorkan (overdosis) dengan VAXIGRIP. Apabila reaksi buruk dilaporkan, maklumat tersebut sesuai dengan profil keselamatan VAXIGRIP yang telah dijelaskan di bahagian 4.8.
05.0 HARTA FARMAKOLOGI
05.1 Sifat farmakodinamik
Kumpulan farmakoterapi: Vaksin influenza
Kod ATC: J07BB02
Tindak balas imun antibodi biasanya disebabkan dalam 2-3 minggu. Tempoh imuniti pasca vaksinasi yang disebabkan adalah berbeza-beza tetapi umumnya antara 6 dan 12 bulan.
05.2 "Sifat farmakokinetik
Tidak berkaitan.
05.3 Data keselamatan praklinikal
Tidak berkaitan.
06.0 MAKLUMAT FARMASI
06.1 Eksipien
Penyelesaian penyangga:
natrium klorida, kalium klorida, disodium fosfat dihidrat, kalium dihidrogen fosfat, air untuk suntikan.
06.2 Ketidaksesuaian
Sekiranya tidak ada kajian keserasian, produk ubat ini tidak boleh dicampurkan dengan produk ubat lain.
06.3 Tempoh sah
1 tahun.
06.4 Langkah berjaga-jaga khas untuk penyimpanan
Simpan di dalam peti sejuk (2 ° C - 8 ° C). Jangan beku. Simpan jarum suntik di casing luar untuk melindunginya dari cahaya.
06.5 Sifat pembungkusan segera dan kandungan bungkusan
Suspensi 0.5 ml dalam jarum suntikan yang sudah diisi (kaca tipe I) dengan jarum pra-dikimpal, dengan meterai pelocok (chlorobromobutyl atau chlorobutyl atau bromobutyl elastomer) - saiz pek 1, 10, 20 atau 50.
Suspensi 0.5 ml dalam jarum suntikan yang sudah diisi (kaca tipe I) tanpa jarum, dengan meterai pelocok (chlorobromobutyl atau chlorobutyl atau bromobutyl elastomer) - saiz pek 1, 10, 20 atau 50.
Tidak semua saiz pek boleh dipasarkan.
06.6 Arahan penggunaan dan pengendalian
Vaksin mesti dibawa ke suhu bilik sebelum digunakan.
Goncang sebelum digunakan. Periksa secara visual sebelum pentadbiran.
Vaksin tidak boleh digunakan jika zarah asing diperhatikan dalam suspensi.
Arahan untuk pentadbiran 0.25 ml pada kanak-kanak dari usia 6 hingga 35 bulan
Apabila dosis 0.25 ml ditunjukkan, untuk menghilangkan separuh isi jarum suntik dari
0,5 ml, pegang jarum suntik tegak dan tekan penutup plunger sehingga anda mencapai garis nipis hitam yang dicetak pada picagari. Suntikan isi padu 0.25 ml. Lihat juga Bahagian 4.2.
Ubat yang tidak digunakan atau sisa yang berasal dari ubat ini mesti dibuang sesuai dengan peraturan tempatan.
07.0 PEMEGANG KEBENARAN PEMASARAN
Sanofi Pasteur MSD Snc
162 jalan Jean Jaurès 69007
Lyon (Perancis)
08.0 NOMBOR KEBENARAN PEMASARAN
"PENGGANTUNGAN YANG TIDAK DAPAT DIGUNAKAN UNTUK PENGGUNAAN INTRAMUSKULAR ATAU SUBUTANE" 20 SYRINGES YANG DIISI SEBELUM 0,5 ML DENGAN JENIS - AIC N. 026032286
"PENGGANTUNGAN YANG TIDAK DAPAT DIGUNAKAN UNTUK PENGGUNAAN INTRAMUSKULAR ATAU SUBUTANE" 1 SYRINGE YANG DIISI SEBELUM 0,5 ML DENGAN JENIS - AIC n. 026032209
"PENGGANTUNGAN YANG TIDAK DAPAT DIGUNAKAN UNTUK PENGGUNAAN INTRAMUSKULAR ATAU SUBSUTANEO" 1 SYRINGE YANG DIISI SEBELUM 0,5 ML DENGAN CAP BARU - AIC n. 026032375
"PENGGANTUNGAN YANG TIDAK DAPAT DIGUNAKAN UNTUK PENGGUNAAN INTRAMUSKULAR ATAU SUBUTAN" 1 SYRINGE YANG DIISI SEBELUM 0,5 ML TANPA PERLU - AIC n. 026032300
"PENGGANTUNGAN YANG TIDAK DAPAT DIGUNAKAN UNTUK PENGGUNAAN INTRAMUSKULAR ATAU SUBUTANE" 10 SYRINGES YANG DIISI SEBELUM 0,5 ML DENGAN JENIS - AIC n. 026032274
"PENGGANTUNGAN YANG TIDAK DAPAT DIGUNAKAN UNTUK PENGGUNAAN INTRAMUSKULAR ATAU SUBSUTANEO" 10 SYRINGES YANG DIISI SEBELUM 0,5 ML DENGAN CAP BARU - AIC N. 026032387
"PENGGANTUNGAN YANG TIDAK TERJADI UNTUK PENGGUNAAN INTRAMUSKULAR ATAU SUBUTAN" 10 SYRINGES YANG DIISI SEBELUM 0,5 ML TANPA PERLU - AIC N. 026032312
"PENGGANTUNGAN YANG TIDAK DAPAT DIGUNAKAN UNTUK PENGGUNAAN INTRAMUSKULAR ATAU SUBUTANE" 20 SYRINGES YANG DIISI SEBELUM 0,5 ML DENGAN CAP BARU - AIC N. 026032399
"PENGGANTUNGAN YANG TIDAK DAPAT DIGUNAKAN UNTUK PENGGUNAAN INTRAMUSKULAR ATAU SUBUTANE" 20 SYRINGES YANG DIISI SEBELUM 0,5 ML TANPA PERLU - AIC N. 026032324
"PENGGANTUNGAN YANG TIDAK DAPAT DIGUNAKAN UNTUK PENGGUNAAN INTRAMUSCULAR ATAU SUBUTANEO" 50 SYRINGES PRE-FILLED OF 0.5 ML WITH NEEDLE - AIC N. 026032298
"PENGGANTUNGAN YANG TIDAK DAPAT DIGUNAKAN UNTUK PENGGUNAAN INTRAMUSKULAR ATAU SUBUTANE" 50 SYRINGES YANG DIISI SEBANYAK 0,5 ML DENGAN CAP BARU - AIC N. 026032401
"PENGGANTUNGAN YANG TIDAK DAPAT DIGUNAKAN UNTUK PENGGUNAAN INTRAMUSKULAR ATAU SUBUTANE" 50 SYRINGES YANG DIISI SEBELUM 0,5 ML TANPA PERLU - AIC N. 026032336
09.0 TARIKH KEBENARAN ATAU PEMBAHARUAN KEBENARAN
Julai 1998 / Jun 2009
10.0 TARIKH SEMAKAN TEKS
Oktober 2015